科学探究题 较难0.4 引用1 组卷145
已知草酸(H2C2O4)固体与浓硫酸共热发生化学反应:H2C2O4 CO2↑+CO↑+H2O。某化学兴趣小组同学设计如下实验装置,用于制取纯净干燥的CO气体来还原氧化铁。请根据题目要求回答问题:
CO2↑+CO↑+H2O。某化学兴趣小组同学设计如下实验装置,用于制取纯净干燥的CO气体来还原氧化铁。请根据题目要求回答问题:
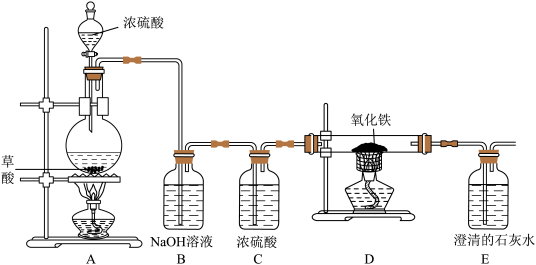
(1)实验开始时,应先点燃_____ 处的酒精灯(填装置序号)。
(2)装置B中的NaOH溶液的作用是_____ ,B、C装置的顺序不能颠倒的原因是_____ 。
(3)从环保角度考虑,上述实验的不足之处是_____ 。反应后玻璃管内固体粉末由红色全部变成黑色,小马同学认为该黑色固体全部是铁,但小军同学提出了质疑,于是小组内的同学们提出查阅资料,寻求真理。
【查阅资料】
①一氧化碳还原Fe2O3的固体产物的成分与反应的温度、时间有关,产物可能是Fe3O4、FeO、Fe;
②几种物质的性质,如下表所示:
③已知反应 :Fe3O4+8HCl=FeCl2+2FeCl3+4H2O, FeCl3溶液呈棕黄色。
【实验探究】
(4)该小组同学将反应后的黑色固体研细后,用磁铁吸引,发现黑色粉末全部被吸引,则该黑色粉末中不可能含有_____ (填化学式)。
(5)黑色固体的成分是什么?
猜想Ⅰ:全部为Fe; 猜想Ⅱ:全部为Fe3O4; 猜想Ⅲ:_____ (填化学式)。
实验:将黑色粉末加入到足量的稀硫酸中,固体全部溶解,观察现象:①有无色气泡产生,证明该固体中一定有_____ (填化学式);②溶液呈棕黄色。
(6)由上述实验现象,得出猜想_____ 正确。

(1)实验开始时,应先点燃
(2)装置B中的NaOH溶液的作用是
(3)从环保角度考虑,上述实验的不足之处是
【查阅资料】
①一氧化碳还原Fe2O3的固体产物的成分与反应的温度、时间有关,产物可能是Fe3O4、FeO、Fe;
②几种物质的性质,如下表所示:
| 物质化学式 | Fe | Fe2O3 | FeO | Fe3O4 |
| 物质的颜色 | 黑色 | 红色 | 黑色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
③已知反应 :Fe3O4+8HCl=FeCl2+2FeCl3+4H2O, FeCl3溶液呈棕黄色。
【实验探究】
(4)该小组同学将反应后的黑色固体研细后,用磁铁吸引,发现黑色粉末全部被吸引,则该黑色粉末中不可能含有
(5)黑色固体的成分是什么?
猜想Ⅰ:全部为Fe; 猜想Ⅱ:全部为Fe3O4; 猜想Ⅲ:
实验:将黑色粉末加入到足量的稀硫酸中,固体全部溶解,观察现象:①有无色气泡产生,证明该固体中一定有
(6)由上述实验现象,得出猜想
19-20九年级下·广西南宁·开学考试
类题推荐
某化学兴趣小组在实验室里探究某些酸碱盐的化学性质,分别做了如下实验:
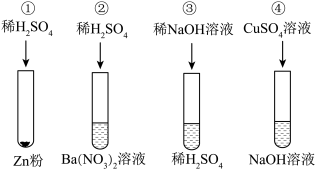
(1)实验①的反应现象是___________ 。
(2)实验④反应的化学方程式为___________ 。
(3)向试管③中滴加了过量的氢氧化钠溶液仍无明显现象,要证明二者已经发生反应,可选用___________(填字母)继续进行实验,以达到实验目的。
(4)小组同学将实验②③④三支试管反应后的物质倒入同一洁净的烧杯中,充分反应后过滤,分别得到沉淀A和无色滤液B。
I.沉淀A的成分是___________ 。(填化学式)
Ⅱ.同学们对无色滤液B继续进行实验,取滤液B于试管,加入足量Ba(NO3)2溶液,无明显现象,由此现象说明滤液B中一定没有的离子是___________ (填离子符号)。同学们经过讨论认为无色滤液B中离子的种类可能有多种情况,你认为溶液中最多含有的离子有___________ (填离子符号)。

(1)实验①的反应现象是
(2)实验④反应的化学方程式为
(3)向试管③中滴加了过量的氢氧化钠溶液仍无明显现象,要证明二者已经发生反应,可选用___________(填字母)继续进行实验,以达到实验目的。
| A.酚酞 | B.氯化钡溶液 | C.pH试纸 | D.碳酸钾溶液 |
I.沉淀A的成分是
Ⅱ.同学们对无色滤液B继续进行实验,取滤液B于试管,加入足量Ba(NO3)2溶液,无明显现象,由此现象说明滤液B中一定没有的离子是
为了测定实验室某生锈铁片中铁元素的质量分数,两位同学分别设计了如下甲、乙两个实验方案。方案甲:称得生锈铁片的质量为m1g,按图I所示装置进行实验。完全反应后,测得室温下产生氢气的体积为V1L,查得其密度为ρ1g/L.方案乙:称得生锈铁片的质量为m2g,先按图Ⅱ所示装置进行实验。当生锈铁片完全变成光亮的银白色时,停止加热,继续通入CO至室温。取出铁片,按图I所示装置继续进行实验。完全反应后,测得室温下产生氢气的体积为V2L,查得其密度为ρ2g/L。
已知: (FeCl3可溶于水)
(FeCl3可溶于水)
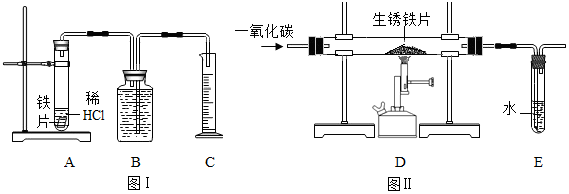
(1)铁锈的成分是______ 。
(2)【评价交流】上述两个方案中,可行的是______ (填“甲”或“乙”);分析不可行方案,其缺陷是______ 。
(3)【设计实验】方案乙中,同学们设计了如下实验报告,请帮助完成表中空格。
(4)图Ⅱ所示装置有缺陷,应如何改进______ 。
(5)【结论】生锈铁片中铁元素的质量分数是______ (用字母表示)。
(6)【发散】实验室经常用一氧化碳来炼铁,实验室炼的铁和工业炼的铁本质区别是______ 。
已知:

(1)铁锈的成分是
(2)【评价交流】上述两个方案中,可行的是
(3)【设计实验】方案乙中,同学们设计了如下实验报告,请帮助完成表中空格。
| 实验编号 | 实验步骤 | 实验现象 | 结论或化学方程式 |
| ①装置Ⅱ | 通入CO,加热。完全反应后,停止加热,继续通CO至室温 | 生锈铁片变成光亮的银白色 | CO具有 化学方程式: |
| ②装置Ⅰ | 将光亮铁片放入稀盐酸中,完全反应 |
(5)【结论】生锈铁片中铁元素的质量分数是
(6)【发散】实验室经常用一氧化碳来炼铁,实验室炼的铁和工业炼的铁本质区别是
小红同学在学习“金属的化学性质”实验操作时,发现几支试管中产生气泡的速率有的快有的慢。于是,她与小芳同学一起合作进行如下探究。
【提出问题】金属与酸反应的快慢受哪些因素影响?
【猜想与假设】猜想1:可能与酸的浓度有关。
猜想2:可能与金属的种类有关。
猜想3:可能与金属的形状有关。
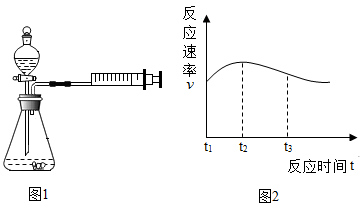
【设计并实验】为了验证猜想,小红和小芳设计如图1所示的装置进行如图实验:
(1)小红和小芳检查图1装置气密性的方法是________________ 。
(2)实验时须将镁片和铁片进行打磨的目的________________ 。
(3)写出镁与稀硫酸反应的化学方程式:________________ 。
【收集证据】
(4)要比较金属的形状对反应快慢的影响,应选择的实验编号是________________ 。
【得出结论】
(5)从上述实验数据可得出的结论是________________ 。
【评价与反思】
(6)测得实验①反应中产生气体的速率(v)与时间(t)的关系如图2所示,t2-t3时间段内反应速率逐渐减慢的主要原因是________________ 。
(7)铁与硫酸反应的快慢还受到温度的影响。请你设计实验验证:________________ (不要求写出现象和结论)。
【提出问题】金属与酸反应的快慢受哪些因素影响?
【猜想与假设】猜想1:可能与酸的浓度有关。
猜想2:可能与金属的种类有关。
猜想3:可能与金属的形状有关。
【设计并实验】为了验证猜想,小红和小芳设计如图1所示的装置进行如图实验:
(1)小红和小芳检查图1装置气密性的方法是
(2)实验时须将镁片和铁片进行打磨的目的
(3)写出镁与稀硫酸反应的化学方程式:
| 实验编号 | 硫酸的浓度(均取20mL) | 金属(均取2g) | 金属的形状 | 收集50mLH2所需时间s |
| ① | 10% | 镁 | 粉末状 | 60 |
| ② | 10% | 铁 | 片状 | 120 |
| ③ | 10% | 镁 | 片状 | 102 |
| ④ | 20% | 铁 | 片状 | 110 |
【收集证据】
(4)要比较金属的形状对反应快慢的影响,应选择的实验编号是
【得出结论】
(5)从上述实验数据可得出的结论是
【评价与反思】
(6)测得实验①反应中产生气体的速率(v)与时间(t)的关系如图2所示,t2-t3时间段内反应速率逐渐减慢的主要原因是
(7)铁与硫酸反应的快慢还受到温度的影响。请你设计实验验证:

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


