科学探究题 较难0.4 引用1 组卷62
工业上制取烧碱的方法之一是电解食盐水法,在生成烧碱的同时还在两电极上产生两种气体(经检验均不是氧气),则该反应的化学方程式为_____ 。
某化学小组在化工商店购得某品牌的烧碱样品,准备用于化学实验。当将其配制成溶液时,小刚同学观察包装袋标签发现了问题:根据生产日期,这包烧碱存放时间较长,会不会变质呢?于是对这包烧碱进行如下探究:
(一)这包烧碱含有什么成分?
(1)打开后发现样品表面出现一层白色粉末,初步判断已经变质,出现该现象的原因是_____ (用化学方程式表示)。
(2)小刚同学猜想:该包烧碱的成分可能是NaOH和Na2CO3也可能完全是Na2CO3。
(3)实验探究:
反思1:小红同学在实验完成后提出个人质疑:化学反应中的原料往往不能完全转化为产品,所以电解食盐水法制得的烧碱中往往会含有杂质_____ (填化学式)。
所以需要进行再探究:另取上述实验①中的上层清液,滴加足量稀硝酸和AgNO3溶液,产生白色沉淀,得出结论,说明小红的质疑是正确的。
反思2:小亮认为,小红的实验设计有缺陷,理由是_____ 。
(二)成分含量测定
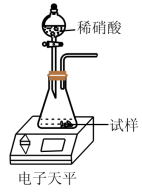
a.取样品mg放入如图装置中加水完全溶解,后放在电子天平上称量为m1g
b.打开分液漏斗活塞加入足量稀硝酸溶液,待反应停止再试样称量为m2g
c.根据化学方程式计算,样品中Na2CO3的质量分数=_____ (写出表达式即可,Na2CO3、CO2的相对分子质量分别为106、44)
某化学小组在化工商店购得某品牌的烧碱样品,准备用于化学实验。当将其配制成溶液时,小刚同学观察包装袋标签发现了问题:根据生产日期,这包烧碱存放时间较长,会不会变质呢?于是对这包烧碱进行如下探究:
(一)这包烧碱含有什么成分?
(1)打开后发现样品表面出现一层白色粉末,初步判断已经变质,出现该现象的原因是
(2)小刚同学猜想:该包烧碱的成分可能是NaOH和Na2CO3也可能完全是Na2CO3。
(3)实验探究:
| 实验操作 | 现象 | 结论 |
| ①取少量样品于试管中,完全溶于水,滴加过量的BaCl2溶液 | 产生白色沉淀 | 含有Na2CO3 |
| ②取①中上层清液,滴加 | 还含有NaOH |
所以需要进行再探究:另取上述实验①中的上层清液,滴加足量稀硝酸和AgNO3溶液,产生白色沉淀,得出结论,说明小红的质疑是正确的。
反思2:小亮认为,小红的实验设计有缺陷,理由是
(二)成分含量测定

a.取样品mg放入如图装置中加水完全溶解,后放在电子天平上称量为m1g
b.打开分液漏斗活塞加入足量稀硝酸溶液,待反应停止再试样称量为m2g
c.根据化学方程式计算,样品中Na2CO3的质量分数=
19-20九年级上·山东泰安·期末
类题推荐
实验室有两瓶常温下的饱和溶液,已知它们是氢氧化钠溶液和石灰水,为了区分并验证它们的性质,小强和小丽同学进行了如下探究实验。
探究一:小强同学用物理方法鉴别它们。他从两瓶溶液取出来少许装入试管并在酒精灯上加热。他根据_________ 现象,判断甲瓶为石灰水。
探究二:小丽同学用化学方法鉴别它们。她从两瓶溶液取出来少许装入试管并向里面吹气,也判断出甲瓶为石灰水,乙瓶中发生的化学反应方程式为__________ 。
探究三:乙瓶溶液敞口放在空气中可能变质。为了探究乙瓶是否变质以及变质后溶液中溶质的成分,两位同学做了如下猜测和实验。
【提出猜想】①只有NaOH ②只有Na2CO3 ③Na2CO3和NaOH ④…
【查阅资料】已知NaCl、CaCl2溶液呈中性,Na2CO3溶液能使酚酞变红。
【实验与结论】(1)取少许溶液并加入足量稀盐酸,看不到任何现象就可证明猜想①成立。
(2)若氢氧化钠溶液已经变质,要探究氢氧化钠溶液是否完全变质,现做如下实验。
【反思与交流】步骤1中所加溶液需过量的主要原因是__________ 。
探究一:小强同学用物理方法鉴别它们。他从两瓶溶液取出来少许装入试管并在酒精灯上加热。他根据
探究二:小丽同学用化学方法鉴别它们。她从两瓶溶液取出来少许装入试管并向里面吹气,也判断出甲瓶为石灰水,乙瓶中发生的化学反应方程式为
探究三:乙瓶溶液敞口放在空气中可能变质。为了探究乙瓶是否变质以及变质后溶液中溶质的成分,两位同学做了如下猜测和实验。
【提出猜想】①只有NaOH ②只有Na2CO3 ③Na2CO3和NaOH ④…
【查阅资料】已知NaCl、CaCl2溶液呈中性,Na2CO3溶液能使酚酞变红。
【实验与结论】(1)取少许溶液并加入足量稀盐酸,看不到任何现象就可证明猜想①成立。
(2)若氢氧化钠溶液已经变质,要探究氢氧化钠溶液是否完全变质,现做如下实验。
| 实验步骤 | 实验现象 | 实验结论或方程式 |
| 步骤1:取少量已变质的NaOH溶液于试管中, 加入过量的溶液。 | 白色浑浊 | 反应方程式: |
| 步骤2:取步骤1所得的澄清溶液少许,并向清液滴入几滴酚酞溶液。 | 猜想②成立 | |
| 猜想③成立 |
一次用餐中,小丽同学对“固体酒精”产生好奇,于是她对其进行研究。
【收集资料】①固体酒精中含有酒精、氢氧化钠、氯化钙等物质 ②酒精的化学式为C2H5OH
【提出问题】(1)酒精的化学式与NaOH相比,都有“OH”,那么酒精的水溶液是否显碱性?从下面试剂中选择合适试剂进行鉴别_____ (填字母)
A硫酸铜 B氯化钠 C硝酸钾 D酚酞
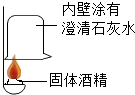
(2)酒精中是否含有碳元素?按如图实验,发现澄清石灰水_____ 。可得出酒精中含有碳元素的结论。
(3)氢氧化钠是否变质?取少量固体酒精于烧杯中,加足量的蒸馏水溶解,发现烧杯底部有白色沉淀,分析实验并结合资料得出氢氧化钠已变质。进一步探究氢氧化钠是否完全变质。
限选试剂:氢氧化钡溶液、硝酸钙溶液、硝酸钡溶液、稀硫酸、稀盐酸、稀硝酸、酚酞溶液
【收集资料】①固体酒精中含有酒精、氢氧化钠、氯化钙等物质 ②酒精的化学式为C2H5OH
【提出问题】(1)酒精的化学式与NaOH相比,都有“OH”,那么酒精的水溶液是否显碱性?从下面试剂中选择合适试剂进行鉴别
A硫酸铜 B氯化钠 C硝酸钾 D酚酞
(2)酒精中是否含有碳元素?按如图实验,发现澄清石灰水

(3)氢氧化钠是否变质?取少量固体酒精于烧杯中,加足量的蒸馏水溶解,发现烧杯底部有白色沉淀,分析实验并结合资料得出氢氧化钠已变质。进一步探究氢氧化钠是否完全变质。
限选试剂:氢氧化钡溶液、硝酸钙溶液、硝酸钡溶液、稀硫酸、稀盐酸、稀硝酸、酚酞溶液
| 实验步骤 | 实验现象 | 实验结论 |
| 1.取上述实验步骤烧杯中的上层清液于试管中,滴入 | 证明固体酒精中有碳酸钠和氢氧化钠,固体酒精部分变质 | |
| 2. |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



