科学探究题 适中0.65 引用3 组卷342
小明同学在做家庭实验时,不小心将过氧化氢溶液溅到妈妈刚刚切好的土豆丝上,发现土豆丝上立即冒气泡,激发了小明的探究欲望,请你参与小明的探究.
(猜想)土豆丝可作过氧化氢分解的催化剂
(实验)设计并完成下表所示的探究实验:
(1)请你帮小明同学填写上表中未填完的空格.
(2)在小明的探究实验中,“实验二”起的作用是_____ .
(反思)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完全证明猜想是正确的:
第一补充实验:在实验三前后,各对土豆丝进行一次称量,其目的是证明:反应前后土豆丝的_____ 没变;
第二补充实验:倾倒掉实验三反应后的液体,向试管中余下的土豆丝中重新加入过氧化氢溶液,又有大量气泡产生,说明土豆丝的_____ 没变.
(结论)通过上述同学所做的实验,我们知道了土豆丝可以作为过氧化氢制取氧气的催化剂.
(猜想)土豆丝可作过氧化氢分解的催化剂
(实验)设计并完成下表所示的探究实验:
(1)请你帮小明同学填写上表中未填完的空格.
| 实验操作 | 实验现象 | 实验结论 | 总结 | |
| 实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是 | 土豆丝可作过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入土豆丝,伸入带火星的木条 | 没有明显现象 | 水和土豆丝不能放出氧气 | |
| 实验三 | 取5mL5%的过氧化氢溶液于试管中,加入土豆丝,伸入带火星的木条 | 土豆丝能加快过氧化氢的分解 |
(2)在小明的探究实验中,“实验二”起的作用是
(反思)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完全证明猜想是正确的:
第一补充实验:在实验三前后,各对土豆丝进行一次称量,其目的是证明:反应前后土豆丝的
第二补充实验:倾倒掉实验三反应后的液体,向试管中余下的土豆丝中重新加入过氧化氢溶液,又有大量气泡产生,说明土豆丝的
(结论)通过上述同学所做的实验,我们知道了土豆丝可以作为过氧化氢制取氧气的催化剂.
19-20九年级上·全国·单元测试
类题推荐
某研究小组对过氧化氢溶液制取氧气进行如下探究:
【实验一】氧气制取和性质实验
(1)现有如下装置:
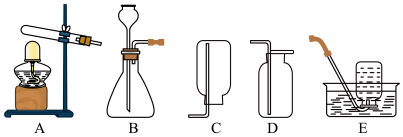
①实验室用过氧化氢溶液制氧气应选择的发生装置和收集装置组合是______ (填标号),反应的化学方程式为_____ 。
②B装置的优点是______ 。
③用收集的氧气进行“铁丝在氧气中燃烧”的实验,观察到的现象是_____ 。
【实验二】探究H2O2质量分数、溶液pH、温度对反应速率的影响
(2)设计如下表实验方案:
①实验1~3的实验目的是______ 。
②a、b的值分别为______ 。
【实验三】探究制取氧气的适宜催化剂
(3)实验方案如下:
在试管中加入20 mL5%H2O2溶液,分别取等质量的重铬酸钾(K2Cr2O7)、CuO、Fe2O3三种物质放在锥形瓶中,采用如图实验装置进行实验,并记录锥形瓶内压强随时间变化的曲线图。
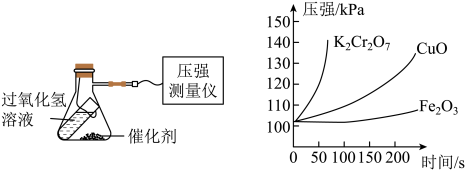
I.实验中,除了通过观察H2O2溶液中产生气泡的快慢来判断H2O2分解的快慢,还可通过______ 来判定H2O2分解的快慢。
II.为了证明CuO是催化剂,除了上述实验,还需要设计实验证明______ 。
III.根据实验结果,小明认为在实验室用H2O2溶液制取氧气实验中,应选择重铬酸钾作为催化剂。你____ (填“是”或“否”)同意他的观点,并说明理由______ 。
【实验一】氧气制取和性质实验
(1)现有如下装置:

①实验室用过氧化氢溶液制氧气应选择的发生装置和收集装置组合是
②B装置的优点是
③用收集的氧气进行“铁丝在氧气中燃烧”的实验,观察到的现象是
【实验二】探究H2O2质量分数、溶液pH、温度对反应速率的影响
(2)设计如下表实验方案:
| 实验序号 | H2O2质量分数% | pH | 温度/℃ | 每分钟气泡数 |
| 1 | 30 | 5 | 20 | |
| 2 | 30 | 6 | 20 | |
| 3 | 30 | 11 | 20 | |
| 4 | 15 | 11 | 30 | |
| 5 | a | 11 | b |
②a、b的值分别为
【实验三】探究制取氧气的适宜催化剂
(3)实验方案如下:
在试管中加入20 mL5%H2O2溶液,分别取等质量的重铬酸钾(K2Cr2O7)、CuO、Fe2O3三种物质放在锥形瓶中,采用如图实验装置进行实验,并记录锥形瓶内压强随时间变化的曲线图。

I.实验中,除了通过观察H2O2溶液中产生气泡的快慢来判断H2O2分解的快慢,还可通过
II.为了证明CuO是催化剂,除了上述实验,还需要设计实验证明
III.根据实验结果,小明认为在实验室用H2O2溶液制取氧气实验中,应选择重铬酸钾作为催化剂。你
在学习完二氧化锰催化过氧化氢分解的试验后,某些兴趣小组在老师的带领下进行了探究实验。
探究一:寻找新的催化剂
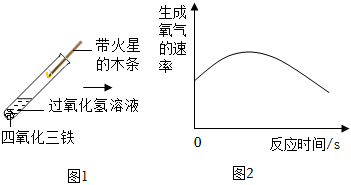
(1)请帮该小组填写表中未填完的表格______ 。
(2)实验结论:四氧化三铁是过氧化氢分解的催化剂,该反应的文字表达式为:______ 。
(3)小明同学认为仅由上述实验还不能得出上述结论,还需要补充实验验证四氧化三铁的______ 和______ 在反应前后是否改变。
探究二:化学反应中的能量变化
(4)小明在实验时发现试管内有许多水雾,由此推断过氧化氢分解是______ (填“放热”或“吸热”)。
(5)实验过程中发现将过氧化氢加入盛有四氧化三铁的试管后,反应速率逐渐加快,然后又逐渐变慢(如图2)(温度、反应物的浓度等)来分析,过氧化氢分解速率发生变化原因。
反应速率先变快原因:______ 。反应速率后变慢原因:______ 。
探究一:寻找新的催化剂

| 试验编号 | 操作 | 现象 | 分析 |
| ① | 取5mL5%的过氧化氢溶液于 试管中,伸入带火星的木条 | 有少量气泡产生, 木条不复燃 | 过氧化氢分解,但 反应速率太慢 |
| ② | ______ | 有大量气泡产生, 木条复燃 | 四氧化三铁能加快 过氧化氢分解 |
(2)实验结论:四氧化三铁是过氧化氢分解的催化剂,该反应的文字表达式为:
(3)小明同学认为仅由上述实验还不能得出上述结论,还需要补充实验验证四氧化三铁的
探究二:化学反应中的能量变化
(4)小明在实验时发现试管内有许多水雾,由此推断过氧化氢分解是
(5)实验过程中发现将过氧化氢加入盛有四氧化三铁的试管后,反应速率逐渐加快,然后又逐渐变慢(如图2)(温度、反应物的浓度等)来分析,过氧化氢分解速率发生变化原因。
反应速率先变快原因:
学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能 否起到类似MnO2的催化剂作用呢?于是进行了以下探究。
否起到类似MnO2的催化剂作用呢?于是进行了以下探究。
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后_____ 。
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢 溶液于试管中,进行如下实验:
溶液于试管中,进行如下实验:

(1)填写下表:
(2)步骤①的目的是_____ 。
(3)步骤④是除去难溶性杂质的操作,所需用到的玻璃仪器 有:漏斗、烧杯、_____ 。
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为_____ 。
 否起到类似MnO2的催化剂作用呢?于是进行了以下探究。
否起到类似MnO2的催化剂作用呢?于是进行了以下探究。【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢
 溶液于试管中,进行如下实验:
溶液于试管中,进行如下实验:
(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中有气泡放出,且 | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立。 |
(3)步骤④是除去难溶性杂质的操作,所需用到的
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


