科学探究题 困难0.15 引用2 组卷273
某化学兴趣小组在实验室做了如下两个探究实验:
(1)实验一;探究学生分组实验废弃液中溶质的成分,并回收处理。
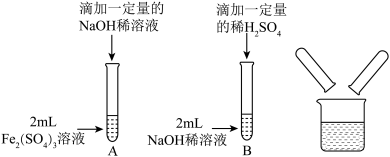
将学生分组实验A、B两支试管中的废弃液同时倒入一洁净的烧杯中,混合,观察到有红褐色沉淀生成,过滤后,对所得滤液中溶质的成分进行探究。
【资料】硫酸钠晶体( ),用于化学和医药工业,水溶液呈中性。
),用于化学和医药工业,水溶液呈中性。
【假设】假设1:滤液中的溶质是 ;
;
假设2:滤液中的溶质是 、
、 ;
;
假设3:滤液中的溶质是 、
、 、
、
假设4:滤液中的溶质还可能是_____________ 。
【讨论】你认为上述假设中____________ 一定不合理,理由是____________ ;如果滤液为无色,还可排除的假设是____________ 。
【实验】某同学通过以下实验方案及现象证明假设4成立,请补充完成下表实验。
【处理】请你设计一个从上述滤液中回收硫酸钠晶体的方案:____________ .
(2)实验二:探究植物营养液中溶质的成分及其含量。
某植物营养液中可能含有 、
、 、
、 、
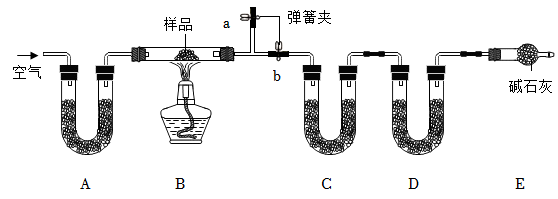
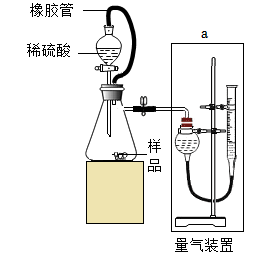
、 中的两种或两种以上的氮、钾化肥。为确认溶质的组成及其质量分数进行如下实验:①取100g上述溶液,加入足量
中的两种或两种以上的氮、钾化肥。为确认溶质的组成及其质量分数进行如下实验:①取100g上述溶液,加入足量 溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.66g,向沉淀中加入过量的稀硝酸,沉淀不溶解;②将①的滤液加热,产生能使湿润红色石蕊试纸变蓝的气体,气体经生石灰干燥后全部被稀硫酸吸收,稀硫酸增重0.85g;③待②的滤液冷却后加入稀硝酸酸化,再加入足量的
溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.66g,向沉淀中加入过量的稀硝酸,沉淀不溶解;②将①的滤液加热,产生能使湿润红色石蕊试纸变蓝的气体,气体经生石灰干燥后全部被稀硫酸吸收,稀硫酸增重0.85g;③待②的滤液冷却后加入稀硝酸酸化,再加入足量的 溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀2.87g。由此判断:该植物营养液中溶质成分及其质量分数是
溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀2.87g。由此判断:该植物营养液中溶质成分及其质量分数是_______ ,含氮量为__________ %,含钾量为__________ %。
(1)实验一;探究学生分组实验废弃液中溶质的成分,并回收处理。
将学生分组实验A、B两支试管中的废弃液同时倒入一洁净的烧杯中,混合,观察到有红褐色沉淀生成,过滤后,对所得滤液中溶质的成分进行探究。

【资料】硫酸钠晶体(
【假设】假设1:滤液中的溶质是
假设2:滤液中的溶质是
假设3:滤液中的溶质是
假设4:滤液中的溶质还可能是
【讨论】你认为上述假设中
【实验】某同学通过以下实验方案及现象证明假设4成立,请补充完成下表实验。
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,滴入 | 假设4正确 |
(2)实验二:探究植物营养液中溶质的成分及其含量。
某植物营养液中可能含有
2019九年级·全国·专题练习
类题推荐
对实验过程中遇到的一些异常现象进行分析能培养我们严谨的科学思维。
【实验一】
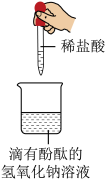
某学习小组同学向滴有酚酞的氢氧化钠溶液中加入一定量稀盐酸(如右图),搅拌后烧杯中溶液由红色变为无色。写出反应的化学方程式______ 。
【实验目的】判断反应后烧杯中无色溶液(溶液A)的溶质成分。
【实验过程】甲、乙同学分别进行如下实验:
【发现问题】甲、乙同学现象有差异
〖继续探究〗
丙同学向烧杯中加入打磨过的镁条,观察到有气泡产生,则_______ (填“甲”或“乙”)同学的结论正确。
丁同学提出:还可以用“加入AgNO3溶液,观察有无白色沉淀产生”的方法验证盐酸是否存在。大家一致认为该方案不可行,理由是______ 。
〖实验反思〗造成甲、乙同学现象有差异的原因是:乙同学的实验烧杯中残留的盐酸较多,1滴氢氧化钠溶液不足以将盐酸完全反应,故溶液仍为无色,而甲同学_______ 。
【实验二】
向氢氧化钠溶液中滴加酚酞,溶液变红,放置一段时间后红色消失,溶液褪为无色。
【提出问题】红色消失的原因是什么?
〖提出猜想〗
猜想1:酚酞与空气中的O2发生了反应;
猜想2:NaOH与空气中的CO2发生了反应;
NaOH与CO2反应的化学方程式为____ 。
经讨论后,大家认为猜想2一定不正确,理由是即便NaOH变质了,______ 。
〖实验验证〗
实验操作中,将NaOH溶液加热煮沸的目的_____ 。
【查阅资料】酚酞的变色范围:pH<8.2时无色;pH等于8.2 10时红色;pH>10时无色。
10时红色;pH>10时无色。
〖继续探究〗溶液红色消失,可能和NaOH溶液的浓度有关。
备选试剂:①号NaOH溶液(质量分数1%, pH约为13.4)
②号NaOH溶液(质量分数0.01%,pH约为11.4)
③号NaOH溶液(质量分数0.0001%,pH约为9.4)
取等体积_____ (选填①②③)于两支试管中,分别滴加等量酚酞试液。观察到其中一支试管中溶液变红,一段时间后红色消失;另一支试管中_____ 。
〖实验结论〗滴有酚酞的NaOH溶液由红色褪为无色与NaOH溶液的浓度有关。
【学以致用】
为测定一瓶氢氧化钠溶液的质量分数,小芳同学进行了如下图所示实验。当溶液颜色由红色恰好变为无色时,消耗稀盐酸7.3g。用该方案测得的氢氧化钠溶液质量分数偏小。结合酚酞的变色范围分析,测量结果偏小的原因是______ 。
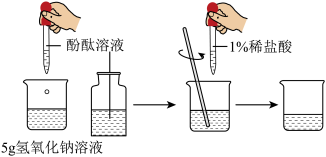
【实验一】
某学习小组同学向滴有酚酞的氢氧化钠溶液中加入一定量稀盐酸(如右图),搅拌后烧杯中溶液由红色变为无色。写出反应的化学方程式

【实验目的】判断反应后烧杯中无色溶液(溶液A)的溶质成分。
【实验过程】甲、乙同学分别进行如下实验:
| 实验操作 | 实验现象 | 实验结论 | |
| 甲 | 从烧杯中取少量溶液(约1mL)于一支试管中,加入1滴氢氧化钠溶液,振荡 | 溶液变红 | 溶液A呈中性,溶质为NaCl |
| 乙 | 直接向烧杯中加入1滴氢氧化钠溶液,振荡 | 溶液仍为无色 | 溶液A呈酸性,溶质为 |
〖继续探究〗
丙同学向烧杯中加入打磨过的镁条,观察到有气泡产生,则
丁同学提出:还可以用“加入AgNO3溶液,观察有无白色沉淀产生”的方法验证盐酸是否存在。大家一致认为该方案不可行,理由是
〖实验反思〗造成甲、乙同学现象有差异的原因是:乙同学的实验烧杯中残留的盐酸较多,1滴氢氧化钠溶液不足以将盐酸完全反应,故溶液仍为无色,而甲同学
【实验二】
向氢氧化钠溶液中滴加酚酞,溶液变红,放置一段时间后红色消失,溶液褪为无色。
【提出问题】红色消失的原因是什么?
〖提出猜想〗
猜想1:酚酞与空气中的O2发生了反应;
猜想2:NaOH与空气中的CO2发生了反应;
NaOH与CO2反应的化学方程式为
经讨论后,大家认为猜想2一定不正确,理由是即便NaOH变质了,
〖实验验证〗
| 实验操作 | 实验现象 | 实验结论 |
| 取少量实验中的NaOH溶液于试管中, 再加热煮沸。待上述溶液冷却后,滴入酚酞溶液,再滴入少量植物油 | 溶液变红,一段时间后红色消失。 | 猜想1 |
【查阅资料】酚酞的变色范围:pH<8.2时无色;pH等于8.2
〖继续探究〗溶液红色消失,可能和NaOH溶液的浓度有关。
备选试剂:①号NaOH溶液(质量分数1%, pH约为13.4)
②号NaOH溶液(质量分数0.01%,pH约为11.4)
③号NaOH溶液(质量分数0.0001%,pH约为9.4)
取等体积
〖实验结论〗滴有酚酞的NaOH溶液由红色褪为无色与NaOH溶液的浓度有关。
【学以致用】
为测定一瓶氢氧化钠溶液的质量分数,小芳同学进行了如下图所示实验。当溶液颜色由红色恰好变为无色时,消耗稀盐酸7.3g。用该方案测得的氢氧化钠溶液质量分数偏小。结合酚酞的变色范围分析,测量结果偏小的原因是

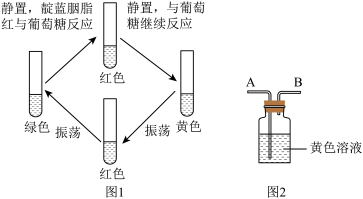
“红绿灯”实验是一个有趣的化学实验:靛蓝胭脂红(C16H8N2Na2O8S2)、氢氧化钠、葡萄糖按一定比例混合的混合液静置一段时间后,溶液出现由绿色到红色,再到黄色的逐渐转变;充分振荡黄色溶液,又逐渐变为红色,最后变为绿色。颜色随静置和振荡多次交替变化,过程如图1所示。
【查阅资料】
Ⅰ、靛蓝胭脂红是一种酸碱指示剂,在pH<11.4溶液中呈蓝色,pH在11.4~13时呈绿色,静置时与葡萄糖逐步反应而发生颜色变化。
Ⅱ、饱和碳酸钠溶液的pH为11.6,饱和碳酸氢钠溶液的pH为8.3,二氧化碳能与碳酸钠溶液反应生成碳酸氢钠。
(1)混合液中属于有机物的是___________ (填一种)。
(2)某化学兴趣小组同学对该实验振荡过程中颜色变化的原因进行如下探究:
【猜想】Ⅰ、溶液中溶入O2;Ⅱ、溶液中溶入CO2;Ⅲ、溶液中溶入___________ (填化学式)。
【实验设计】
①兴趣小组同学利用图2装置,从A端通入氧气,若观察到___________ 的现象,则证明猜想Ⅰ正确。
②小红同学也利用图2装置,从A端吹入呼出的气体,观察到混合液颜色变化为:黄色→红色→绿色,小明认为由此不能得出猜想Ⅱ正确,理由是___________ 。
③小明同学对猜想Ⅱ进行再探究,向上述图2装置内通入足量的二氧化碳后,并未观察到溶液由黄色→红色→绿色的变化,反而观察到溶液最终变为蓝色,请写使溶液变为蓝色的化学方程式___________ 。
(3)图1所示的实验循环多次后,溶液颜色最终为绿色的原因是___________ 。
(4)兴趣小组同学在静置混合液时,发现不同组的变色的时间各不相同,他们又对影响混合液变色时间的因素进行了探究。在大试管中分别加入表中试剂(所用溶液密度差异忽略不计),充分混合后,溶液为绿色。静置,观察并记录:
①由a、b两组实验,你得出的结论是___________ 。
②b、c两组实验是探究靛蓝胭脂红浓度对变色时间的影响,则x=___________ 。

【查阅资料】
Ⅰ、靛蓝胭脂红是一种酸碱指示剂,在pH<11.4溶液中呈蓝色,pH在11.4~13时呈绿色,静置时与葡萄糖逐步反应而发生颜色变化。
Ⅱ、饱和碳酸钠溶液的pH为11.6,饱和碳酸氢钠溶液的pH为8.3,二氧化碳能与碳酸钠溶液反应生成碳酸氢钠。
(1)混合液中属于有机物的是
(2)某化学兴趣小组同学对该实验振荡过程中颜色变化的原因进行如下探究:
【猜想】Ⅰ、溶液中溶入O2;Ⅱ、溶液中溶入CO2;Ⅲ、溶液中溶入
【实验设计】
①兴趣小组同学利用图2装置,从A端通入氧气,若观察到
②小红同学也利用图2装置,从A端吹入呼出的气体,观察到混合液颜色变化为:黄色→红色→绿色,小明认为由此不能得出猜想Ⅱ正确,理由是
③小明同学对猜想Ⅱ进行再探究,向上述图2装置内通入足量的二氧化碳后,并未观察到溶液由黄色→红色→绿色的变化,反而观察到溶液最终变为蓝色,请写使溶液变为蓝色的化学方程式
(3)图1所示的实验循环多次后,溶液颜色最终为绿色的原因是
(4)兴趣小组同学在静置混合液时,发现不同组的变色的时间各不相同,他们又对影响混合液变色时间的因素进行了探究。在大试管中分别加入表中试剂(所用溶液密度差异忽略不计),充分混合后,溶液为绿色。静置,观察并记录:
| 实验序号 | 0.1%靛蓝胭脂红溶液体积/mL | 2%氢氧化钠溶液体积/mL | 18%葡萄糖溶液体积/mL | 水体积/mL | 温度/℃ | 变色时间/s | ||
| 绿→红 | 红→黄 | 合计 | ||||||
| a | 10 | 70 | 10 | 10 | 20 | 178 | 81 | 259 |
| b | 10 | 70 | 10 | 10 | 40 | 22 | 21 | 43 |
| c | 20 | 70 | 10 | x | 40 | 21 | 27 | 48 |
②b、c两组实验是探究靛蓝胭脂红浓度对变色时间的影响,则x=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网