填空与简答-流程题 较难0.4 引用1 组卷86
黄铜矿(主要成分是CuFeS2)经初步处理后,所得溶液甲中溶质为Fe2(SO4)3、CuSO4及H2SO4。某同学通过废铁屑与溶液甲反应,制取补血剂原料碳酸亚铁并回收铜。主要步骤如图所示[Fe2(SO4)3+Fe═3FeSO4]:
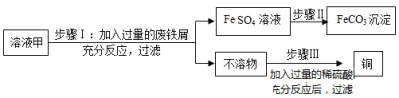
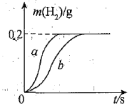
图1 图2
(1)步骤Ⅰ加入的废铁屑中含有少量铁锈,但对产物的成分没有影响,原因是_____ .
(2)步骤Ⅱ中加入一种可溶性试剂可实现其转化,该试剂可以是_____ 。
(3)为了测定步骤Ⅲ中所用稀硫酸的溶质质量分数,该同学取两份相同溶质质量分数的稀硫酸各100g,分别加入等质量的铁和锌,相同条件下充分反应,产生氢气的质量随时间变化的曲线如图2所示,则下列说法正确的是_____ 。
A 表示锌和稀硫酸反应的情况的是曲线a
B 稀硫酸的溶质质量分数为9.8%
C 加入铁的质量至少有5.6g
D 加入锌的质量可能是13g


图1 图2
(1)步骤Ⅰ加入的废铁屑中含有少量铁锈,但对产物的成分没有影响,原因是
(2)步骤Ⅱ中加入一种可溶性试剂可实现其转化,该试剂可以是
(3)为了测定步骤Ⅲ中所用稀硫酸的溶质质量分数,该同学取两份相同溶质质量分数的稀硫酸各100g,分别加入等质量的铁和锌,相同条件下充分反应,产生氢气的质量随时间变化的曲线如图2所示,则下列说法正确的是
A 表示锌和稀硫酸反应的情况的是曲线a
B 稀硫酸的溶质质量分数为9.8%
C 加入铁的质量至少有5.6g
D 加入锌的质量可能是13g
2018·江苏淮安·一模
类题推荐
金属与人类的生产和生活密切相关。
(1)《梦溪笔谈》中:“古人以剂刚为刃,柔铁为茎干,不尔则多断折。……….”,剂刚、柔铁均为铁的合金,这主要因为合金比纯金属__________ 的优良性能。
(2)为探究银、铜、铁的活动性顺序,设计了四种方案,每种方案所用的试剂如下,其中你认为不可行的是__________。
(3)在一定质量Cu(NO3)2、AgNO3、Zn(NO3)2的混合溶液中加入一定量Fe粉,充分反应后,过滤,得到固体和滤液,且滤液为蓝色。滤液中一定含有的溶质是___________ 。
(4)某机械厂金属废料的成分是Zn、Cu、ZnO和CuO,下图是某化学小组利用该金属废料回收铜并制取氧化锌的流程图。请回答下列问题。

①步骤I所得滤液a中溶质的成分是____________ (填写化学式)。
②步骤Ⅲ加入试剂甲的名称是___________ 。
③步骤IV加入适量NaOH溶液发生反应的化学方程式为___________ (任写一个)。
(1)《梦溪笔谈》中:“古人以剂刚为刃,柔铁为茎干,不尔则多断折。……….”,剂刚、柔铁均为铁的合金,这主要因为合金比纯金属
(2)为探究银、铜、铁的活动性顺序,设计了四种方案,每种方案所用的试剂如下,其中你认为不可行的是__________。
| A.Fe、Ag、CuSO4溶液 | B.Fe、Cu、AgNO3溶液、稀盐酸 |
| C.Cu、FeCl2溶液、AgNO3溶液 | D.Cu、Ag、Fe、稀盐酸 |
(4)某机械厂金属废料的成分是Zn、Cu、ZnO和CuO,下图是某化学小组利用该金属废料回收铜并制取氧化锌的流程图。请回答下列问题。

①步骤I所得滤液a中溶质的成分是
②步骤Ⅲ加入试剂甲的名称是
③步骤IV加入适量NaOH溶液发生反应的化学方程式为
硫酸铁铵NH4Fe(SO4)2·xH2O是一种重要的化合物,常用于物质检测的指示剂。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:回答下列问题:

(1)硫酸铁铵属于____________ (填“酸”、“碱”、“盐”),其中铁元素的化合价是____________ 。
(2)步骤①的目的是除去废铁屑表面的油污,可选择的试剂有 。
(3)步骤②中发生的反应化学方程式为____________ 。该反应加热的目的是____________ 。温度欲保持在80~90℃,采用的合适加热方式是____________ 。
(4)步骤③中的反应为2FeSO4+X+H2O2=Fe2(SO4)3+2H2O(放热),X的化学式为____________ 。反应过程中要分批加入H2O2溶液,原因是____________ 。
(5)步骤⑤的具体实验操作有:________ 、降温结晶、过滤、洗涤、干燥得到硫酸铁铵晶体样品。
(6)为测定硫酸铁铵所带结晶水个数,实验小组进行了如下实验:称取4.82g硫酸铁铵晶体溶于水,加入足量BaCl2溶液,将生成的沉淀经过滤、洗涤、干燥,测得质量为4.66g。请通过计算确定x的值(要有计算过程)____________ 。实验过程中,若沉淀未洗涤干净,则测得的x的值会_______ (“偏大”、“偏小”、“无影响”)。

(1)硫酸铁铵属于
(2)步骤①的目的是除去废铁屑表面的油污,可选择的试剂有 。
| A.稀盐酸 | B.纯碱溶液 | C.氢氧化钠溶液 |
(4)步骤③中的反应为2FeSO4+X+H2O2=Fe2(SO4)3+2H2O(放热),X的化学式为
(5)步骤⑤的具体实验操作有:
(6)为测定硫酸铁铵所带结晶水个数,实验小组进行了如下实验:称取4.82g硫酸铁铵晶体溶于水,加入足量BaCl2溶液,将生成的沉淀经过滤、洗涤、干燥,测得质量为4.66g。请通过计算确定x的值(要有计算过程)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


