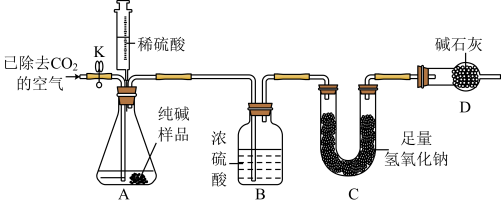科学探究题 较难0.4 引用2 组卷84
现有A、B、C、D四种溶液,某研究小组的同学取少量四种溶液样品,分别加入一定量的稀硫酸,观察实验现象。
其中不能与稀硫酸发生反应的是_____ (填字母);与稀硫酸反应产生白色沉淀的化学方程式为_____ 。
实验结束后小组同学将废液倒入同一废液缸中,过滤,得到滤渣和滤液
【提出问题】滤液中含有哪些离子?
经分析可知,滤液中一定含有的离子是_____ (填离子符号)。
【实验探究】对滤液中可能含有的离子进行探究。
小刚的实验操作:取样,用pH试纸测得滤液的pH约为3,由此可以得出结论:滤液中定不含有的离子是_____ (填离子符号)。
小明的实验操作:取滤液少许于试管中,向其中滴加氯化钡溶液,观察到有白色沉淀产。
由此可以得出结论:滤液中一定含有硫酸根离子,
【总结与评价】请你对小明的实验做出评价_____ 。
小组同学经过合作与交流,最终确定了滤液中的离子成分。
【反思与收获】上述探究给我们的启示是:要想确定实验最终所得溶液中的离子成分,首先可以依据已有知识和题中信息进行合理推断,比如:可以推断出_____ 。然后再选取合适的试剂,对_____ 进行探究即可。
| A | B | C | D |
| 氢氧化钠溶液 | 氯化钠溶液 | 碳酸钠溶液 | 氯化钡溶液 |
其中不能与稀硫酸发生反应的是
实验结束后小组同学将废液倒入同一废液缸中,过滤,得到滤渣和滤液
【提出问题】滤液中含有哪些离子?
经分析可知,滤液中一定含有的离子是
【实验探究】对滤液中可能含有的离子进行探究。
小刚的实验操作:取样,用pH试纸测得滤液的pH约为3,由此可以得出结论:滤液中定不含有的离子是
小明的实验操作:取滤液少许于试管中,向其中滴加氯化钡溶液,观察到有白色沉淀产。
由此可以得出结论:滤液中一定含有硫酸根离子,
【总结与评价】请你对小明的实验做出评价
小组同学经过合作与交流,最终确定了滤液中的离子成分。
【反思与收获】上述探究给我们的启示是:要想确定实验最终所得溶液中的离子成分,首先可以依据已有知识和题中信息进行合理推断,比如:可以推断出
2019·黑龙江哈尔滨·一模
类题推荐
化学实验室有一包白色粉末,可能由碳酸钡、氯化钾、硫酸钠、氯化钡、硫酸铜中的一种或几种组成,化学兴趣小组的同学对其成分进行了如下探究。
【提出问题】该粉末的成分是什么?
【实验探究】
【实验分析】
步骤2中沉淀部分溶解反应的化学方程式为______ 。
【反思评价】
小亮认为上述实验还不能确定氯化钾是否存在,因此继续进行了如下实验:取少量步骤1所得溶液于试管中,向其中滴加硝酸银溶液,观察到有白色沉淀生成。由此得出结论:原白色粉末中一定含有氯化钾。小明认为小亮的实验不能确定氯化钾的存在,理由是______ 。
【提出问题】该粉末的成分是什么?
【实验探究】
实验操作 | 实验现象 | 实验结论 |
步骤1:取适量粉末于烧杯中,加入 足量的水,充分搅拌,过滤 | 产生白色沉淀和 无色溶液 | 原粉末中一定不含有 |
步骤2:取少量步骤1的白色沉淀沉 淀于试管中,加入过量的稀硝酸 | 沉淀部分溶解, 并产生气泡 | 白色沉淀是 |
【实验分析】
步骤2中沉淀部分溶解反应的化学方程式为
【反思评价】
小亮认为上述实验还不能确定氯化钾是否存在,因此继续进行了如下实验:取少量步骤1所得溶液于试管中,向其中滴加硝酸银溶液,观察到有白色沉淀生成。由此得出结论:原白色粉末中一定含有氯化钾。小明认为小亮的实验不能确定氯化钾的存在,理由是
热水瓶用久后,瓶胆内壁常附着一层水垢,其成分是CaCO3、Mg(OH)2及少量水。实验室现有一份水垢样品,为测定其中各成分的质量分数,某化学兴趣小组的同学利用下图所示装置进行实验。
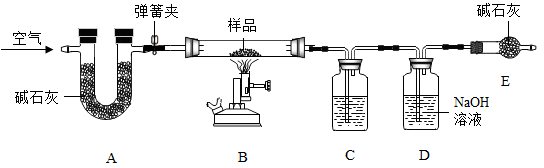
已知:①A、C、D中所装药品均为足量;
②碱石灰是氧化钙和氢氧化钠的固体混合物;
③在加热条件下,氢氧化镁易分解成两种氧化物。
主要实验步骤如下:
Ⅰ.将质量为12.0g的样品装入装置B的玻璃管中,连接装置,关闭弹簧夹,加热;
Ⅱ.待样品完全反应,先________(选填序号);
A.打开弹簧夹缓缓通入空气 B.熄灭酒精喷灯
Ⅲ.实验完毕,测得装置C、D中质量分别增加了2.5g、3.3g;
Ⅳ.根据实验所测数据计算该样品中碳酸钙、氢氧化镁和水的质量分数。
请回答下列问题:
(1)步骤Ⅱ中,待样品完全反应,先_________ (选填序号);
(2)装置C中所装药品为_________ 。
(3)装置E的作用为_________ 。
(4)样品中CaCO3的质量分数为_________ ;Mg(OH)2的质量分数为_________ 。(结果保留到0.1%)
实验反思:
(5)实验步骤不变,若没有装置A,会导致Mg(OH)2的测定结果_________ (填“偏大”、“偏小”或“无法判断”)。

已知:①A、C、D中所装药品均为足量;
②碱石灰是氧化钙和氢氧化钠的固体混合物;
③在加热条件下,氢氧化镁易分解成两种氧化物。
主要实验步骤如下:
Ⅰ.将质量为12.0g的样品装入装置B的玻璃管中,连接装置,关闭弹簧夹,加热;
Ⅱ.待样品完全反应,先________(选填序号);
A.打开弹簧夹缓缓通入空气 B.熄灭酒精喷灯
Ⅲ.实验完毕,测得装置C、D中质量分别增加了2.5g、3.3g;
Ⅳ.根据实验所测数据计算该样品中碳酸钙、氢氧化镁和水的质量分数。
请回答下列问题:
(1)步骤Ⅱ中,待样品完全反应,先_________ (选填序号);
| A.打开弹簧夹缓缓通入空气 | B.熄灭酒精喷灯 |
(3)装置E的作用为
(4)样品中CaCO3的质量分数为
实验反思:
(5)实验步骤不变,若没有装置A,会导致Mg(OH)2的测定结果
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网