科学探究题 适中0.65 引用3 组卷132
自来水厂常用氯气来杀菌消毒,某班学生对氯气的制取、性质进行如下探究:
【查阅资料】氯气(C12)是无色有刺激性气味的有毒气体,它的密度比空气大,可溶于水生成盐酸和次氯酸(HClO),写出氯气与水反应的化学方程式______ 。
【探究一】制取氯气
(1)实验室常用二氧化锰固体和浓盐酸加热制取氯气,同时还生成氯化锰(其中锰元素显+2价)和水,请写出该反应的化学方程式:______ 。
(2)实验室制取氯气应选择的发生装置是____ ,最佳收集装置是 ____ (填序号)。
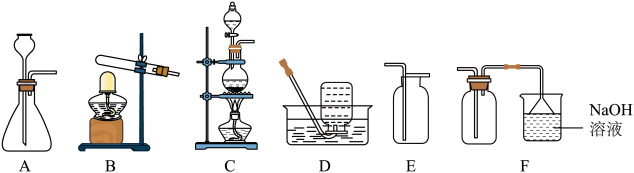
【探究二】氯气的性质实验步骤:I.用锌粒和稀硫酸在A装置中制取氢气,请写出该反应的化学方程式:____ 。
II.先____ ,然后再点燃氢气,观察到淡蓝色火焰,写出氢气在空气中燃烧的化学方程式 ____ 。
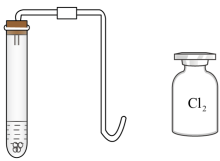
Ⅲ.将燃着的氢气导管缓缓伸到装满氯气的集气瓶乙中,观察到氢气继续燃烧并产生苍白色火焰。请写出该反应的化学方程式:____ 。甲乙实验反思:小星发现氢气在氯气中燃烧时,集气瓶乙瓶口上方有大量白雾,你认为产生白雾的可能原因是 ____ 。
【查阅资料】氯气(C12)是无色有刺激性气味的有毒气体,它的密度比空气大,可溶于水生成盐酸和次氯酸(HClO),写出氯气与水反应的化学方程式
【探究一】制取氯气
(1)实验室常用二氧化锰固体和浓盐酸加热制取氯气,同时还生成氯化锰(其中锰元素显+2价)和水,请写出该反应的化学方程式:
(2)实验室制取氯气应选择的发生装置是

【探究二】氯气的性质实验步骤:I.用锌粒和稀硫酸在A装置中制取氢气,请写出该反应的化学方程式:
II.先
Ⅲ.将燃着的氢气导管缓缓伸到装满氯气的集气瓶乙中,观察到氢气继续燃烧并产生苍白色火焰。请写出该反应的化学方程式:

2019·山东淄博·一模
类题推荐
学习了二氧化锰对过氧化氢有催化作用的知识后。小明同学想:氧化铜能否起到类似二氧化锰的催化剂作用呢?于是进行了如下探究。
【猜想】Ⅰ氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ氧化铜是反应的催化剂,反应前后质量和化学性质不变。
【实验】用天平称量0.2g氧化铜,取5mL 5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
(2)步骤①的目的是_________ 。
(3)过氧化氢能被氧化铜催化分解放出氧气的化学反应的符号表达式为_________ 。
【拓展】
(4)小明在实验室中想用过氧化氢溶液来制取氧气,为获得平稳氧气流,应从下列装置中选用的发生装置是________ (填序号,下同),收集一瓶较纯净的氧气宜采用的装置是_______ 。

【猜想】Ⅰ氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ氧化铜是反应的催化剂,反应前后质量和化学性质不变。
【实验】用天平称量0.2g氧化铜,取5mL 5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 所得固体 | 溶液中有气泡放出, | 猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
(3)过氧化氢能被氧化铜催化分解放出氧气的化学反应的符号表达式为
【拓展】
(4)小明在实验室中想用过氧化氢溶液来制取氧气,为获得平稳氧气流,应从下列装置中选用的发生装置是

实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气。小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除MnO2、CuO(氧化铜)外,Al2O3(氧化铝)也可以作KClO3分解的催化剂。
【完成实验】按如表进行实验:测定分解温度(分解温度越低,催化效果越好)。
【分析数据、得出结论】
(1)由实验___________ 与实验④对比,证明猜想合理。
(2)实验所用的三种催化剂,催化效果最好的是___________ 。
【反思】若要证明Al2O3也是该反应的催化剂,请你一起参与他的探究过程,并填写下列空白。
【问题】Al2O3能不能作过氧化氢分解的催化剂呢?
【猜想】Al2O3能作过氧化氢分解的催化剂。
【实验验证】
【结论】Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂。
【讨论与反思】经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:【实验目的】探究________ 。
【实验步骤】
①准确称量Al2O3(少量)的质量;
②完成实验二;
③待反应结束,将实验二试管里的物质进行过滤,洗涤,烘干,________ ;
④对比反应前后Al2O3的质量。
【讨论】如果Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂。
但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究_______ 。
写出过氧化氢溶液在氧化铝作催化剂的条件下反应的文字表达式(或化学方程式):________ 。
【提出猜想】除MnO2、CuO(氧化铜)外,Al2O3(氧化铝)也可以作KClO3分解的催化剂。
【完成实验】按如表进行实验:测定分解温度(分解温度越低,催化效果越好)。
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | KClO3 | 580 |
| ② | KClO3、MnO2(质量比1:1) | 350 |
| ③ | KClO3、CuO(质量比1:1) | 370 |
| ④ | KClO3、Al2O3(质量比1:1) | 390 |
(1)由实验
(2)实验所用的三种催化剂,催化效果最好的是
【反思】若要证明Al2O3也是该反应的催化剂,请你一起参与他的探究过程,并填写下列空白。
【问题】Al2O3能不能作过氧化氢分解的催化剂呢?
【猜想】Al2O3能作过氧化氢分解的催化剂。
【实验验证】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 在装有过氧化氢溶液的试管中将带火星的木条伸入试管中 | 常温下过氧化氢溶液不分解 | |
| 实验二 | 木条复燃 |
【讨论与反思】经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:【实验目的】探究
【实验步骤】
①准确称量Al2O3(少量)的质量;
②完成实验二;
③待反应结束,将实验二试管里的物质进行过滤,洗涤,烘干,
④对比反应前后Al2O3的质量。
【讨论】如果Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂。
但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究
写出过氧化氢溶液在氧化铝作催化剂的条件下反应的文字表达式(或化学方程式):
兴趣小组同学在老师的带领下,探究影响过氧化氢分解速率的因素。
【提出问题】影响过氧化氢分解的因素有哪些?
【作出假设】猜想1:催化剂的种类;猜想2:过氧化氢溶液的浓度;猜想3:温度
【实验探究】学生利用如图1所示装置,以收集50mL的气体为标准,比较反应的快慢,实验方案如下表所示:
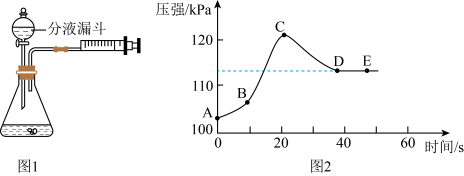
(1)实验中使用分液漏斗目的:_______ ,使用注射器的优点是_______ 。
(2)写出实验3发生反应的文字或符号表达式_______ 。
(3)通过对比实验1和3,得出二氧化锰的催化效果比氧化铜强,则b_______ (填“>”“=”或“<”)37。对比实验1和2,得出的结论是_______ 。
(4)实验过程中,学生触摸锥形瓶外壁,有发烫的感觉,说明过氧化氢分解的反应是放出热量的。在实验3探究中,测出了实验过程中装置压强与时间的关系图(图2),BC段压强急剧上升原因与:_______ 和_______ 有关。CD段压强降低的主要原因是:_______ 。
【提出问题】影响过氧化氢分解的因素有哪些?
【作出假设】猜想1:催化剂的种类;猜想2:过氧化氢溶液的浓度;猜想3:温度
【实验探究】学生利用如图1所示装置,以收集50mL的气体为标准,比较反应的快慢,实验方案如下表所示:

| 序号 | 温度/℃ | 过氧化氢溶液浓度 | 过氧化氢溶液体积/mL | 1g催化剂 | 时间/s |
| 1 | 20 | 5% | 40 | 二氧化锰 | 37 |
| 2 | 20 | 10% | 40 | 二氧化锰 | 14 |
| 3 | 20 | 5% | 40 | 氧化铜 | b |
| 4 | 80 | 5% | 40 | 二氧化锰 | 29 |
(1)实验中使用分液漏斗目的:
(2)写出实验3发生反应的文字或符号表达式
(3)通过对比实验1和3,得出二氧化锰的催化效果比氧化铜强,则b
(4)实验过程中,学生触摸锥形瓶外壁,有发烫的感觉,说明过氧化氢分解的反应是放出热量的。在实验3探究中,测出了实验过程中装置压强与时间的关系图(图2),BC段压强急剧上升原因与:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


