科学探究题 较难0.4 引用1 组卷81
高锰酸钾在生产、生活中有广泛应用。
实验一:实验室制取气体
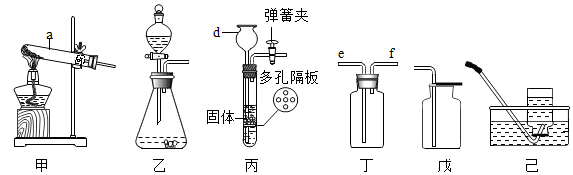
(1)实验室可以用高锰酸钾制取氧气。其反应原理______ (化学方程式表示)选用的发生装置是 ______ (填序号);仪器d的名称是 ______ 。
(2)实验室用丁装置收集二氧化碳气体,气体应从______ (填“e”或“f”端)通入;若要检验收集的气体是否为二氧化碳,需向集气瓶中加入适量澄清石灰水并振荡,该反应的化学方程式为 ______ 。
(3)梁明同学认为乙装置和丙装置类似,都可以用于液体与固体在常温下制取气体的反应。由此他认为实验室用二氧化锰和双氧水制取氧气可用丙装置进行,以便控制反应的发生和停止。刘彬同学经过认真思考后认为梁明同学的看法是错误的。刘彬同学的理由是______ 。
实验二:实验小组对高锰酸钾进行再探究
I.经硫酸酸化的高锰酸钾溶液和草酸(H2C2O4)溶液混合,发现刚开始反应时溶液褪色不明显,但不久后褪色速度突然加快。为了探究反应过程中褪色速度加快的原因,小明查到了如下资料:
资料1:2KMnO4+5H2C2O4+3H2SO4===2MnSO4+K2SO4+8H2O+10CO2↑
资料2:通常情况下,反应物浓度变大,反应加快;温度升高,反应加快。
(1)根据这些资料,小明提出了两个假设。
假设一:褪色速度突然加快是由反应物浓度变大引起的;
假设二:褪色速度突然加快是由反应过程中温度升高引起的。
小明经过分析,否定了假设一,理由是______ 。
(2)小丽针对假设二进行实验探究后,经过思考,又做了如下实验:
把经硫酸酸化的高锰酸钾溶液等分为两份,分装A、B两试管,同时向两支试管中加入等量等浓度的草酸溶液,并置于同一水浴中。迅速向A试管中加入一定量的MnSO4发现A试管中溶液褪色明显快于B试管。上述实验中,把2支试管置于同一水浴中的目的是______ 。这一实验基于的假设是 ______ 。
Ⅱ.【查阅资料】KMnO4溶液呈中性、有腐蚀性。
【进行实验】
实验1:将新鲜鸡皮在不同浓度的KMnO4溶液中浸泡相同时间,现象如下表。
实验2:将铜片分别浸泡在4种溶液中进行实验,所得数据如下表。
【解释与结论】
(1)实验1的目的是______ 。
(2)实验2中,通过对比②和④,得出的结论是______ 。
(3)实验2中,欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,需要对比______ (填编号)。
(4)实验2中,铜片被腐蚀的反应如下,补全该反应的化学方程式。
5Cu+2KMnO4+8H2SO4===5CuSO4+2MnSO4+K2SO4+______ 。
实验一:实验室制取气体

(1)实验室可以用高锰酸钾制取氧气。其反应原理
(2)实验室用丁装置收集二氧化碳气体,气体应从
(3)梁明同学认为乙装置和丙装置类似,都可以用于液体与固体在常温下制取气体的反应。由此他认为实验室用二氧化锰和双氧水制取氧气可用丙装置进行,以便控制反应的发生和停止。刘彬同学经过认真思考后认为梁明同学的看法是错误的。刘彬同学的理由是
实验二:实验小组对高锰酸钾进行再探究
I.经硫酸酸化的高锰酸钾溶液和草酸(H2C2O4)溶液混合,发现刚开始反应时溶液褪色不明显,但不久后褪色速度突然加快。为了探究反应过程中褪色速度加快的原因,小明查到了如下资料:
资料1:2KMnO4+5H2C2O4+3H2SO4===2MnSO4+K2SO4+8H2O+10CO2↑
资料2:通常情况下,反应物浓度变大,反应加快;温度升高,反应加快。
(1)根据这些资料,小明提出了两个假设。
假设一:褪色速度突然加快是由反应物浓度变大引起的;
假设二:褪色速度突然加快是由反应过程中温度升高引起的。
小明经过分析,否定了假设一,理由是
(2)小丽针对假设二进行实验探究后,经过思考,又做了如下实验:
把经硫酸酸化的高锰酸钾溶液等分为两份,分装A、B两试管,同时向两支试管中加入等量等浓度的草酸溶液,并置于同一水浴中。迅速向A试管中加入一定量的MnSO4发现A试管中溶液褪色明显快于B试管。上述实验中,把2支试管置于同一水浴中的目的是
Ⅱ.【查阅资料】KMnO4溶液呈中性、有腐蚀性。
【进行实验】
实验1:将新鲜鸡皮在不同浓度的KMnO4溶液中浸泡相同时间,现象如下表。
| KMnO4 溶液浓度 | 0.002% | 0.01% | 0.1% | 1% |
| 鸡皮的 变化 | 无明显 变化 | 边缘部分变 为棕黄色 | 全部变 为棕色 | 全部变 为黑色 |
实验2:将铜片分别浸泡在4种溶液中进行实验,所得数据如下表。
编号 | ① | ② | ③ | ④ | |
实验 |
|
|
|
| |
铜片质量/g | 实验 | 0.54 | 0.54 | 0.54 | 0.54 |
18小 | 0.54 | 0.52 | 0.54 | 0.43 | |
【解释与结论】
(1)实验1的目的是
(2)实验2中,通过对比②和④,得出的结论是
(3)实验2中,欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,需要对比
(4)实验2中,铜片被腐蚀的反应如下,补全该反应的化学方程式。
5Cu+2KMnO4+8H2SO4===5CuSO4+2MnSO4+K2SO4+
2019·福建泉州·一模
类题推荐
催化剂在化学反应中起着非常重要的作用,某化学兴趣小组对氯酸钾制取氧气的催化剂展开探究。请回答下列问题:
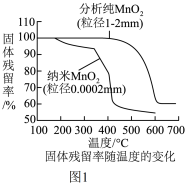
探究一:二氧化锰粒径大小对催化效果的影响。
取两份等质量氟酸钾,分别加入等质量、粒径大小不同的二氧化锰进行加热,用传感器测得固体残留率(反应后剩余固体质量与反应前固体质量之比)如图1:
(1)二氧化锰作催化剂,加热氯酸钾制取氧气的化学符号表达式为_______ 。
(2)分析上图,对氯酸钾分解催化效果更好的是_____ 。催化效果更好的原因可能是_____ 。
探究二:催化剂用量及催化剂种类对催化效果的影响。同学们用图2装置进行如下实验:
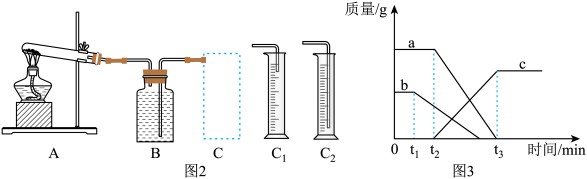
(3)可采取排水法的收集氧气的原因是___ ,收集气体前集气瓶内未装满水,对实验结果____ (填“有”或“没有”)影响。为了较精确测定排出水的体积,C框内应选用的装置为____ (填“C1”或“C2”)。
(4)实验1的目的是_____ 。
(5)表中所列三种催化剂中,催化效果最好的是_______ 。
(6)二氧化锰与氯酸钾的质量比为_______ 时,催化效果最好。
(7)氯化钾_______ (填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集50mL氧气,所需时间明显少于171s,原因是_______ 。
(8)要比较氯酸钾分解反应中不同催化剂的催化效果,除了测量收集50mLO2所需时间外,还可以测量相同时间内_______ 。
【拓展延伸】某同学误将少量高锰酸钾当成二氧化锰加入氯酸钾中进行加热制取氧气,部分物质质量随时间变化如图3所示。氧气从_______ (填“t1”、“t2”或“t3”)时刻开始产生,c代表的物质是_____ 。

探究一:二氧化锰粒径大小对催化效果的影响。
取两份等质量氟酸钾,分别加入等质量、粒径大小不同的二氧化锰进行加热,用传感器测得固体残留率(反应后剩余固体质量与反应前固体质量之比)如图1:
(1)二氧化锰作催化剂,加热氯酸钾制取氧气的化学符号表达式为
(2)分析上图,对氯酸钾分解催化效果更好的是
探究二:催化剂用量及催化剂种类对催化效果的影响。同学们用图2装置进行如下实验:
| 编号 | 氯酸钾质量/g | 催化剂 | 催化剂质量/g | 收集50mL氧气所需时间/s |
| 实验1 | 5 | 无 | 无 | 171 |
| 实验2 | 5 | 二氧化锰 | 0.25 | 79 |
| 实验3 | 5 | 二氧化锰 | 0.5 | 49 |
| 实验4 | 5 | 二氧化锰 | 2.5 | 93 |
| 实验5 | 5 | 氧化铁 | 0.5 | 58 |
| 实验6 | 5 | 氯化钾 | 0.5 | 154 |

(3)可采取排水法的收集氧气的原因是
(4)实验1的目的是
(5)表中所列三种催化剂中,催化效果最好的是
(6)二氧化锰与氯酸钾的质量比为
(7)氯化钾
(8)要比较氯酸钾分解反应中不同催化剂的催化效果,除了测量收集50mLO2所需时间外,还可以测量相同时间内
【拓展延伸】某同学误将少量高锰酸钾当成二氧化锰加入氯酸钾中进行加热制取氧气,部分物质质量随时间变化如图3所示。氧气从
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网