填空与简答-流程题 较难0.4 引用4 组卷631
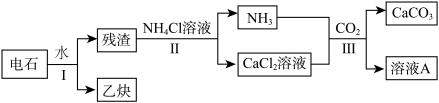
利用某工业废弃固体(成分为Cu2S和FeS2)制备硫酸铜溶液和硫酸亚铁晶体,流程如图所示。
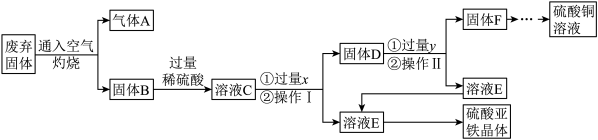
(已知:①固体B含有氧化铜、氧化铁②铁能与硫酸铁反应,生成硫酸亚铁)
(1)操作I是_____ 。为了提高废弃固体的反应速率,除将固体粉碎、提高温度外,还可以采取的具体措施有_____ (写一条)。
(2)写出FeS2在空气中灼烧的化学方程式_____ 。
(3)溶液C中的溶质有_____ (用化学式表示)。
(4)试剂y的作用是_____ 。

(已知:①固体B含有氧化铜、氧化铁②铁能与硫酸铁反应,生成硫酸亚铁)
(1)操作I是
(2)写出FeS2在空气中灼烧的化学方程式
(3)溶液C中的溶质有
(4)试剂y的作用是
2018·广西玉林·中考真题
类题推荐
阅读科普短文,回答下列问题。
松花蛋又称皮蛋、变蛋、灰包蛋等,因剥开蛋壳后胶冻状的蛋清中常有松针状的结晶或花纹而得名。中医认为,松花蛋性凉,对牙痛、眼痈等疾病有有一定疗效。由于松松花蛋会有一股碱涩味,在吃松花蛋的时候可以加入少量的姜醋汁。
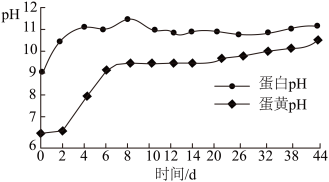
松花蛋是用料泥包裹鸭蛋、鸡蛋等加工而成。料泥是由生石灰、纯碱、食盐、红茶、草木灰(主要成分K2CO3)等原料与水按比例混合均匀制得,料泥制作过程中,通过一系列反应,产生的强碱(NaOH、KOH)经蛋壳渗入到蛋清和蛋黄中,与其中的蛋白质作用,致使蛋白质分解、凝固并放出少量硫化氢气体和氨气。同时渗入的碱还会与蛋白质分解出的氨基做进一步发生中和反应,生成的盐的晶体沉积在凝胶态的蛋清中,便出现了朵朵“松花”,而硫化氢气体则与蛋清和蛋黄中的矿物质作用生成各种硫化物,使蛋清和蛋黄的颜色发生改交,蛋清呈特殊的茶褐色、蛋黄则呈墨绿色。下图表示松花蛋腌制时间与其中蛋清和蛋黄的pH的变化关系。
很多人非常喜欢吃皮蛋瘦肉粥、凉拌松花蛋,专家提醒这种食物少吃无妨,却不能过多食用。其一,松花蛋腌制过程中蛋白质分解、变质,导致营养价值遭到了一定的破坏。其二,市售松花蛋还可能含铅(国家规定铅含量需小于0.5 mg/kg),微量铅很容易被儿童吸收,导致铅中毒,其三,剥开皮的松花蛋1至2小时内一定要吃完,若长时间暴露在空气中,非常容易感染沙门氏杆菌,沙门氏杆菌会快速繁殖,此时食用松花蛋很容易引起中毒现象。
(1)食用松花蛋时加入少量姜醋汁可以除去松花蛋中______ 味。
(2)料泥制作过程中发生的一系列反应中属于化合反应的化学方程式为______ 。
(3)依据松花蛋腌制时间与其中蛋清和蛋黄pH的变化关系判断,当蛋清和蛋黄pH均达到9以上时。松花蛋至少腌制的天数为______(填字母序号,下同)。
(4)下列关于松花蛋的说法正确的是______。
松花蛋又称皮蛋、变蛋、灰包蛋等,因剥开蛋壳后胶冻状的蛋清中常有松针状的结晶或花纹而得名。中医认为,松花蛋性凉,对牙痛、眼痈等疾病有有一定疗效。由于松松花蛋会有一股碱涩味,在吃松花蛋的时候可以加入少量的姜醋汁。
松花蛋是用料泥包裹鸭蛋、鸡蛋等加工而成。料泥是由生石灰、纯碱、食盐、红茶、草木灰(主要成分K2CO3)等原料与水按比例混合均匀制得,料泥制作过程中,通过一系列反应,产生的强碱(NaOH、KOH)经蛋壳渗入到蛋清和蛋黄中,与其中的蛋白质作用,致使蛋白质分解、凝固并放出少量硫化氢气体和氨气。同时渗入的碱还会与蛋白质分解出的氨基做进一步发生中和反应,生成的盐的晶体沉积在凝胶态的蛋清中,便出现了朵朵“松花”,而硫化氢气体则与蛋清和蛋黄中的矿物质作用生成各种硫化物,使蛋清和蛋黄的颜色发生改交,蛋清呈特殊的茶褐色、蛋黄则呈墨绿色。下图表示松花蛋腌制时间与其中蛋清和蛋黄的pH的变化关系。

很多人非常喜欢吃皮蛋瘦肉粥、凉拌松花蛋,专家提醒这种食物少吃无妨,却不能过多食用。其一,松花蛋腌制过程中蛋白质分解、变质,导致营养价值遭到了一定的破坏。其二,市售松花蛋还可能含铅(国家规定铅含量需小于0.5 mg/kg),微量铅很容易被儿童吸收,导致铅中毒,其三,剥开皮的松花蛋1至2小时内一定要吃完,若长时间暴露在空气中,非常容易感染沙门氏杆菌,沙门氏杆菌会快速繁殖,此时食用松花蛋很容易引起中毒现象。
(1)食用松花蛋时加入少量姜醋汁可以除去松花蛋中
(2)料泥制作过程中发生的一系列反应中属于化合反应的化学方程式为
(3)依据松花蛋腌制时间与其中蛋清和蛋黄pH的变化关系判断,当蛋清和蛋黄pH均达到9以上时。松花蛋至少腌制的天数为______(填字母序号,下同)。
| A.2天 | B.6天 | C.12天 | D.32天 |
(4)下列关于松花蛋的说法正确的是______。
| A.松花蛋特殊颜色的形成与硫化氢气体有关 |
| B.松花蛋具有很高的营养价值,成人可以多吃 |
| C."市售松花蛋可能含有少量的铅,儿童不宜食用 |
| D.剥开皮的松花蛋隔夜放置后依然可以放心食用 |
以某菱镁矿石(主要成分是MgCO3,含少量MnCO3、SiO2)制取MgSO4·7H2O,流程如下:______ (写出一种)。此时,MnCO3发生反应的化学方程式是______ 。
(2)“转化”时主要反应是 ,氯元素反应前后化合价变化情况是
,氯元素反应前后化合价变化情况是______ (填“升高”或“降低”)。
(3)硫酸镁溶液在不同温度下进行浓缩结晶,可得到不同的晶体:
①“操作1”的具体操作是:蒸发浓缩滤液至表面有晶膜出现(此时MgSO4溶液已饱和)、______ 、过滤、洗涤、低温干燥。
②“操作1”所得滤液中能分离出一种可循环使用的物质,该物质是______ (填化学式)。循环使用的目的是______ 。
(4)已知:MgSO4·7H2O中镁元素质量分数为9.76%,采用热分析法测定所得MgSO4·7H2O样品中镁元素质量分数:
①未加热前,测得样品中镁元素质量分数略大于9.76%,可能的原因是______ 。
②高于900℃后,测得剩余固体中镁元素质量分数大于20%,可能的原因是______ 。
(5)若用100t菱镁矿石可制得246 t MgSO4·7H2O产品,忽略反应过程中镁元素损失,求该菱镁矿石中MgCO3的质量分数。(写出计算过程)______ 。
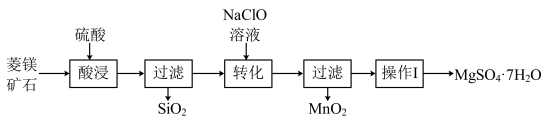
(2)“转化”时主要反应是
(3)硫酸镁溶液在不同温度下进行浓缩结晶,可得到不同的晶体:
| 温度/℃ | -3.9-1.8 | 1.8-48.1 | 48.1-67.5 | 67.5-200 |
| 析出晶体 | MgSO4·12H2O | MgSO4·7H2O | MgSO4·6H2O | MgSO4·H2O等 |
②“操作1”所得滤液中能分离出一种可循环使用的物质,该物质是
(4)已知:MgSO4·7H2O中镁元素质量分数为9.76%,采用热分析法测定所得MgSO4·7H2O样品中镁元素质量分数:
①未加热前,测得样品中镁元素质量分数略大于9.76%,可能的原因是
②高于900℃后,测得剩余固体中镁元素质量分数大于20%,可能的原因是
(5)若用100t菱镁矿石可制得246 t MgSO4·7H2O产品,忽略反应过程中镁元素损失,求该菱镁矿石中MgCO3的质量分数。(写出计算过程)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网