科学探究题 较难0.4 引用4 组卷1841
小明进行H2O2溶液制O2的实验探究。结合下列过程,回答有关问题。
(1)MnO2作催化剂,向5mL5%的H2O2溶液中加入少量MnO2,立即产生大量气泡。
①写出用H2O2溶液制备O2的化学方程式:____________________________________ 。
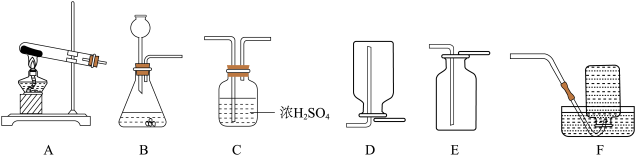
②用上述反应原理制备并收集一瓶干燥的O2,从所给装置图中选择并组装一套装置,其连接顺序为_______ → __________ → ________ (填标号)。为了确保实验成功,在装药品之前应该_________ 。
③检验O2的方法是___________________________ ,若木条复燃,则证明收集的气体为O2。
(2)FeCl3溶液做催化剂
向5mL5%的H2O2溶液中加入2滴一定浓度的 FeCl3溶液,立即产生大量气泡。
【已知】FeCl3溶液中主要含有三种微粒:H2O、Fe3+、Cl-
【问题】那种微粒对H2O2溶液的分解起催化作用?
【假设】假设一:可能是H2O
假设二:可能是Fe3+
假设三:可能是Cl-
【分析】①假设一不可能成立,理由是__________________________________________ 。
【实验】
【结论】②假设___ 成立,而假设一和另一种假设不成立。
③催化剂比较从循环利用的角度分析,_____ (填化学式)更适合做该反应的催化剂。
(1)MnO2作催化剂,向5mL5%的H2O2溶液中加入少量MnO2,立即产生大量气泡。

①写出用H2O2溶液制备O2的化学方程式:
②用上述反应原理制备并收集一瓶干燥的O2,从所给装置图中选择并组装一套装置,其连接顺序为
③检验O2的方法是
(2)FeCl3溶液做催化剂
向5mL5%的H2O2溶液中加入2滴一定浓度的 FeCl3溶液,立即产生大量气泡。
【已知】FeCl3溶液中主要含有三种微粒:H2O、Fe3+、Cl-
【问题】那种微粒对H2O2溶液的分解起催化作用?
【假设】假设一:可能是H2O
假设二:可能是Fe3+
假设三:可能是Cl-
【分析】①假设一不可能成立,理由是
【实验】
| 操作 | 现象 |
| 其他条件不变,向H2O2溶液中加入NaCl溶液 | 无明显变化 |
| 其他条件不变,向H2O2溶液中加入Na2SO4溶液 | 无明显变化 |
| 其他条件不变,向H2O2溶液中加入Fe2(SO4)3溶液 | 立即产生大量气泡 |
③催化剂比较从循环利用的角度分析,
2018·广东深圳·中考真题
类题推荐
同学们为了研究氧化铁能否在氯酸钾制取氧气的实验中起催化作用,进行了以下实验,如表所示:
【资料】①氯酸钾分解反应的化学方程式为
②氯酸钾和氯化钾均能溶于水。
【实验一】氧化铁能否在氯酸钾制取氧气实验中加快反应速率。
(1)实验3中氧化铁的质量为__________ 。
(2)以上实验采用了__________ 的实验方法。
(3)实验一得到的结论是__________ 。
【实验二】为证明氧化铁是该反应的催化剂,同学们又完成了以下的实验:
Ⅰ.在实验3反应后的混合物中加足量的水溶解,过滤得到红色固体,洗涤干燥并用电子天平称量,质量为0.2g。
Ⅱ.将一定量的 通入滤出的固体,按图进行实验:
通入滤出的固体,按图进行实验:

甲同学的实验报告如表所示:
(4)写出A中玻璃管内发生反应的化学方程式________________ 。
【实验结论】氧化铁在氯酸钾制取氧气反应中起催化作用。
【实验反思】乙同学查阅资料发现一氧化碳还原氧化铁后剩余固体可能由氧化亚铁、四氧化三铁、铁粉和未反应的氧化铁中的一种或几种组成。
为了研究剩余固体的成分,丙同学查阅了以下资料,如表所示:
(5)丙同学认为剩余固体中一定没有氧化铁,原因是________________ 。
(6)测定剩余固体的组成,并填入表中。
【资料】①氯酸钾分解反应的化学方程式为
②氯酸钾和氯化钾均能溶于水。
| 实验编号 | 氧化物 | 产生气体的体积(mL) | 耗时(s) | |
| 1 | 0.6 | / | 67 | 1800 |
| 2 | 0.6 | 0.2g二氧化锰 | 67 | 36.5 |
| 3 | 0.6 | __ g氧化铁 | 67 | 89.5 |
(1)实验3中氧化铁的质量为
(2)以上实验采用了
(3)实验一得到的结论是
【实验二】为证明氧化铁是该反应的催化剂,同学们又完成了以下的实验:
Ⅰ.在实验3反应后的混合物中加足量的水溶解,过滤得到红色固体,洗涤干燥并用电子天平称量,质量为0.2g。
Ⅱ.将一定量的

甲同学的实验报告如表所示:
| 装置 | 实验现象 | 实验分析 |
| A | 红色固体全部变黑 | 生成了铁 |
| B | 石灰水变浑浊 | 产生二氧化碳 |
【实验结论】氧化铁在氯酸钾制取氧气反应中起催化作用。
【实验反思】乙同学查阅资料发现一氧化碳还原氧化铁后剩余固体可能由氧化亚铁、四氧化三铁、铁粉和未反应的氧化铁中的一种或几种组成。
为了研究剩余固体的成分,丙同学查阅了以下资料,如表所示:
| 铁粉 | 氧化亚铁 | 氧化铁 | 四氧化三铁 | |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 磁性 | 有 | 无 | 无 | 有 |
| 与 | 不反应 | 反应 | 反应 | 反应 |
| 与稀盐酸反应 | 反应 | 生成氯化亚铁和水 | 生成氯化铁和水 | 生成氯化亚铁、氯化铁和水 |
| 与硫酸铜溶液反应 | 反应 | 不反应 | 不反应 | 不反应 |
(6)测定剩余固体的组成,并填入表中。
| 步骤 | 实验操作 | 实验现象 | 结论和解释 |
| 1 | 用磁铁吸引剩余固体 | 剩余固体中没有氧化亚铁 | |
| 2 | 剩余固体中只有铁粉 |
实验室用氯酸钾制氧气常用二氧化锰作催化剂。某兴趣小组希望寻找到一种廉价易得的MnO2替代品。通过查阅资料,他们选择了两种替代品:碗渣、红砖。其中碗渣和红砖经粉碎后,分成“60目”和“30目”两种颗粒大小不同的粉末(目数越高,颗粒越小)。下表是相关实验数据记录:
(1)该实验可以比较___________(填字母)对收集O2速率的影响。
(2)实验3、4可得出催化剂目数与反应分解速率的关系是:其他条件相同时,___________ 。由此可推测出x的数值为___________ (填字母编号)。
A.10.6 B.21.1 C.23.8 D.49.1
(3)表中所列催化剂的催化效果最佳的是实验___________ (填数字),请写出这种物质催化分解KC1O3化学方程式___________ ,若用该方法进行实验,当气体质量不再增加时,试管中剩余固体质量为___________ g。
| 编号 | KC1O3质量/g | 催化剂 | 催化剂质量/g | 收集O2平均速率mL。min-1 |
| 实验1 | 0.49 | 无 | 0 | 11.8 |
| 实验2 | 0.49 | MnO2 | 0.2 | 28.2 |
| 实验3 | 0.49 | 碗渣粉(60目) | 0.2 | 49.1 |
| 实验4 | 0.49 | 碗渣粉(30目) | 0.2 | 23.7 |
| 实验5 | 0.49 | 红砖粉(60目) | 0.2 | 28.3 |
| 实验6 | 0.49 | 红砖粉(30目) | 0.2 | x |
| A.有无催化剂 | B.催化剂种类 |
| C.催化剂的质量 | D.催化剂颗粒大小 |
A.10.6 B.21.1 C.23.8 D.49.1
(3)表中所列催化剂的催化效果最佳的是实验
某研究小组发现,将适量淀粉放入过氧化氢溶液中,过氧化氢溶液的分解速率加快。对于此现象,该小组同学进行了如下探究:
【提出问题】淀粉能否作过氧化氢分解的催化剂?
【作出猜想】淀粉能作过氧化氢分解的催化剂
(1)【实验验证】
写出淀粉催化过氧化氢分解的文字(或符号)表达式:_______ 。
【拓展探究】探究小组想验证向上排空气法收集的氧气是否纯净,进行了几组实验,取几只集气瓶,分别装入其总体积不同含量的水用排水法收集氧气,恰好把几只集气瓶中的水排去。将带火星的木条依次插入集气瓶中,发现收集的氧气占容积的体积分数最低为35%时,木条复燃。
(2)从以上探究可知:使用带火星木条验满氧气的方法是否可靠_______ ?(填“是”或“否”)。
(3)空气中氧气的体积分数占_______ %。
(4)当收集的氧气占容积的体积分数最低为35%时,可使带火星的木条复燃,这时集气瓶(容积为200mL)中氧气的体积分数是_______ %(写出计算过程,结果保留整数)。
【提出问题】淀粉能否作过氧化氢分解的催化剂?
【作出猜想】淀粉能作过氧化氢分解的催化剂
(1)【实验验证】
| 实验步骤 | 实验现象 | 结论及解释 |
| I.在盛有5mL5%过氧化氢的试管中加入ag淀粉 | 产生大量能使带火星木条复燃的气体 | 产生的气体是 |
| II.试管中重新加入的5mL5%过氧化氢溶 液,反应停止后过滤、洗涤、干燥、称量滤渣 | ①又产生大量使带火星木条复燃的气体 ②滤渣质量为ag | ①淀粉 ②淀粉能作过氧化氢分解的 |
【拓展探究】探究小组想验证向上排空气法收集的氧气是否纯净,进行了几组实验,取几只集气瓶,分别装入其总体积不同含量的水用排水法收集氧气,恰好把几只集气瓶中的水排去。将带火星的木条依次插入集气瓶中,发现收集的氧气占容积的体积分数最低为35%时,木条复燃。
(2)从以上探究可知:使用带火星木条验满氧气的方法是否可靠
(3)空气中氧气的体积分数占
(4)当收集的氧气占容积的体积分数最低为35%时,可使带火星的木条复燃,这时集气瓶(容积为200mL)中氧气的体积分数是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


