科学探究题 适中0.65 引用1 组卷54
实验室中有一包白色粉末,可能是碳酸钠,也可能是氧化钙或氢氧化钙。为确定其组成,某同学设计了以下实验方案进行探究,请你按要求帮助完成探究活动。
(1)提出假设:
假设① 白色粉末是碳酸钠
假设② 白色粉末是氧化钙
假设③ 白色粉末是氢氧化钙
(2)设计实验,通过实验分析进行判断并填空:
(3)实验后思考:假定这包白色粉末是混有少量氧化钙的碳酸钠粉末,将混合物溶于水可观察到的现象是____________ ;若恰好完全反应,将反应后的混合物进行分离,分离的方法是________ ;再将分离后的溶液蒸干,得到的固体物质是______ (填化学式)。
(1)提出假设:
假设① 白色粉末是碳酸钠
假设② 白色粉末是氧化钙
假设③ 白色粉末是氢氧化钙
(2)设计实验,通过实验分析进行判断并填空:
| 假设 | 设计的相关实验操作 | 实验中观察到的现象 | 假设是否成立 |
| ① | 取一定量粉末加入稀盐酸 | 假设①不成立 | |
| ② | 取一定量粉末溶于水 | 溶液浑浊且温度升高 | 假设②成立 |
| ③ | 取一定量粉末溶于水,静置后取上层清液再通入二氧化碳 | 没有沉淀产生 | 假设③ |
(3)实验后思考:假定这包白色粉末是混有少量氧化钙的碳酸钠粉末,将混合物溶于水可观察到的现象是
2018·湖北恩施·一模
类题推荐
Na2CO3和 NaHCO3有相似的化学性质,都能与酸、某些碱反应。
【查阅资料】获得如下信息:
①氯化钙溶液呈中性,与碳酸氢钠溶液混合不发生反应。
②碳酸钠稳定,而NaHCO3受热分解: 。
。
(1)NaHCO3遇到盐酸的化学反应方程式为_____ 。
(2)工业上用碳酸钠制烧碱的化学反应方程式为_____ 。
(3)同学们在探究其化学性质实验后,将剩余固体药品集中放在烧杯中。小明为了弄清剩余固体的成分,进行了如下的探究:
【提出猜想】剩余固体是:I、Na2CO3;Ⅱ、NaHCO3;Ⅲ、_____ 。
【进行实验】
【结论分析】
①据上述实验现象,小明认为猜想Ⅲ正确。但有同学认为小明的判断不严谨,因为猜想_____ 也有相同现象。
②同学们讨论后认为,如要确定剩余固体成分,小明只要在做实验操作①时,改动一下操作,滴加_____ ,出现 _____ 现象,即可得出猜想Ⅲ正确结论。
【查阅资料】获得如下信息:
①氯化钙溶液呈中性,与碳酸氢钠溶液混合不发生反应。
②碳酸钠稳定,而NaHCO3受热分解:
(1)NaHCO3遇到盐酸的化学反应方程式为
(2)工业上用碳酸钠制烧碱的化学反应方程式为
(3)同学们在探究其化学性质实验后,将剩余固体药品集中放在烧杯中。小明为了弄清剩余固体的成分,进行了如下的探究:
【提出猜想】剩余固体是:I、Na2CO3;Ⅱ、NaHCO3;Ⅲ、
【进行实验】
| 操作 | 现象 | 结论 |
| ①取少量剩余固体于试管中,加入足量水,充分溶解后,滴加几滴酚酞溶液。 | 溶液由无色变 | 剩余固体一定有: |
| ②取适量剩余固体于试管中,固定在铁架台上,充分加热。 | 白色固体质量减少,试管内壁有较多水珠出现。 |
【结论分析】
①据上述实验现象,小明认为猜想Ⅲ正确。但有同学认为小明的判断不严谨,因为猜想
②同学们讨论后认为,如要确定剩余固体成分,小明只要在做实验操作①时,改动一下操作,滴加
某校化学兴趣小组对如何鉴别生活中的苏打(Na2CO3)和小苏打(NaHCO3),进行了下列探究: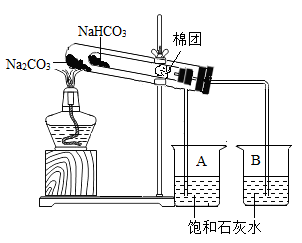
(查阅资料)
①相同条件下,碳酸钠溶液比碳酸氢钠溶液的碱性强;
②270℃时,NaHCO3会完全分解生成二氧化碳、水及一种白色固体,而Na2CO3不易分解:
③常见的碳酸盐中,只有碳酸钠、碳酸钾和碳酸铵溶于水,其它碳酸盐大多不溶于水。
(实验探究)
(1)充分加热后,A、B两烧杯中的现象分别为__ 、__ 、__ ,由此可得出的结论是__ 。
(2)现有浓度相同的Na2CO3与NaHCO3溶液,充分利用所学知识和资料,你认为区分二者最简单的方法是__ 。
A 加热 B 用pH试纸测溶液pH C 滴加稀盐酸
(反思与评价)
(1)常用小苏打治疗轻度胃酸过多的病人,原因是___ (用化学方程式表示)。
(2)检验碳酸钠粉未中是否含有碳酸氢钠的方法是____ 。
(拓展延伸)该兴趣小组同学认为,充分加热NaHCO3后的白色固体产物可能是NaOH或Na2CO3。
(1)他们猜想的依据是_____ 。
(2)设计实验检验反应后的固体产物是NaOH还是Na2CO3,并完成下表(限选试剂及仪器:稀盐酸、氯化钡溶液、澄清石灰水、酚酞试液、蒸馏水、试管、胶头滴管)。

(查阅资料)
①相同条件下,碳酸钠溶液比碳酸氢钠溶液的碱性强;
②270℃时,NaHCO3会完全分解生成二氧化碳、水及一种白色固体,而Na2CO3不易分解:
③常见的碳酸盐中,只有碳酸钠、碳酸钾和碳酸铵溶于水,其它碳酸盐大多不溶于水。
(实验探究)
(1)充分加热后,A、B两烧杯中的现象分别为
(2)现有浓度相同的Na2CO3与NaHCO3溶液,充分利用所学知识和资料,你认为区分二者最简单的方法是
A 加热 B 用pH试纸测溶液pH C 滴加稀盐酸
(反思与评价)
(1)常用小苏打治疗轻度胃酸过多的病人,原因是
(2)检验碳酸钠粉未中是否含有碳酸氢钠的方法是
(拓展延伸)该兴趣小组同学认为,充分加热NaHCO3后的白色固体产物可能是NaOH或Na2CO3。
(1)他们猜想的依据是
(2)设计实验检验反应后的固体产物是NaOH还是Na2CO3,并完成下表(限选试剂及仪器:稀盐酸、氯化钡溶液、澄清石灰水、酚酞试液、蒸馏水、试管、胶头滴管)。
| 序号 | 实验操作 | 实验现象 | 实验结论 |
| ① | 取少量加热后的固体产物于试管A中,加入适量蒸馏水并充分振荡溶解,再加入足量 | 产生白色沉淀 | 产物中含有Na2CO3 |
| ② | 取操作①后的上层清液于试管B中,滴加 | 产物中不含NaOH |
如图是某果蔬洗涤盐说明书。小明对配料表中的成分很好奇:食盐可用于杀菌消毒,为什么要加入pH调节剂,它的成分是什么?
【查阅资料】①该品牌果蔬洗涤盐pH调节剂的成分可能是碳酸钠、碳酸氢钠、酒石酸、柠檬酸中的一种或两种。pH调节剂能维持渗透压、控制酸碱平衡。
②大多数农药是酸性的。③碳酸氢钠受热易分解为二氧化碳和碳酸钠等三种物质,碳酸钠则有较高的热稳定性,二者的溶液都显碱性。
(1)【实验初探】取少量该固体溶于水配成溶液A,用pH试纸测得该溶液的pH=10,该洗涤盐溶液显______ 性,则pH调节剂中一定不含的物质是______ 。
【猜想与假设】该配料表中的pH调节剂可能是:①碳酸钠;②碳酸氢钠;③______ 。
(2)【实验再探】
请写出上表操作①中反应的化学方程式______ 。
请写出上表操作②中碳酸氢钠分解的化学方程式______ 。
【分析与结论】猜想③正确
(3)【反思与评价】
①你认为果蔬洗涤盐中pH调节剂的作用是什么______ 。
②该商品配料表中有一处表述不恰当,请你改正过来______ 。
| 品牌:X盐 名称:果蔬洗涤盐 净含量:400g 保质期:五年 储存方法:常温下置于干燥处存放,防潮 配料表:食用精制食盐、食品级pH调节剂 |
②大多数农药是酸性的。③碳酸氢钠受热易分解为二氧化碳和碳酸钠等三种物质,碳酸钠则有较高的热稳定性,二者的溶液都显碱性。
(1)【实验初探】取少量该固体溶于水配成溶液A,用pH试纸测得该溶液的pH=10,该洗涤盐溶液显
【猜想与假设】该配料表中的pH调节剂可能是:①碳酸钠;②碳酸氢钠;③
(2)【实验再探】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少许A溶液于试管中,滴加氯化钙溶液 | 有白色沉淀生成 | |
| ②取适量洗涤盐,加热,将生成的气体通入澄清石灰水 | 观察到 | 证明该pH调节剂中含有碳酸氢钠。 |
请写出上表操作②中碳酸氢钠分解的化学方程式
【分析与结论】猜想③正确
(3)【反思与评价】
①你认为果蔬洗涤盐中pH调节剂的作用是什么
②该商品配料表中有一处表述不恰当,请你改正过来
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


