科学探究题 适中0.65 引用1 组卷101
化学是以实验为基础的科学,实验是科学探究的重要手段。
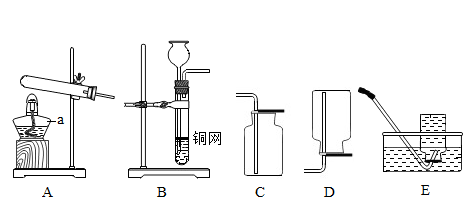
(1)如图是初中化学常见的仪器和装置,请回答下列问题。
①写出a的名称____________ ;②实验室选用装置A、E组合制取氧气,写出反应的化学方程式__________ ;③实验室用B、C装置制取二氧化碳时,若用铁丝网代替铜网,产生的后果是__________ 。
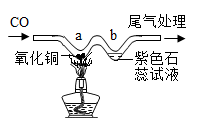
(2)如图所示,用“W”型玻璃管进行微型实验。
①b处发生的现象是_____________ ;②写出a处发生反应的化学方程式__________ ;③请简述该实验的尾气处理方法_____________ 。
(3)可燃冰(天然气水合物)是资源量丰富的高效清洁能源。科学家开采出一种可燃冰,取100g样品放置在一密闭容器内,该样品迅速转化为甲烷和水,将甲烷分离并完全燃烧,得到35.2g二氧化碳。求该可燃冰样品中甲烷的质量分数(精确到0.1%)_____ 。

(1)如图是初中化学常见的仪器和装置,请回答下列问题。
①写出a的名称

(2)如图所示,用“W”型玻璃管进行微型实验。
①b处发生的现象是
(3)可燃冰(天然气水合物)是资源量丰富的高效清洁能源。科学家开采出一种可燃冰,取100g样品放置在一密闭容器内,该样品迅速转化为甲烷和水,将甲烷分离并完全燃烧,得到35.2g二氧化碳。求该可燃冰样品中甲烷的质量分数(精确到0.1%)
2018·河南洛阳·一模
类题推荐
相同的反应物在不同外界条件下,会发生不同的反应。
I.CO2与NaOH反应的产物与反应物的量有关。
【资料】
①少量CO2得到Na2CO3;过量CO2得到NaHCO3。反应的化学方程式 ;
; 。
。
②铝、锌、铁、铜的盐溶液与NaHCO3溶液混合不会产生沉淀。
【提出问题】将CO2通入NaOH溶液反应后,溶液中溶质是什么?
【猜想与假设】
(1)猜想①:Na2CO3。
猜想②:NaHCO3。
猜想③:Na2CO3、NaOH。
猜想④:______ 。
【实验与探究】
(2)请完善下面的表格。
【定量分析】
(3)将4 gNaOH固体溶解在100mL水中,理论上通入______ gCO2气体,所得溶液中溶质只有Na2CO3。
【拓展】
(4)实验室用澄清石灰水检验二氧化碳时,如果向一定量的澄清石灰水中不断通入二氧化碳气体,下列图像能正确反映生成的碳酸钙沉淀与二氧化碳的质量之间变化关系的是______。(填字母序号,碳酸氢钙可溶于水)
Ⅱ.Na2CO3与盐酸反应的产物也与反应物的量有关。
【资料】少量盐酸与Na2CO3反应先得到NaHCO3,继续加入盐酸才能生成CO2,反应的化学方程式: ;
; 。
。
【实验】
(5)有两瓶无色溶液a和b,分别是碳酸钠溶液和稀盐酸,要求只用试管和胶头滴管鉴别两种物质,并填写实验表格。
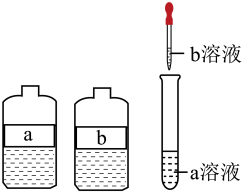
还有许多化学反应的产物也与反应物的量有关,试举一例:________ 。
I.CO2与NaOH反应的产物与反应物的量有关。
【资料】
①少量CO2得到Na2CO3;过量CO2得到NaHCO3。反应的化学方程式
②铝、锌、铁、铜的盐溶液与NaHCO3溶液混合不会产生沉淀。
【提出问题】将CO2通入NaOH溶液反应后,溶液中溶质是什么?
【猜想与假设】
(1)猜想①:Na2CO3。
猜想②:NaHCO3。
猜想③:Na2CO3、NaOH。
猜想④:
【实验与探究】
(2)请完善下面的表格。
| 实验操作 | 实验现象 | 结论 |
| 取适量反应后的溶液于试管中加入适量的CaCl2溶液,振荡;再加入 | 若 | 猜想②成立 |
| 取适量反应后的溶液于试管中,加入过量的CaCl2溶液,振荡;过滤。取滤液于另一支试管中,滴加 | 若产生白色沉淀; | 猜想③成立 |
【定量分析】
(3)将4 gNaOH固体溶解在100mL水中,理论上通入
【拓展】
(4)实验室用澄清石灰水检验二氧化碳时,如果向一定量的澄清石灰水中不断通入二氧化碳气体,下列图像能正确反映生成的碳酸钙沉淀与二氧化碳的质量之间变化关系的是______。(填字母序号,碳酸氢钙可溶于水)
A.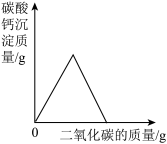 | B.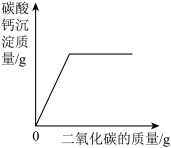 |
C.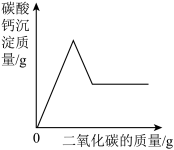 | D.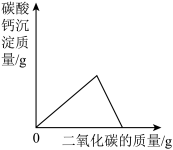 |
Ⅱ.Na2CO3与盐酸反应的产物也与反应物的量有关。
【资料】少量盐酸与Na2CO3反应先得到NaHCO3,继续加入盐酸才能生成CO2,反应的化学方程式:
【实验】
(5)有两瓶无色溶液a和b,分别是碳酸钠溶液和稀盐酸,要求只用试管和胶头滴管鉴别两种物质,并填写实验表格。

| 操作 | 现象与结论 |
| 取适量a溶液于试管中,用胶头滴管逐滴滴入b溶液并振荡 | 若看到 |
某化学兴趣小组查阅资料,得知氧化铜( )可能也能催化过氧化氢的分解,为验证真伪,进行了如下探究。
)可能也能催化过氧化氢的分解,为验证真伪,进行了如下探究。
【猜想】
(1)Ⅰ. 不是催化剂,也不参与反应
不是催化剂,也不参与反应
Ⅱ. 参与反应产生氧气
参与反应产生氧气
Ⅲ._________
【实验】用天平称量 ,取
,取 的过氧化氢溶液于试管中,进行如下实验:
的过氧化氢溶液于试管中,进行如下实验:
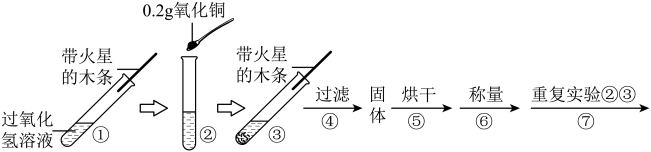
(2)将猜想Ⅲ补充完整:
(3)步骤①的目的_________ 。
(4)步骤④需要用到玻璃棒,其作用是_________ 。
(5)若实验过程中共收集到氧气的质量为 ,则参加反应的过氧化氢质量为
,则参加反应的过氧化氢质量为_________ 。
【猜想】
(1)Ⅰ.
Ⅱ.
Ⅲ.
【实验】用天平称量

(2)将猜想Ⅲ补充完整:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
溶液中有气泡放出,带火星的木条复燃猜 | 想Ⅰ、Ⅱ不成立,猜想Ⅲ成立 |
(4)步骤④需要用到玻璃棒,其作用是
(5)若实验过程中共收集到氧气的质量为
某同学在博物馆看到一些铜制文物上有绿色的锈迹后,对绿色锈迹产生了探究兴趣。该同学查阅资料得知:
Ⅰ.绿色锈迹是碱式碳酸铜【Cu2(OH)2CO3】,受热易分解。
Ⅱ.无水硫酸铜为白色粉末,遇水变蓝。
Ⅲ.碱石灰是CaO和NaOH的固体混合物,NaOH与CO2反应生成碳酸钠和水。
Ⅳ.氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中。
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成。为了进一步确定碱式碳酸铜受热分解的产物,进行了如下猜想与探究:
(1)该黑色固体可能是①碳粉;②氧化铜:③_______ 。
请帮助该同学完成下述实验方案设计与记录。
(2)对于“加热碱式碳酸铜,试管壁上有无色液滴生成”的现象,该同学猜想无色液滴可能是水,根据反应前后元素守恒,猜想分解产物还有CO2,并选择如图所示装置进行探究。
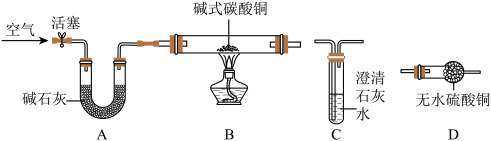
①实验步骤:
步骤一:连接A和B,打开活塞,通入一段时间的空气。
步骤二:关闭活塞,依次连接装置A→B→_______ →_______ (填“C”、“D”)。
步骤三:点燃酒精灯,观察到明显现象后,停止加热。
②当观察到_______ ,可以得出碱式碳酸铜受热分解生成了H2O,根据装置C的实验现象可以得出碱式碳酸铜受热分解生成了CO2,请写出C中反应的化学方程式_______ 。理论上,221克的碱式碳酸铜能生成_______ 克氧化铜。
③上述装置A中碱石灰的作用是_______ 。
Ⅰ.绿色锈迹是碱式碳酸铜【Cu2(OH)2CO3】,受热易分解。
Ⅱ.无水硫酸铜为白色粉末,遇水变蓝。
Ⅲ.碱石灰是CaO和NaOH的固体混合物,NaOH与CO2反应生成碳酸钠和水。
Ⅳ.氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中。
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成。为了进一步确定碱式碳酸铜受热分解的产物,进行了如下猜想与探究:
(1)该黑色固体可能是①碳粉;②氧化铜:③
请帮助该同学完成下述实验方案设计与记录。
| 实验操作 | 现象 | 实验结论 |
| 将少量黑色固体放入试管中,加入 | 猜想②正确 |

①实验步骤:
步骤一:连接A和B,打开活塞,通入一段时间的空气。
步骤二:关闭活塞,依次连接装置A→B→
步骤三:点燃酒精灯,观察到明显现象后,停止加热。
②当观察到
③上述装置A中碱石灰的作用是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


