综合应用题 适中0.65 引用1 组卷97
骗子往往披着科学的外衣,而科学可以给我们一双明辨是非的眼睛。例如:有人提出使用 “高科技的添加剂”可以使水变成汽油。小明同学在学习过物质构成的奥秘后,认为可以用物质组成的观点解开这个骗局。
【提出问题】根据水的组成和汽油的组成判断,水是否可以变成汽油。
【猜想与验证】
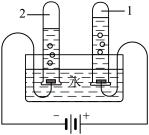
(1)确定水的组成。实验装置如右图所示:通电一段时间后,试管1和试管2中所收集的气体体积比约为_______ 。对两支试管中的气体进行检验,试管1中的气体可使 _______ (填现象),说明是 _________ 。
实验结论:水是由氢元素和氧元素组成的。电解水的化学方程式 : ___________________ 。
(2)确定汽油的成分。操作如下:
【实验结论】汽油的组成元素为______________ 。汽油和水的组成元素不同,水不能变成汽油。

【提出问题】根据水的组成和汽油的组成判断,水是否可以变成汽油。
【猜想与验证】
(1)确定水的组成。实验装置如右图所示:通电一段时间后,试管1和试管2中所收集的气体体积比约为
实验结论:水是由氢元素和氧元素组成的。电解水的
(2)确定汽油的成分。操作如下:
| 实验步骤 | 实验现象 | 结论 |
| ①点燃使用汽油作燃料的油灯 ②将光洁干冷的烧杯罩在油灯火焰上方 | 现象: | 证明汽油在空气中燃烧后的产物中有 |
| ③将内壁蘸有 的烧杯罩在油灯火焰上方 | 现象: | 证明汽油在空气中燃烧后的产物中有二氧化碳 |
【实验结论】汽油的组成元素为
18-19九年级上·江西赣州·期中
类题推荐
氢能是一种极具发展潜力的清洁能源。
I.甲烷热解制氢
高温时,以熔融金属锡(Sn)为液态传热介质,细小的甲烷气泡从鼓泡反应器底部注入并发生分解,得到固体石墨。反应原理示意图如图所示。
已知:物质的部分性质
_______________ 。
(2)该反应温度T3与金属锡的熔点T1、沸点T2三者之间的大小关系为_______________ 。
(3)该方法可避免石墨在介质中大量附着,主要原因是_______________ 。
II.海水电解制氢
海水无淡化直接电解制氢的原理和装置如图所示。PTFE膜两侧有水蒸气压力差,使膜外侧的水转化为水蒸气,水蒸气通过PTFE膜后液化。液态水和高分子均不能直接通过PTFE膜。_______________ 。
(5)在电解过程中,PTFE膜内侧KOH溶液的溶质质量分数保持不变,原因是____________ 。
Ⅲ.热化学循环制氢
一种循环利用Zn/ZnO制氢的原理如下。
反应l:
反应2:
(6)理论上产生氢气与氧气的质量比为_______________ 。
(7)已知ZnO在2000℃左右充分分解,但反应1分离得到的Zn很少,若往装置中充入氩气,制得到的Zn明显增加。可能的原因是_______________ 。
I.甲烷热解制氢
高温时,以熔融金属锡(Sn)为液态传热介质,细小的甲烷气泡从鼓泡反应器底部注入并发生分解,得到固体石墨。反应原理示意图如图所示。
已知:物质的部分性质
| 液态锡 | 石墨 | |
| 密度g/cm3 | 7.0 | 2.2 |
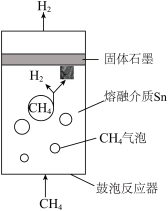
(2)该反应温度T3与金属锡的熔点T1、沸点T2三者之间的大小关系为
(3)该方法可避免石墨在介质中大量附着,主要原因是
II.海水电解制氢
海水无淡化直接电解制氢的原理和装置如图所示。PTFE膜两侧有水蒸气压力差,使膜外侧的水转化为水蒸气,水蒸气通过PTFE膜后液化。液态水和高分子均不能直接通过PTFE膜。
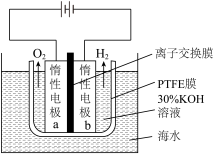
(5)在电解过程中,PTFE膜内侧KOH溶液的溶质质量分数保持不变,原因是
Ⅲ.热化学循环制氢
一种循环利用Zn/ZnO制氢的原理如下。
反应l:
反应2:
(6)理论上产生氢气与氧气的质量比为
(7)已知ZnO在2000℃左右充分分解,但反应1分离得到的Zn很少,若往装置中充入氩气,制得到的Zn明显增加。可能的原因是
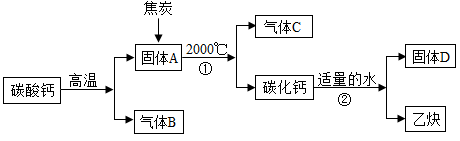
工业上生产电石(CaC2)并制备重要工业原料乙炔(CxHy)流程如下:
(资料)
1 碳酸钙高温分解可得两种氧化物,且变化前后元素化合价不变。
2 浓硫酸具有强吸水性,碱石灰能吸收CO2和水。
3 含碳、氢元素的化合物完全燃烧生成CO2和水,反应前后各元素质量不变。
(讨论)
(1)碳酸钙高温分解的化学方程式为___________ 。
(2)C有毒,与B组成元素相同,但二者化学性质不同,原因是___________ 。
(3)D的水溶液可用于实验室检验气体B,D的化学式是___________ 。
(测定乙炔组成)
资料:一个乙炔分子有四个原子构成。
(4)将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过如图的___________ (选填“甲”或“乙”)装置,并再缓缓通一段时间的N2,并记录实验数据于表中。

(5)实验中“缓缓通一段时间的N2”的目的是___________ 。
(6)计算:乙炔中碳元素质量为___________ g,氢元素质量为___________ g,乙炔化学式为___________ 。

(资料)
1 碳酸钙高温分解可得两种氧化物,且变化前后元素化合价不变。
2 浓硫酸具有强吸水性,碱石灰能吸收CO2和水。
3 含碳、氢元素的化合物完全燃烧生成CO2和水,反应前后各元素质量不变。
(讨论)
(1)碳酸钙高温分解的化学方程式为
(2)C有毒,与B组成元素相同,但二者化学性质不同,原因是
(3)D的水溶液可用于实验室检验气体B,D的化学式是
(测定乙炔组成)
资料:一个乙炔分子有四个原子构成。
(4)将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过如图的

| 装置 | 反应前质量 | 反应后质量 |
| 浓硫酸 | 125.3g | 127.1g |
| 碱石灰 | 78.2g | 87.0g |
(6)计算:乙炔中碳元素质量为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网