科学探究题 困难0.15 引用2 组卷345
镁是20世纪才发展起来的年轻金属,广泛应用于航空、汽车、船舶、通讯电子和国防工业等。兴趣小组同学对金属镁进行了如下探究。
(一)有关金属镁的化学性质探究
兴趣小组同学根据金属的化学性质,知道金属镁能与O2、稀盐酸和CuSO4溶液反应,并设计了如下实验进行验证(以下实验用镁条、镁条均已除去氧化膜)。
(1)兴趣小组同学把镁粉轻轻洒在酒精灯的火焰上,观察到火焰上跳动闪烁着点点银色火花,如绽放的美丽烟花。该反应的化学方程式是_______________________ 。
(2)兴趣小组同学探究镁与稀盐酸的反应,除观察到预期现象外,还观察到有灰白色沉淀生成的“异常”现象。于是进行了以下探究。
【实验1】向4份相同体积与浓度的稀盐酸中分别加入一定长度的某种镁带,现象如下:
【实验结论1】据表分析,________________ 是实验出现“异常”的因素之一。
【实验2】向4份相同体积与浓度的稀硫酸中分别加入一定长度的某种镁带,现象如下:
【实验结论2】对比实验1和实验2,______________ 是实验出现“异常”的因素之一。
(3)兴趣小组同学取一支试管,放入一根镁条,加入一定量硫酸铜溶液,观察到镁条表面有少量气泡产生,且有黑色物质生成。同学们对此实验的现象感到意外和困惑,于是查阅到了相关资料:
资料1:硫酸铜溶液在配制时加入了少量稀硫酸;
资料2:当金属粉末颗粒很小时,容易成为黑色;
资料3:生成的黑色物质可能是CuO、Cu中的一种或两种。
①镁条与硫酸铜溶液反应的实验中产生的气体可能为______________ (写化学式)。
②同学们进一步设计实验确定黑色物质的成分,请在下表中补全实验方案。
通过以上探究,兴趣小组同学确定了黑色物质为Cu和CuO两种。
(二)有关镁条表面灰黑色“外衣”组成的探究
【发现问题】镁是一种银白色有金属光泽的金属,但久置的镁条总有一层灰黑色的“外衣”,这层灰黑色的“外衣”是什么物质呢?
【查阅资料】
(1)灰黑色“外衣”的成分是碱式碳酸镁晶体,化学式为:xMgCO3•yMg(OH)2•zH2O;
(2)Mg(OH)2:白色固体,难溶于水,受热会分解生成两种氧化物;
(3)MgCO3:白色固体,微溶于水,受热会分解生成两种氧化物;
(4)相同条件下,Mg(OH)2受热分解的温度比MgCO3分解的温度更低。
【组成测定】为精确测量碱式碳酸镁晶体的组成,兴趣小组同学取4.66g该晶体用热重分析仪对进行加热,使得各成份在不同温度下逐个分解(加热首先失去结晶水),测定剩余固体质量与分解温度之间关系(如下图所示)。
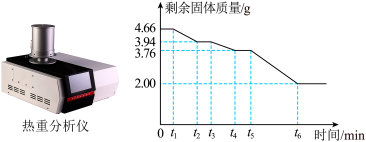
请回答下列问题:
(1)晶体中结晶水的质量为_______ g。
(2)t4~t5段中,固体为_________ (写化学式)。
(3)t5~t6段反应的化学方程式为________ 。
(4)根据图中数据计算xMgCO3•yMg(OH)2•zH2O中x:y:z =___________ (填最简比)。
(一)有关金属镁的化学性质探究
兴趣小组同学根据金属的化学性质,知道金属镁能与O2、稀盐酸和CuSO4溶液反应,并设计了如下实验进行验证(以下实验用镁条、镁条均已除去氧化膜)。
(1)兴趣小组同学把镁粉轻轻洒在酒精灯的火焰上,观察到火焰上跳动闪烁着点点银色火花,如绽放的美丽烟花。该反应的化学方程式是
(2)兴趣小组同学探究镁与稀盐酸的反应,除观察到预期现象外,还观察到有灰白色沉淀生成的“异常”现象。于是进行了以下探究。
【实验1】向4份相同体积与浓度的稀盐酸中分别加入一定长度的某种镁带,现象如下:
实验组别 | A | B | C | D |
镁带长度 | 1cm | 2cm | 3cm | 4cm |
沉淀量 | 无沉淀 | 少量沉淀 | 沉淀较多 | 沉淀很多 |
【实验2】向4份相同体积与浓度的稀硫酸中分别加入一定长度的某种镁带,现象如下:
实验组别 | A | B | C | D |
镁带长度 | 1cm | 2cm | 3cm | 4cm |
沉淀量 | 无沉淀 | 无沉淀 | 无沉淀 | 无沉淀 |
(3)兴趣小组同学取一支试管,放入一根镁条,加入一定量硫酸铜溶液,观察到镁条表面有少量气泡产生,且有黑色物质生成。同学们对此实验的现象感到意外和困惑,于是查阅到了相关资料:
资料1:硫酸铜溶液在配制时加入了少量稀硫酸;
资料2:当金属粉末颗粒很小时,容易成为黑色;
资料3:生成的黑色物质可能是CuO、Cu中的一种或两种。
①镁条与硫酸铜溶液反应的实验中产生的气体可能为
②同学们进一步设计实验确定黑色物质的成分,请在下表中补全实验方案。
| 实验操作 | 实验现象 | 结论 |
| 将黑色物质过滤、晾干后,分成两份 | / | / |
| 将其中一份装入硬质玻璃管中,向其中通入CO后,加热,并将生成的气体通入澄清石灰水中 | 黑色粉末中 含有CuO | |
| 将另一份置于坩埚中,称其质量为m1,在空气中加热一段时间后冷却,称其质量为m2 | m1 | 黑色粉末中 含有Cu |
(二)有关镁条表面灰黑色“外衣”组成的探究
【发现问题】镁是一种银白色有金属光泽的金属,但久置的镁条总有一层灰黑色的“外衣”,这层灰黑色的“外衣”是什么物质呢?
【查阅资料】
(1)灰黑色“外衣”的成分是碱式碳酸镁晶体,化学式为:xMgCO3•yMg(OH)2•zH2O;
(2)Mg(OH)2:白色固体,难溶于水,受热会分解生成两种氧化物;
(3)MgCO3:白色固体,微溶于水,受热会分解生成两种氧化物;
(4)相同条件下,Mg(OH)2受热分解的温度比MgCO3分解的温度更低。
【组成测定】为精确测量碱式碳酸镁晶体的组成,兴趣小组同学取4.66g该晶体用热重分析仪对进行加热,使得各成份在不同温度下逐个分解(加热首先失去结晶水),测定剩余固体质量与分解温度之间关系(如下图所示)。

请回答下列问题:
(1)晶体中结晶水的质量为
(2)t4~t5段中,固体为
(3)t5~t6段反应的化学方程式为
(4)根据图中数据计算xMgCO3•yMg(OH)2•zH2O中x:y:z =
18-19九年级上·江苏南京·期末
类题推荐
工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4,为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析。
【资料1】草酸晶体(H2C2O4•3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4•3H2O CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
【问题讨论】用如图所示装置进行实验:

(1)实验前应先检查装置的气密性。
(2)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是_____ (填字母编号)
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(3)B装置的作用是_____ 。
(4)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前将装置中的空气排出,防止发生爆炸
②停止加热后_____ 。
【数据分析与计算】
【资料2】铁的常见氧化物中铁的质量分数
(5)称取铁红样品10.0g用上述装置进行实验,测定铁红中铁的质量分数。
①D中充分反应后得到Fe粉的质量为mg,则m的取值范围是_____ 。
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是_____ 。(计算结果精确到0.1%)
【实验评价】
(6)本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会_____ (填“偏小”、“不变”或“偏大”)。
【资料1】草酸晶体(H2C2O4•3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4•3H2O
【问题讨论】用如图所示装置进行实验:

(1)实验前应先检查装置的气密性。
(2)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(3)B装置的作用是
(4)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前将装置中的空气排出,防止发生爆炸
②停止加热后
【数据分析与计算】
【资料2】铁的常见氧化物中铁的质量分数
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
①D中充分反应后得到Fe粉的质量为mg,则m的取值范围是
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是
【实验评价】
(6)本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会
铜及其化合物有着优良的物理和化学性质,在生产、生活中有广泛的用途。
(1)某同学将铜片加入稀硝酸中,发现开始时反应非常慢,一段时间后反应速率明显加快。
该同学通过实验探究其原因。
①配平该反应的化学方程式::_____ 
_____  =
=_____ 
_____ 
_____ 
②提出合理假设:该实验中反应速率明显加快的原因可能是_____ 。
A 反应放热导致温度升高 B 压强增大
C 生成物的催化作用 D 反应物接触面积增大
③初步探究:测定反应过程中不同时间溶液的温度,结果如表所示:
结合实验目的和表中数据,你得出的结论是_____ 。
(2)0.80 g 样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。
样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。

①试确定105℃时固体物质的化学式为_____ 。
②取270℃所得的样品在570℃灼烧,得到的主要产物是黑色粉末和含+6价元素的非金属氧化物。该反应的化学方程式为_____ 。把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,其存在的最高温度是_____ 。
(1)某同学将铜片加入稀硝酸中,发现开始时反应非常慢,一段时间后反应速率明显加快。
该同学通过实验探究其原因。
①配平该反应的化学方程式::
②提出合理假设:该实验中反应速率明显加快的原因可能是
A 反应放热导致温度升高 B 压强增大
C 生成物的催化作用 D 反应物接触面积增大
③初步探究:测定反应过程中不同时间溶液的温度,结果如表所示:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
(2)0.80 g

①试确定105℃时固体物质的化学式为
②取270℃所得的样品在570℃灼烧,得到的主要产物是黑色粉末和含+6价元素的非金属氧化物。该反应的化学方程式为
除了盐以为,铁在历史上也一直是重要的战略资源。我国钢铁年产量居世界第一,为国民经济的发展必定了坚实的基础。
(一)工业炼铁
工业上以空气、铁矿石、石灰石和______ (写名称)为原料来冶炼生铁,石灰石的作用是______ 。铁矿石冶炼成铁是一个复杂的过程,某炼铁厂用赤铁矿来炼铁,其炼铁的主要原理是______ (用化学方程式表示)。
(二)铁生锈探究
已知某铁锈的成分为Fe2O3·xH2O和FeCO3,某兴趣小组的同学在老师指导下测定其组成。
[提出问题1]铁锈的成分是什么?
根据该铁锈的成分推测,反应物除了铁与空气中的氧气和水蒸气之外,还有______ 参加了反应,猜测的依据是______ 。
[提出问题2]如何确定此铁锈的组成?
[查阅资料]
①Fe2O3·xH2O失去结晶水温度为110℃,FeCO3在282℃分解为FeO和CO2,Fe2O3在300℃时不分解。
②本实验条件下,二氧化碳气体的密度为1.80g/L,装置内空气中的水蒸气和二氧化碳对相关数据测定的影响可忽略不计。
③浓硫酸有吸水性
[设计方案]兴趣小组的同学设计了如图所示的实验装置(夹持仪器省略)进行实验。(B装置中药品足量)
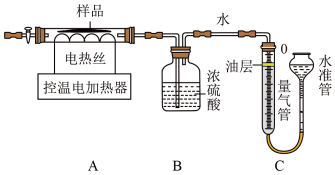
[实验步骤]
①连接仪器并检查装置气密性,往量气管和水准管里加适量的水,上下调整水准管,若看到______ ,说明气密性良好。
②取一定量此铁锈样品,准确称得其质量为5.44g。
③按图所示装入药品,测量并记录相关数据Ⅰ。
④连接A、B、C装置,关闭装置A中活塞,C装置读数后,控制A装置在300℃进行实验。当观察到C装置中有______ 现象时,停止加热,待装置冷却后,再次测量并记录相关数据Ⅱ。
[相关数据]
[问题讨论]
(1)装置B中浓硫酸的作用是______ 。
(2)量气管中水面上放油的目的是______ 。
(3)分析计算测量的数据,FeCO3的质量为______ ,x的值是______ 。
(4)下列数据组合能确定Fe2O3·xH2O中x的是______ (填序号)。
①A、B装置反应前后测得的数据
②A、C装置反应前后测得的数据
③B、C装置反应前后测得的数据
[拓展]请你列举一条生活中防止自行车链条生锈的措施______ 。
(一)工业炼铁
工业上以空气、铁矿石、石灰石和
(二)铁生锈探究
已知某铁锈的成分为Fe2O3·xH2O和FeCO3,某兴趣小组的同学在老师指导下测定其组成。
[提出问题1]铁锈的成分是什么?
根据该铁锈的成分推测,反应物除了铁与空气中的氧气和水蒸气之外,还有
[提出问题2]如何确定此铁锈的组成?
[查阅资料]
①Fe2O3·xH2O失去结晶水温度为110℃,FeCO3在282℃分解为FeO和CO2,Fe2O3在300℃时不分解。
②本实验条件下,二氧化碳气体的密度为1.80g/L,装置内空气中的水蒸气和二氧化碳对相关数据测定的影响可忽略不计。
③浓硫酸有吸水性
[设计方案]兴趣小组的同学设计了如图所示的实验装置(夹持仪器省略)进行实验。(B装置中药品足量)

[实验步骤]
①连接仪器并检查装置气密性,往量气管和水准管里加适量的水,上下调整水准管,若看到
②取一定量此铁锈样品,准确称得其质量为5.44g。
③按图所示装入药品,测量并记录相关数据Ⅰ。
④连接A、B、C装置,关闭装置A中活塞,C装置读数后,控制A装置在300℃进行实验。当观察到C装置中有
[相关数据]
| Ⅰ | Ⅱ | |
| A装置的质量/g | 55.44 | 53.92 |
| B装置的质量/g | 102.00 | 103.08 |
| C装置的读数/mL | 0 | 244.4 |
(1)装置B中浓硫酸的作用是
(2)量气管中水面上放油的目的是
(3)分析计算测量的数据,FeCO3的质量为
(4)下列数据组合能确定Fe2O3·xH2O中x的是
①A、B装置反应前后测得的数据
②A、C装置反应前后测得的数据
③B、C装置反应前后测得的数据
[拓展]请你列举一条生活中防止自行车链条生锈的措施
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


