科学探究题 较难0.4 引用2 组卷180
某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
(1)催化剂的种类与过氧化氢溶液分解速率是否有关呢?甲设计以下对比实验:
Ⅰ.将3.0g 10%H2O2溶液与1.0g MnO2均匀混合;
Ⅱ.将x g 10%H2O2溶液与1.0g CuO均匀混合。
在相同温度下,比较两组实验产生O2的快慢。
Ⅰ中反应的化学方程式是_________________________ ;
Ⅱ中x的值应为_____________ g。
若Ⅰ产生氧气的速率比Ⅱ快,由此得出的实验结论是____________________ 。
(2)乙探究了影响过氧化氢溶液分解速度的某种因素。实验数据记录如下:
本实验中,测量O2体积的装置是____________ (填编号)。
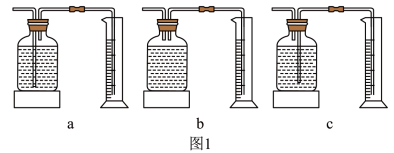
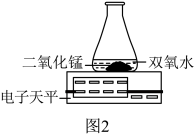
实验结论:在相同条件下,___________________ ,过氧化氢溶液分解得越快。
(3)丙用如图2装置进行实验,通过比较相同时间内_________ 也能达到实验目的。
(1)催化剂的种类与过氧化氢溶液分解速率是否有关呢?甲设计以下对比实验:
Ⅰ.将3.0g 10%H2O2溶液与1.0g MnO2均匀混合;
Ⅱ.将x g 10%H2O2溶液与1.0g CuO均匀混合。
在相同温度下,比较两组实验产生O2的快慢。
Ⅰ中反应的化学方程式是
Ⅱ中x的值应为
若Ⅰ产生氧气的速率比Ⅱ快,由此得出的实验结论是
(2)乙探究了影响过氧化氢溶液分解速度的某种因素。实验数据记录如下:
过氧化氢溶液的质量 | 过氧化氢溶液的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
Ⅰ | 50.0g | 1% | 0.1g | 9mL |
Ⅱ | 50.0g | 2% | 0.1g | 16mL |
Ⅲ | 50.0g | 4% | 0.1g | 31mL |


实验结论:在相同条件下,
(3)丙用如图2装置进行实验,通过比较相同时间内
16-17九年级上·四川资阳·期末
类题推荐
实验探究一:课本第二单元课后作业中有“寻找新的催化剂” 的探究内容,实验中学探究小组据此设计了如下探究方案。
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】
【拓展应用】
已知CuSO4也可作为过氧化氢分解的催化剂。向101.2g一定溶质质量分数的过氧化氢溶液中加入2g CuSO4粉末,充分反应后得到溶质质量分数为2%的溶液,则生成氧气_____ g。
实验探究二:实验室中的试剂一般要密封保存,否则可能会与空气接触而变质。淅河中学化学学习小组发现一瓶未密封的氢氧化钾固体,对其是否变质进行探究。
【提出猜想】1.未变质 2.部分变质 3.完全变质
【查阅资料】KOH与NaOH性质类似,也能与CO2反应而变质。写出KOH变质的化学方程式为_____ 。
【设计实验】
(l)取少量样品于试管中配成溶液,滴加足量稀盐酸有气泡产生,则猜想_____ 不成立。
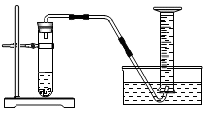
(2)准确称取一定质量的固体样品,放在右图所示装置中进行实验,根据CO2的体积和密度计算变质产物的质量,从而确定变质情况,你认为这个方案是否可行,并说明理由_________ 。
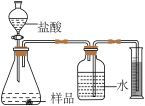
(3)请你另外设计一个方案,进一步探究变质情况
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】
| 实验步骤 | 实验现象 | 实验结论及解释 |
Ⅰ. | A中无明显现象, B中产生大量能使带火星木条复燃的气体 | ① 产生的气体是 ② 红砖粉末能改变过氧化氢分解速率 |
| Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ① 又产生大量能使带火星木条复燃的气体 ② 滤渣质量等于ag | 红砖粉末的 |
Ⅲ.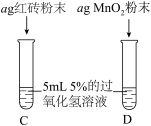 | 两试管中均产生气泡且 | 红砖粉末的催化效果没有二氧化锰粉末好 |
已知CuSO4也可作为过氧化氢分解的催化剂。向101.2g一定溶质质量分数的过氧化氢溶液中加入2g CuSO4粉末,充分反应后得到溶质质量分数为2%的溶液,则生成氧气
实验探究二:实验室中的试剂一般要密封保存,否则可能会与空气接触而变质。淅河中学化学学习小组发现一瓶未密封的氢氧化钾固体,对其是否变质进行探究。
【提出猜想】1.未变质 2.部分变质 3.完全变质
【查阅资料】KOH与NaOH性质类似,也能与CO2反应而变质。写出KOH变质的化学方程式为
【设计实验】
(l)取少量样品于试管中配成溶液,滴加足量稀盐酸有气泡产生,则猜想
(2)准确称取一定质量的固体样品,放在右图所示装置中进行实验,根据CO2的体积和密度计算变质产物的质量,从而确定变质情况,你认为这个方案是否可行,并说明理由

(3)请你另外设计一个方案,进一步探究变质情况
| 实验步骤 | 实验现象 | 实验结论 |
| 猜想2成立 |
兴趣小组同学在老师的带领下,探究影响过氧化氢分解速率的因素。
【提出问题】影响过氧化氢分解的因素有哪些?
【作出假设】猜想1:催化剂的种类 猜想2:过氧化氢溶液的浓度 猜想3:温度
【实验探究】学生利用如图1所示装置,以收集50mL的气体为标准,比较反应的快慢,实验方案如下表所示:
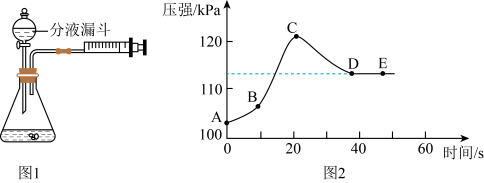
(1)实验中使用分液漏斗目的:_______ 写出实验3发生反应的文字或符号表达式________ 。
(2)对比实验1和2,得出的结论是______ 。
(3)通过对比实验1和3,得出二氧化锰的催化效果比氧化铜强的实验依据是_______ ,通过实验_______ 和________ 对比,证明猜想3成立
(4)实验过程中,学生触摸锥形瓶外壁,有发烫的感觉,说明过氧化氢分解的反应是_______ (填“吸热”或“放热”)反应。在实验3探究中,测出了实验过程中装置压强与时间的关系图(图2),BC段压强急剧上升原因与:________ 和_______ 有关
(5)CD段压强降低的主要原因是:______ 。
【提出问题】影响过氧化氢分解的因素有哪些?
【作出假设】猜想1:催化剂的种类 猜想2:过氧化氢溶液的浓度 猜想3:温度
【实验探究】学生利用如图1所示装置,以收集50mL的气体为标准,比较反应的快慢,实验方案如下表所示:

| 序号 | 温度/℃ | 过氧化氢溶液浓度 | 过氧化氢溶液体积/mL | 1g催化剂 | 时间/s |
| 1 | 20 | 5% | 40 | 二氧化锰 | 37 |
| 2 | 20 | 10% | 40 | 二氧化锰 | 14 |
| 3 | 20 | 5% | 40 | 氧化铜 | b |
| 4 | 80 | 5% | 40 | 二氧化锰 | 29 |
(2)对比实验1和2,得出的结论是
(3)通过对比实验1和3,得出二氧化锰的催化效果比氧化铜强的实验依据是
(4)实验过程中,学生触摸锥形瓶外壁,有发烫的感觉,说明过氧化氢分解的反应是
(5)CD段压强降低的主要原因是:
化学反应速率是衡量化学反应进行快慢的物理量。为了探究影响化学反应速率的因素,以过氧化氢分解为研究对象进行实验。三个小组均采用如图装置进行实验,记录收集10mL氧气的时间。实验室可供选择的试剂有: 、
、 、
、 三种浓度的
三种浓度的 溶液、
溶液、 、CuO、红砖粉末。
、CuO、红砖粉末。
(1) 组:探究催化剂对化学反应速率的影响,取
组:探究催化剂对化学反应速率的影响,取 溶液,三次实验分别加入
溶液,三次实验分别加入 、红砖粉末、CuO进行实验,记录数据如下:
、红砖粉末、CuO进行实验,记录数据如下:
由此得出结论: 、CuO对
、CuO对 分解有催化作用,红砖粉末无催化作用。某同学对该结论提出疑问。
分解有催化作用,红砖粉末无催化作用。某同学对该结论提出疑问。
补充对比实验,操作为__________ 。
结果:长时间 大于
大于 ,收集到很少量气体。
,收集到很少量气体。
(2) 组:探究浓度对化学反应速率的影响
组:探究浓度对化学反应速率的影响
甲同学:取 溶液,加入
溶液,加入 为催化剂,进行实验,记录时间
为催化剂,进行实验,记录时间 。
。
乙同学:取 溶液,加入
溶液,加入 为催化剂,进行实验,记录时间
为催化剂,进行实验,记录时间 。
。
实验结果:
______ 。
结论:浓度越大,反应速率越快。
丙同学:对实验设计提出疑问,并补充实验
_________ 。
记录时间 ,且
,且 。
。
更正结论为:当
_______ 时,反应物浓度越大,反应速率越快。
(3) 组:探究
组:探究______ 对化学反应速率的影响。
取 溶液和
溶液和 为催化剂进行实验,两次实验分别将试管置于冰水浴和
为催化剂进行实验,两次实验分别将试管置于冰水浴和 热水浴记录时间
热水浴记录时间 、
、 ,且
,且 。
。
结论:当反应物浓度和催化剂相同时,_________ 。
(4)综上所述:
 为了研究某一因素对化学反应速率的影响,必须
为了研究某一因素对化学反应速率的影响,必须________ 。
 探究发现影响化学反应速率的因素有:
探究发现影响化学反应速率的因素有:_______ 。

(1)
| 试剂 | 红砖粉末 | CuO | |
| 10 | 60 | 20 |
补充对比实验,操作为
结果:长时间
(2)
甲同学:取
乙同学:取
实验结果:
结论:浓度越大,反应速率越快。
丙同学:对实验设计提出疑问,并补充实验
记录时间
更正结论为:当
(3)
取
结论:当反应物浓度和催化剂相同时,
(4)综上所述:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


