科学探究题 适中0.65 引用5 组卷178
为了探究化学反应前后各物质的总质量是否发生改变,甲、乙、丙三组同学分别进行了下列实验,请根据图示回答问题。
[实验探究]甲、乙、丙三组同学用托盘天平分别称量反应前后物质的质量。
⑴甲组同学的实验现象是红磷燃烧,产生大量_______ ;小气球先膨胀,冷却后变得更瘪;反应后冷却到室温称量,天平的指针_______ (填:“向右”、“向左”或“不”)偏转。在该实验中,玻璃管上系一个小气球的目的是________ 。该反应的化学方程式为_______ 。
⑵乙组同学的实验现象是铁钉表面有红色固体析出,溶液变为________ 色,反应前、后天平保持平衡。该反应的化学方程式为________ 。
⑶丙组同学的实验现象是反应剧烈,产生大量气泡,反应后天平不保持平衡。
[实验结论]化学反应前后各物质的总质量不发生改变。
[实验反思]在探究化学反应前后各物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在________ 装置中进行。
[实验探究]甲、乙、丙三组同学用托盘天平分别称量反应前后物质的质量。
| 甲组 | 乙组 | 丙组 | |
实验装置 | 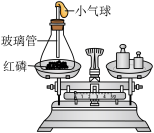 | 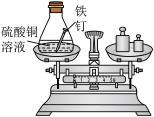 | 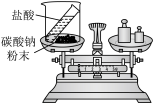 |
⑵乙组同学的实验现象是铁钉表面有红色固体析出,溶液变为
⑶丙组同学的实验现象是反应剧烈,产生大量气泡,反应后天平不保持平衡。
[实验结论]化学反应前后各物质的总质量不发生改变。
[实验反思]在探究化学反应前后各物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在
17-18九年级上·辽宁辽阳·期中
类题推荐
为了探究化学反应前后物质的总质量是否发生改变,甲同学和乙同学分别设计了下面两个实验,请根据图示回答问题:
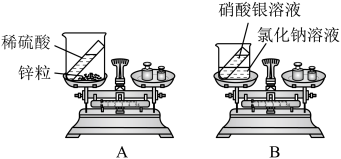
友情提示:A的反应方程式:
B的反应方程式:
(1)甲同学设计的实验如图A所示,反应前,托盘天平的指针指向刻度盘的中间;两种物质反应后,托盘天平的指针___________ (选填“向左”、“向右”或“不”)偏转,原因是___________ 。
(2)乙同学设计的实验如图B所示,通过实验得出结论:化学反应前后物质的总质量________ 。
(3)两位同学通过交流反思得到启示:在探究化学反应前后物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在___________ 装置中进行。
(4)从微观角度分析,在化学反应前后一定不变的是___________ (选填序号)。
①原子种类 ②分子种类 ③原子质量 ④分子质量 ⑤分子数目
(5)质量守恒定律是帮助我们学习和认识化学反应实质的重要理论。下列表述正确的是________。
(6)【拓展应用】将32g纯净物R在足量的O2中完全燃烧,生成88gCO2和72gH2O。则纯净物R的组成中一定含有的元素是___________ 。

友情提示:A的反应方程式:
B的反应方程式:
(1)甲同学设计的实验如图A所示,反应前,托盘天平的指针指向刻度盘的中间;两种物质反应后,托盘天平的指针
(2)乙同学设计的实验如图B所示,通过实验得出结论:化学反应前后物质的总质量
(3)两位同学通过交流反思得到启示:在探究化学反应前后物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在
(4)从微观角度分析,在化学反应前后一定不变的是
①原子种类 ②分子种类 ③原子质量 ④分子质量 ⑤分子数目
(5)质量守恒定律是帮助我们学习和认识化学反应实质的重要理论。下列表述正确的是________。
| A.蜡烛燃烧后质量减少,不遵守质量守恒定律 |
| B.每48gMg和32gO2完全反应后,生成80gMgO |
| C.在化学反应 |
(6)【拓展应用】将32g纯净物R在足量的O2中完全燃烧,生成88gCO2和72gH2O。则纯净物R的组成中一定含有的元素是
Ⅰ.化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如下图1)。观察到镁条在空气中剧烈燃烧,发出耀眼的白光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体。
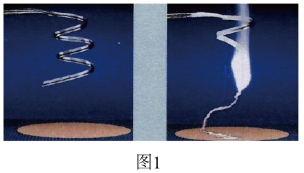
(1)通过称量发现:在石棉网上收集到的产物的质量小于镁条的质量。你认为出现这一实验结果的原因可能是___________ 。
Ⅱ.小红按如图2所示的改进装置验证质量守恒定律,发现白色固体中含有少量黄色固体。
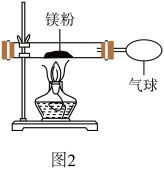
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;
②镁能与氮气剧烈反应生成黄色固体氮化镁(Mg3N2);
③氮化镁可与水剧烈反应产生氨气(NH3),氨气具有刺激性气味,能使湿润的红色石蕊试纸变蓝。
【作出猜想】黄色固体是Mg3N2。
【实验探究】
(2)请设计实验,验证猜想。
【反思与交流】
(3)空气中氮气(N2)和氧气(O2)的体积比约为___________ ,可是镁条在空气中的燃烧产物MgO却远多于Mg3N2,合理的解释是___________ 。

(1)通过称量发现:在石棉网上收集到的产物的质量小于镁条的质量。你认为出现这一实验结果的原因可能是
Ⅱ.小红按如图2所示的改进装置验证质量守恒定律,发现白色固体中含有少量黄色固体。

【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;
②镁能与氮气剧烈反应生成黄色固体氮化镁(Mg3N2);
③氮化镁可与水剧烈反应产生氨气(NH3),氨气具有刺激性气味,能使湿润的红色石蕊试纸变蓝。
【作出猜想】黄色固体是Mg3N2。
【实验探究】
(2)请设计实验,验证猜想。
| 实验操作 | 实验现象 | 实验结论 |
| a.取少量产物中的黄色固体于试管中,并往其中加入适量的 b.在试管口放置一片湿润的红色石蕊试纸 | ①生成具有刺激性气味的气体; ②试纸由红色变成 | 猜想正确 |
【反思与交流】
(3)空气中氮气(N2)和氧气(O2)的体积比约为
为验证质量守恒定律,某学习小组做了镁条在空气中燃烧的实验(图1)
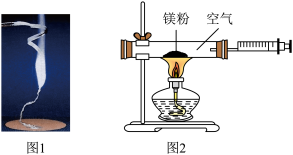
(1)请写出镁条燃烧的化学方程式_____ .
(2)镁条完全燃烧后,称量发现石棉网上的燃烧产物的质量反而比反应前镁条的质量小,其主导原因可能有_____ .
A 燃烧增加了氧元素的质量 B 有部分白烟逸散在空气中 C 部分产物粘在坩埚钳上
故探究化学反应前后物质的总质量关系时,如反应过程中有气体参加或生成,需要在____ 容器中进行。
(3)小红按图2装置改进实验,验证了质量守恒定律,最终得出结论是:参加化学反应的各物质的质量总和_____ (填"<”、“>"或"=")反应后生成的各物质的质量总和。(微观解释)从微观角度分析,在化学反应前后一定不变的是____ (选填序号)。
①原子种类 ②分子种类 ③原子数目 ④分子质量 ⑤分子数目 ⑥原子质量
(4)小红结束图2实验后发现产物中还有一些黄色固体。
【查阅资料】①氧化镁为白色固体;②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应生成氨气,氨气能使酚酞溶液变红。
【提出问题】黄色固体是什么呢?
【做出猜想】黄色固体为Mg3N2
【实验探究】
【反思与交流】
①空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,请给出合理的解释_____ 。
②如果用图2装置(气密性良好)和药品(足量)测定空气中氧气含量,结合注射器的刻度显示,最终测得氧气体积分数___ 1/5(填“大于”、“小于或“等于”)。注射器在本实验中还具备的优点为:____ 。

(1)请写出镁条燃烧的化学方程式
(2)镁条完全燃烧后,称量发现石棉网上的燃烧产物的质量反而比反应前镁条的质量小,其主导原因可能有
A 燃烧增加了氧元素的质量 B 有部分白烟逸散在空气中 C 部分产物粘在坩埚钳上
故探究化学反应前后物质的总质量关系时,如反应过程中有气体参加或生成,需要在
(3)小红按图2装置改进实验,验证了质量守恒定律,最终得出结论是:参加化学反应的各物质的质量总和
①原子种类 ②分子种类 ③原子数目 ④分子质量 ⑤分子数目 ⑥原子质量
(4)小红结束图2实验后发现产物中还有一些黄色固体。
【查阅资料】①氧化镁为白色固体;②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应生成氨气,氨气能使酚酞溶液变红。
【提出问题】黄色固体是什么呢?
【做出猜想】黄色固体为Mg3N2
【实验探究】
| 实验操作 | 实验现象及结论 |
如图,取燃烧产物于烧杯B中,加入适量水,然后用大烧杯罩住小烧杯A和B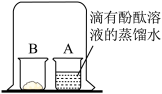 | 现象: 结论:燃烧产物中含Mg3N2 |
①空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,请给出合理的解释
②如果用图2装置(气密性良好)和药品(足量)测定空气中氧气含量,结合注射器的刻度显示,最终测得氧气体积分数
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


