填空与简答-推断题 较难0.4 引用1 组卷240
有一包粉末,已知其由BaCO3、Cu(NO3)2、Na2SO4、NaCl、NaOH中的几种组成,现对其做以下实验,各步骤均已经充分反应,请回答问题:
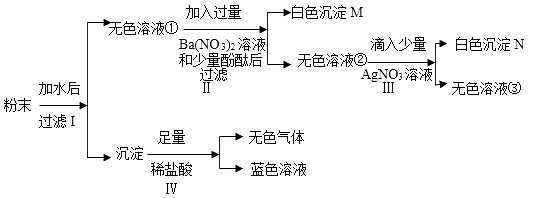
(1)请写出沉淀N的化学式:___________ 。
(2)步骤Ⅱ所发生反应的化学方程式为_________ ,其基本反应类型为____ 。
(3)无色溶液②中一定存在的溶质(酚酞除外)的化学式为___________ 。
(4)这包粉末中共含有___________ 种物质。

(1)请写出沉淀N的化学式:
(2)步骤Ⅱ所发生反应的化学方程式为
(3)无色溶液②中一定存在的溶质(酚酞除外)的化学式为
(4)这包粉末中共含有
2017·辽宁锦州·三模
类题推荐
人类历史发展的不同阶段曾以不同金属材料的使用作为标志,当今社会铁已是年产量最高的金属,铁的合金及其铁的化合物在生产生活中有着广泛的应用。
(1)人类最早使用的金属主要是金、银,金、银在自然界有单质形式存在,说明他们的化学性质都______ 。
(2)铝的利用要比铜和铁晚的多,铝具有密度小和抗腐蚀等优良性能,现在铝的年产量已超过铜,居第二位,铝具有优良抗腐蚀性能的原因______ 。
(3)钛和钛合金是21世纪的重要的金属材料。钛合金制品放在海水中数年,取出后仍光亮如新,是因为其______(填字母序号)非常好。
(4)铁在潮湿的空气中反应生成疏松的铁锈。已知:2FeCl3+Fe=3FeC12
铁锈的主要成分是______ (填化学式),将生锈的铁制品放入一定量的稀盐酸中充分反应,首先观察到溶液由无色变为黄色,该过程发生反应的化学方程式为______ , 整个变化过程中最多涉及______ 种化学反应基本类型。
(5)四氧化三铁可用于医疗器械、电子等工业、某实验兴趣小组从工厂采集废液(含FeSO4和少量ZnSO4、MgSO4),进行四氧化三铁的制备实验。
【阅读资料】①25℃时,氢氧化物沉淀的pH范围如表。
②25℃时,Zn(OH)₂可溶于pH > 10.5的碱溶液。
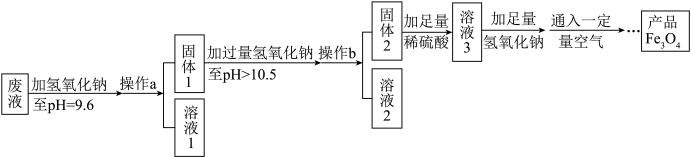
制备Fe3O4的实验流程如图:
【回答问题】
①往废液中加入氢氧化钠溶液后,溶液pH可容许的范围为______ 。
②溶液1中一定含有溶质是______ 。
③该实验取废液100g,最终得到产品四氧化三铁质量为4.64g,则原废液中硫酸亚铁溶质的质量分数不低于______ (精确到0.01%)。
(1)人类最早使用的金属主要是金、银,金、银在自然界有单质形式存在,说明他们的化学性质都
(2)铝的利用要比铜和铁晚的多,铝具有密度小和抗腐蚀等优良性能,现在铝的年产量已超过铜,居第二位,铝具有优良抗腐蚀性能的原因
(3)钛和钛合金是21世纪的重要的金属材料。钛合金制品放在海水中数年,取出后仍光亮如新,是因为其______(填字母序号)非常好。
| A.可塑性 | B.机械性能 | C.抗腐蚀性能 |
铁锈的主要成分是
(5)四氧化三铁可用于医疗器械、电子等工业、某实验兴趣小组从工厂采集废液(含FeSO4和少量ZnSO4、MgSO4),进行四氧化三铁的制备实验。
【阅读资料】①25℃时,氢氧化物沉淀的pH范围如表。
Zn(OH)₂ | Fe(OH)2 | Mg(OH)2 | |
开始沉淀的pH | 5.7 | 7.6 | 10.4 |
沉淀完全的pH | 8.0 | 9.6 | 12.4 |
制备Fe3O4的实验流程如图:

【回答问题】
①往废液中加入氢氧化钠溶液后,溶液pH可容许的范围为
②溶液1中一定含有溶质是
③该实验取废液100g,最终得到产品四氧化三铁质量为4.64g,则原废液中硫酸亚铁溶质的质量分数不低于
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网