填空与简答-推断题 困难0.15 引用1 组卷644
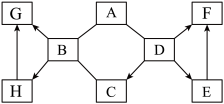
如图是中学常见物质的转换关系图,其中A、B常温下都为无色液体,且组成元素相同.A、B、X、Y、E都为氧化物,X、E都为黑色固体,Y可用作干燥剂,F是大理石的主要成分,I为蓝色沉淀,L为不溶于稀硝酸的白色沉淀.请回答:

(1)X在反应①中起_________ 作用。
(2)写出反应④的化学方程式________ 。
(3)写出L的化学式________ 。
(4)写出G在空气中变质发生反应的化学方程式__________ 。

(1)X在反应①中起
(2)写出反应④的化学方程式
(3)写出L的化学式
(4)写出G在空气中变质发生反应的化学方程式
16-17九年级下·江苏镇江·阶段练习
类题推荐
硼酸( )能溶于水,可用于玻璃、医药、纺织等工业。碳酸镁可用于制造防火涂料、牙膏等。某工厂以硼镁铁矿(主要成分为
)能溶于水,可用于玻璃、医药、纺织等工业。碳酸镁可用于制造防火涂料、牙膏等。某工厂以硼镁铁矿(主要成分为 ,杂质有
,杂质有 、FeO、
、FeO、 、
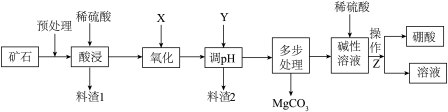
、 )为原料制备硼酸、碳酸镁的工艺流程如下图所示:
)为原料制备硼酸、碳酸镁的工艺流程如下图所示:
已知:①常温时实验条件下几种金属离子形成沉淀的pH如下表;
②SiO2不溶于水,也不与酸反应;
③硼酸各温度下的的溶解度如下表。
硼酸的溶解度
(1)预处理的内容包括矿石的筛选、_______ ,写出料渣1的化学式_______ 。
(2)酸浸时 与硫酸反应生成硫酸镁和硼酸,写出化学方程式
与硫酸反应生成硫酸镁和硼酸,写出化学方程式_______ ;氧化过程的化学方程式为: 。X化学式是
。X化学式是_______ ,X作氧化剂的优点_______ 。
(3)为提高产品纯度,控制的pH范围是_______ ;试剂Y为_______ (填选项)。
A.MgO B.Fe2O3 C.Fe(OH)3 D.Mg(OH)2
(4)为测量所得硼酸纯度,取3.00g制取的硼酸样品溶于甘露醇与蒸馏水混合溶液中配成500mL溶液,取出25.00mL放入锥形瓶并滴加3滴酚酞试液,用0.004g/mLNaOH标准溶液进行中和滴定,滴定终点时消耗22.00mL标准溶液。则滴定终点时的现象是_______ ,样品中硼酸的纯度是____ ?(请写出计算过程,小数点后保留一位有效数字,中和反应的化学方程式为 )。
)。
(5)操作Z包括:_______ 、_______ 、过滤、洗涤、干燥。
(6)此工艺流程中提高硼酸产率措施有:_______ 、_______ ……

已知:①常温时实验条件下几种金属离子形成沉淀的pH如下表;
②SiO2不溶于水,也不与酸反应;
③硼酸各温度下的的溶解度如下表。
硼酸的溶解度
| 温度/℃ | 溶解度,q/100g | 温度,°C | 溶解度,g/100g |
| 0 | 2.77 | 40 | 8.90 |
| 10 | 3.65 | 50 | 11.39 |
| 20 | 4.87 | 60 | 14.89 |
| 25 | 5.74 | 80 | 23.54 |
| 30 | 6.77 | 100 | 38.00 |
| 开始沉淀 | 完全沉淀 | |
| Fe3+ | 2.7 | 3.2 |
| Fe2+ | 7.6 | 9.6 |
| Al3+ | 4.0 | 5.2 |
| Mg2+ | 9.6 | 11.1 |
(2)酸浸时
(3)为提高产品纯度,控制的pH范围是
A.MgO B.Fe2O3 C.Fe(OH)3 D.Mg(OH)2
(4)为测量所得硼酸纯度,取3.00g制取的硼酸样品溶于甘露醇与蒸馏水混合溶液中配成500mL溶液,取出25.00mL放入锥形瓶并滴加3滴酚酞试液,用0.004g/mLNaOH标准溶液进行中和滴定,滴定终点时消耗22.00mL标准溶液。则滴定终点时的现象是
(5)操作Z包括:
(6)此工艺流程中提高硼酸产率措施有:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网