科学探究题 适中0.65 引用2 组卷336
如图是木炭还原氧化铜的探究实验装置。
【提出问题】木炭还原氧化铜产生什么气体?
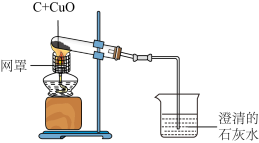
【提出猜想】产生的气体有三种情况:①CO;②CO2;③______ ;
【设计方案】实验前后分别对试管和烧杯里的物质进行称量,数据设计如下:
(1)若△m2=0,说明反应产生的气体不能被澄清石灰水吸收,则猜想______ 成立;
(2)若猜想②正确,理论上△m1与△m2的关系是:△m1_____ △m2(填“>”、“<”或“=”);
【实验并记录】实验得到的数据如下表:
用以上实验数据分析,结果应该是猜想_____ 成立;
同学们对CO产生的原因进行了分析:
①原因一:木炭和氧化铜在高温条件下直接发生反出产生CO;反应方程式为____
②原因二:木炭和氧化铜在高温条件下反应中的一种产物和反应物木炭又发生了化学反应,产生了CO;反应方程式为_______
【反思与评价】经查阅资料知道:木炭还原氧化铜产生CO2气体,反应化学方程式为:____ ;
本次实验结果与资料显示不一致.对其可能原因有同学提出下列分析,其中合理的是_______ ;
A 装置漏气
B 生成的CO2部分与过量的C反应生成了CO
C 澄清石灰水吸收CO2效果不好
D 装置内还有CO2气体未被吸收
【定量分析】6克碳与一定质量的氧化铜恰好完全反应,生成的气体完全被足量的石灰水吸收,可得到沉淀____ 克?
【提出问题】木炭还原氧化铜产生什么气体?

【提出猜想】产生的气体有三种情况:①CO;②CO2;③
| 称量对象 | 反应前质量 | 反应后质量 | 质量差 |
| 试管+固体混合物 | M1 | M2 | ∆m1即(M1-M2) |
| 烧杯+澄清石灰水 | M3 | M4 | ∆m2即(M4-M3) |
(1)若△m2=0,说明反应产生的气体不能被澄清石灰水吸收,则猜想
(2)若猜想②正确,理论上△m1与△m2的关系是:△m1
| 称量对象 | 反应前质量 | 反应后质量 | 质量差 |
| 试管+固体混合物 | 69.8g | 65.4g | ∆m1 |
| 烧杯+澄清石灰水 | 118.9g | 122.6g | ∆m2 |
用以上实验数据分析,结果应该是猜想
同学们对CO产生的原因进行了分析:
①原因一:木炭和氧化铜在高温条件下直接发生反出产生CO;反应方程式为
②原因二:木炭和氧化铜在高温条件下反应中的一种产物和反应物木炭又发生了化学反应,产生了CO;反应方程式为
【反思与评价】经查阅资料知道:木炭还原氧化铜产生CO2气体,反应化学方程式为:
本次实验结果与资料显示不一致.对其可能原因有同学提出下列分析,其中合理的是
A 装置漏气
B 生成的CO2部分与过量的C反应生成了CO
C 澄清石灰水吸收CO2效果不好
D 装置内还有CO2气体未被吸收
【定量分析】6克碳与一定质量的氧化铜恰好完全反应,生成的气体完全被足量的石灰水吸收,可得到沉淀
16-17九年级上·江苏无锡·阶段练习
类题推荐
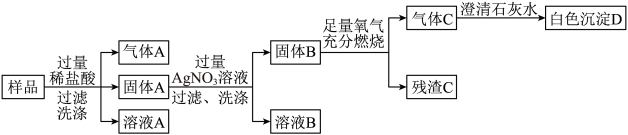
化学兴趣小组的同学们用盐酸和大理石制备CO2,产生了大量废液。兴趣小组的同学们通过研究确定了废液处理方案:
(1)废液成分:
①推测废液所含溶质。
猜想1:___________ ;猜想2:CaCl2和HCl
(2)若用一种药品验证哪种猜想成立,可选择的试剂是_______(填标号)。
废液处理:实验表明猜想2正确,小组同学决定用Na2CO3除去它们。
【提出问题】如何估算Na2CO3固体的用量?
【进行实验】取100mL废液样品于烧杯中,逐滴滴加5. 3%的Na2CO3溶液,用pH传感器测定滴加过程中溶液的pH。实验结果如图所示。
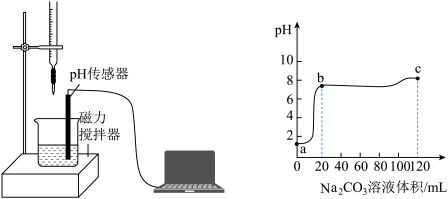
【结果讨论】
(3)①a-b阶段,观察到烧杯中的现象是___________ 。
②b点后曲线处于平缓阶段,当加入40mL碳酸钠溶液时,溶液中含有的阳离子有__________ 。(填离子符号)
③c点时,取少量烧杯中的清液于试管中,滴加CaCl2溶液,有白色沉淀生成。说明处理100mL废液,所需5.3%的Na2CO3溶液的体积______ 120mL。(填“大于”“等于”或“小于”)
④将烧杯中的沉淀过滤、洗涤、干燥、称重,质量为4g,若处理1L该废液,理论上需要Na2CO3固体_______ g。(实验所用Na2CO3溶液的密度近似看作1g/cm3)
(1)废液成分:
①推测废液所含溶质。
猜想1:
(2)若用一种药品验证哪种猜想成立,可选择的试剂是_______(填标号)。
| A.石蕊溶液 | B.AgNO3溶液 | C.锌粒 | D.CuO粉末 | E.NaOH溶液 |
废液处理:实验表明猜想2正确,小组同学决定用Na2CO3除去它们。
【提出问题】如何估算Na2CO3固体的用量?
【进行实验】取100mL废液样品于烧杯中,逐滴滴加5. 3%的Na2CO3溶液,用pH传感器测定滴加过程中溶液的pH。实验结果如图所示。

【结果讨论】
(3)①a-b阶段,观察到烧杯中的现象是
②b点后曲线处于平缓阶段,当加入40mL碳酸钠溶液时,溶液中含有的阳离子有
③c点时,取少量烧杯中的清液于试管中,滴加CaCl2溶液,有白色沉淀生成。说明处理100mL废液,所需5.3%的Na2CO3溶液的体积
④将烧杯中的沉淀过滤、洗涤、干燥、称重,质量为4g,若处理1L该废液,理论上需要Na2CO3固体
我国劳动人民早在五千年前就会使用木炭炼铜,在化学实验室里模拟炼铜,既可用传统的实验装置(见图甲),又能用改进的微型实验装置(见图乙),化学兴趣小组采用图乙装置,开展以下探究活动:
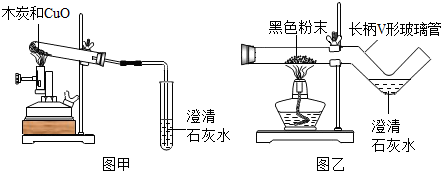
【提出问题】木炭与CuO反应所得红色固体中含有什么物质?
【查阅资料】
(1)①木炭与CuO反应的化学方程式是:_____ ,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O)。
②Cu2O是红色固体,能与稀硫酸反应:Cu2O+H2SO4=Cu+CuSO4+H2O。
【作出猜想】
(2)红色固体的成分:①全部是Cu;②全部是_____ ;③是Cu和Cu2O的混合物。
【实验探究】
(3)①取木炭、CuO两种黑色粉末适量,再加少许CaCl2(能降低反应温度,加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内。
②按图乙连好实验装置,然后加热反应物;2分钟后,黑色粉末变红,同时澄清的石灰水变浑浊,(写出石灰水变浑浊的化学方程式_____ )此时停止加热。
③待玻璃管冷却后,提取里面的红色固体,进行如下的验证:
【评价反思】
(4)用图乙装置与使用图甲装置相比,其优点是_____ (写出1条即可)。

【提出问题】木炭与CuO反应所得红色固体中含有什么物质?
【查阅资料】
(1)①木炭与CuO反应的化学方程式是:
②Cu2O是红色固体,能与稀硫酸反应:Cu2O+H2SO4=Cu+CuSO4+H2O。
【作出猜想】
(2)红色固体的成分:①全部是Cu;②全部是
【实验探究】
(3)①取木炭、CuO两种黑色粉末适量,再加少许CaCl2(能降低反应温度,加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内。
②按图乙连好实验装置,然后加热反应物;2分钟后,黑色粉末变红,同时澄清的石灰水变浑浊,(写出石灰水变浑浊的化学方程式
③待玻璃管冷却后,提取里面的红色固体,进行如下的验证:
| 步骤 | 现象 | 结论 |
| ①取1.44g红色固体装入试管,滴入足量的稀硫酸,充分反应 | 红色固体部分减少,溶液变为 | 猜想 |
| ②滤出试管中残留的红色固体,洗涤干燥,称其质量为1.04g | / | 猜想 |
【评价反思】
(4)用图乙装置与使用图甲装置相比,其优点是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网