科学探究题 较难0.4 引用3 组卷241
实验室常用过氧化氢溶液和二氧化锰(催化剂)制取氧气.
【提出问题】催化剂二氧化锰的用量对反应速率是否有影响?
【设计实验】
实验装置如图所示:
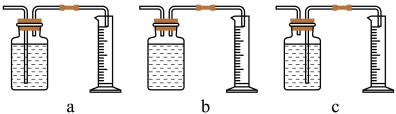
实验记录:实验数据如下表:
【实验分析】
(1)过氧化氢分解的文字表达式为_____ ;二氧化锰可作为该反应的催化剂的依据是_____ .
(2)表格中的“测量数据”是:相同时间内_____

(3)本实验中,测定待测数据的装置(图中虚线框里)是_____ (填编号).
(4)若第Ⅱ次比第Ⅲ次实验的“测量数据”更_____ (填“大”或“小”)说明催化剂的用量越多,反应更快.
【实验反思】除了上述因素会影响过氧化氢的反应速率外,_____ (写一种)也会影响过氧化氢的分解反应速率,请写出你的实验方案:_____ .
【提出问题】催化剂二氧化锰的用量对反应速率是否有影响?
【设计实验】
实验装置如图所示:

实验记录:实验数据如下表:
过氧化氢体积(mL) | 过氧化氢浓度 | 二氧化锰质量(g) | 测量数据(mL) | |
Ⅰ | 30 | 5% | 0.1 | |
Ⅱ | 30 | 5% | 0.2 | |
Ⅲ | 30 | 5% | 0.3 |
(1)过氧化氢分解的文字表达式为
(2)表格中的“测量数据”是:相同时间内

(3)本实验中,测定待测数据的装置(图中虚线框里)是
(4)若第Ⅱ次比第Ⅲ次实验的“测量数据”更
【实验反思】除了上述因素会影响过氧化氢的反应速率外,
16-17九年级上·安徽亳州·阶段练习
类题推荐
化学实验小组的同学们对催化剂产生了兴趣,通过查阅资料了解到氧化铁也能加速氯酸钾的分解。为了探究氧化铁能否加快过氧化氢的分解,他们设计了实验装置,并进行气体的制备和测量实验。实验时均以生成40mL气体为标准,相关实验数据记录如下表:
(1)完成上述实验及数据的测定需要用到如图中的部分装置,请按组装顺序写出所用到的装置代号___________ 。

(2)通过实验①和④对比可知,化学反应速率与温度的关系是______________________ ;通过实验②和③对比可知,化学反应速率与___________ 有关;通过实验___________ 和___________ 对比可知,氧化铁可以加快过氧化氢分解放氧的速率。
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总量__ (选填“减小”“不变”或“增大”)。
(4)若要证明氧化铁是过氧化氢分解的催化剂,还需要验证它在该反应前后的___________ 和___________ 未发生改变。
(5)同学们还想探究催化剂的___________ ,对化学反应速率是有影响的,请你帮他们设计实验方案进行研究:______________________ 。
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液体积/mL | 过氧化氢溶液温度/℃ | 氧化铁的用量/g | 收集40mL氧气所需时间/s |
| ① | 5 | 10 | 20 | 0 | 128.5 |
| ② | 5 | 10 | 20 | 1.2 | 16.8 |
| ③ | 15 | 10 | 20 | 1.2 | 10.5 |
| ④ | 5 | 10 | 70 | 0 | 32.7 |
(1)完成上述实验及数据的测定需要用到如图中的部分装置,请按组装顺序写出所用到的装置代号

(2)通过实验①和④对比可知,化学反应速率与温度的关系是
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总量
(4)若要证明氧化铁是过氧化氢分解的催化剂,还需要验证它在该反应前后的
(5)同学们还想探究催化剂的
研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的过程:
【假设】H2O2生成O2的快慢与催化剂种类有关。
【实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间。
【进行实验】下图是他们进行实验的装置图,气体发生装置中A仪器的名称是________ ,此实验中B处宜采用的气体收集方法是 _______________ 。
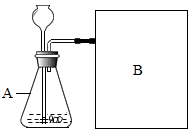
【实验记录】
[实验结论]
【结论】该探究过程得出的结论是___________ 。
【反思】H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快。若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的________ 和 _________ 是否改变。
【实验拓展】H2O2生成O2的快慢还与哪些因素有关?研究性学习小组进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
请你设计:
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
【假设】H2O2生成O2的快慢与催化剂种类有关。
【实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间。
【进行实验】下图是他们进行实验的装置图,气体发生装置中A仪器的名称是

【实验记录】
实验编号 | 1 | 2 |
反应物 | 5%H2O2 | 5%H2O2 |
催化剂 | 1g水泥块 | 1gMnO2 |
时间 | 165s | 46s |
【结论】该探究过程得出的结论是
【反思】H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快。若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的
【实验拓展】H2O2生成O2的快慢还与哪些因素有关?研究性学习小组进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
| 实验步骤 | 现 象 | 结 论 |
| 取一支试管加入3~5mL5%的过氧化氢溶液,然后加入少量二氧化锰。 | 缓慢有少量气泡冒出 | |
| 另取一支试管加入3~5mL15%的过氧化氢溶液,然后加入少量二氧化锰。 | 迅速有大量气泡冒出 |
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
| 实验步骤 | 现 象 | 结 论 |
| 其它条件相同时,温度越高,过氧化氢分解的速率越大 | ||
兴趣小组同学在老师的带领下,探究影响过氧化氢分解速率的因素。
【提出问题】影响过氧化氢分解的因素有哪些?
【作出假设】猜想1:催化剂的种类 猜想2:过氧化氢溶液的浓度 猜想3:温度
【实验探究】学生利用如图1所示装置,以收集50mL的气体为标准,比较反应的快慢,实验方案如下表所示:
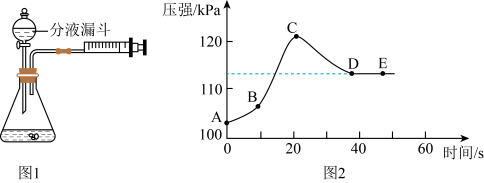
(1)实验中使用分液漏斗目的:_______ 写出实验3发生反应的文字或符号表达式________ 。
(2)对比实验1和2,得出的结论是______ 。
(3)通过对比实验1和3,得出二氧化锰的催化效果比氧化铜强的实验依据是_______ ,通过实验_______ 和________ 对比,证明猜想3成立
(4)实验过程中,学生触摸锥形瓶外壁,有发烫的感觉,说明过氧化氢分解的反应是_______ (填“吸热”或“放热”)反应。在实验3探究中,测出了实验过程中装置压强与时间的关系图(图2),BC段压强急剧上升原因与:________ 和_______ 有关
(5)CD段压强降低的主要原因是:______ 。
【提出问题】影响过氧化氢分解的因素有哪些?
【作出假设】猜想1:催化剂的种类 猜想2:过氧化氢溶液的浓度 猜想3:温度
【实验探究】学生利用如图1所示装置,以收集50mL的气体为标准,比较反应的快慢,实验方案如下表所示:

| 序号 | 温度/℃ | 过氧化氢溶液浓度 | 过氧化氢溶液体积/mL | 1g催化剂 | 时间/s |
| 1 | 20 | 5% | 40 | 二氧化锰 | 37 |
| 2 | 20 | 10% | 40 | 二氧化锰 | 14 |
| 3 | 20 | 5% | 40 | 氧化铜 | b |
| 4 | 80 | 5% | 40 | 二氧化锰 | 29 |
(2)对比实验1和2,得出的结论是
(3)通过对比实验1和3,得出二氧化锰的催化效果比氧化铜强的实验依据是
(4)实验过程中,学生触摸锥形瓶外壁,有发烫的感觉,说明过氧化氢分解的反应是
(5)CD段压强降低的主要原因是:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


