科学探究题 较难0.4 引用3 组卷378
某化学兴趣小组发现铜片在加热的条件下可以与浓硫酸反应,产生气泡并闻到刺激性气味,铜片溶解,溶液呈蓝色,请你参与实验探究。
【查阅资料】SO2是一种无色,有刺激性气味,有毒的气体。
【提出问题】产生的气体是什么?
【提出猜想】猜想一:SO2;猜想二:SO2和H2。
你认为猜想二___________________ (填:“正确”或“错误”)。
【提出问题】蓝色溶液的溶质是什么?
【提出猜想】猜想一:CuSO4;猜想二:CuSO4和H2SO4。
【进行实验】取一定量反应后的溶液进行稀释,并分装在A、B两支试管中,然后进行下列实验,并完成如表:
【探究结论】通过实验,猜想二正确。
写出步骤一发生反应的化学方程式:_____________ 。
完成并配平方程式:_____ Cu+_____ H2SO4(浓)_____________ 。
【反思评价】根据化学方程式:小王认为工业上可以用铜和浓硫酸反应大量制取硫酸铜,小李认为不适宜,理由是_____________ 。
【查阅资料】SO2是一种无色,有刺激性气味,有毒的气体。
【提出问题】产生的气体是什么?
【提出猜想】猜想一:SO2;猜想二:SO2和H2。
你认为猜想二
【提出问题】蓝色溶液的溶质是什么?
【提出猜想】猜想一:CuSO4;猜想二:CuSO4和H2SO4。
【进行实验】取一定量反应后的溶液进行稀释,并分装在A、B两支试管中,然后进行下列实验,并完成如表:
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| 步骤一 | 在试管A中加入少量的CuO粉末 | ① | 溶液中含有H2SO4 |
| 步骤二 | 在试管B中加入过量的NaOH溶液 | ② | 溶液中含有CuSO4 |
写出步骤一发生反应的化学方程式:
完成并配平方程式:
【反思评价】根据化学方程式:小王认为工业上可以用铜和浓硫酸反应大量制取硫酸铜,小李认为不适宜,理由是
2016·广西贺州·中考真题
类题推荐
某实验小组同学们利用老师提供的试剂:锌片、铜片、银片、硫酸锌溶液、硫酸铜溶液、硝酸银溶液和稀硫酸,探究锌、铜、银三种金属活动性顺序。请你参与他们的实验探究。
【实验目的】探究锌、铜、银三种金属活动性顺序。
【设计实验方案】经过讨论,他们设计出了以下几种实验方案。
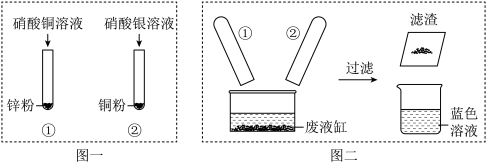
方案I:铜片、硫酸锌溶液、硝酸银溶液;
方案Ⅱ:锌片、铜片、稀硫酸、硝酸银溶液;
方案Ⅲ:锌片、铜片、硫酸铜溶液、硝酸银溶液;
方案Ⅳ:___________ 。
【进行实验】小鸿同学选用方案Ⅲ进行如下探究,请你帮他完成表格中横线上的空白处:
【实验结论】根据上述实验,小鸿得出三种金属活动性顺序是Zn>Cu>Ag
【反思与评价】探究活动结束后,同学们对实验进行分析与反思:
(1)有同学提出小鸿的实验中不用硫酸铜溶液也能得到相同的实验结论。简要说明其验证方法:___________ 。
(2)经过讨论,大家一致认为以上实验方案中,方案___________ 较好。
(3)小沛提出,试管中的金属可以回收再利用,这样做的意义是___________ 。
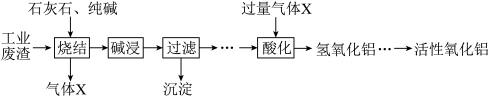
【拓展与延伸】在征老师同意后,小沛把一定量的锌粒加入硫酸铜和硝酸银的混合溶液中,充分反应一段时间后,过滤,发现滤液呈蓝色。此时,滤渣中可能含有___________ ,滤液中一定含有的阳离子是___________ 。
【实验目的】探究锌、铜、银三种金属活动性顺序。
【设计实验方案】经过讨论,他们设计出了以下几种实验方案。
方案I:铜片、硫酸锌溶液、硝酸银溶液;
方案Ⅱ:锌片、铜片、稀硫酸、硝酸银溶液;
方案Ⅲ:锌片、铜片、硫酸铜溶液、硝酸银溶液;
方案Ⅳ:
【进行实验】小鸿同学选用方案Ⅲ进行如下探究,请你帮他完成表格中横线上的空白处:
| 实验操作 | 实验现象 | 分析与结论 |
①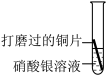 | 有银白色固体析出,溶液由无色逐渐变为蓝色 | 金属活动性:Cu>Ag |
②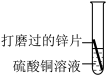 | 有红色固体析出,溶液由蓝色逐渐变为无色 | 金属活动性:Zn>Cu,反应的化学方程式为 |
【反思与评价】探究活动结束后,同学们对实验进行分析与反思:
(1)有同学提出小鸿的实验中不用硫酸铜溶液也能得到相同的实验结论。简要说明其验证方法:
(2)经过讨论,大家一致认为以上实验方案中,方案
(3)小沛提出,试管中的金属可以回收再利用,这样做的意义是
【拓展与延伸】在征老师同意后,小沛把一定量的锌粒加入硫酸铜和硝酸银的混合溶液中,充分反应一段时间后,过滤,发现滤液呈蓝色。此时,滤渣中可能含有
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网