填空与简答-填空题 较难0.4 引用5 组卷495
有一包白色的粉末,是(NH4)2SO4、NaCl、BaCl2、Na2CO3、Na2SO4中的一种或几种,为确定白色粉末的成份,进行如下探究:
(1)取适量白色粉末与熟石灰混匀、共热,没有任何异味产生,说明原白色粉末一定不存在_____ ,其理由是_____________________________ ;
(2)另取适量白色粉末加入足量的水,搅拌,得到白色沉淀和无色溶液,可推测原白色粉末中一定含有______________ ;
(3)取(2)中的白色沉淀,往其中加入过量的稀盐酸,产生大量的气泡,白色沉淀全部消失,说明原白色粉末中一定还含有__________ ,一定不含有_________ ,写出产生白色沉淀的化学方程式_________________________________ ;
(4)取(2)中的无色溶液蒸干,得固体物质,此固体物质的成份可能有______ 种组成情况。
(1)取适量白色粉末与熟石灰混匀、共热,没有任何异味产生,说明原白色粉末一定不存在
(2)另取适量白色粉末加入足量的水,搅拌,得到白色沉淀和无色溶液,可推测原白色粉末中一定含有
(3)取(2)中的白色沉淀,往其中加入过量的稀盐酸,产生大量的气泡,白色沉淀全部消失,说明原白色粉末中一定还含有
(4)取(2)中的无色溶液蒸干,得固体物质,此固体物质的成份可能有
2016·湖南郴州·中考真题
类题推荐
稀土金属是我国战略性资源,应加以保护。稀土金属钇(Y)是很活泼的金属,常见化合价为+3价,它是激光和超导的重要材料。
以钇矿石(Y2FeBe2Si2O10) 为原料生产氧化钇(Y2O3) 的主要流程如下:
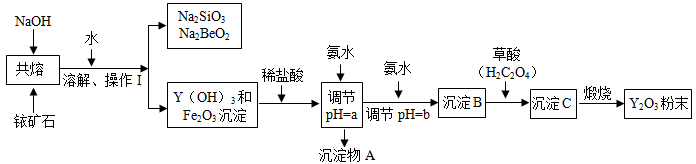
资料卡:有关金属离子形成氢氧化物沉淀时的pH如下表:
(1)钇矿石与NaOH共熔前粉碎的目的是_____________________ 。
(2)操作Ⅰ是_________ ,需要的玻璃仪器有____________________ 。
(3)加盐酸时,发生中和反应的化学方程式为:____________________ 。
(4)调节pH=a,则a应控制在__________________ 的范围内。
(5)沉淀C是草酸钇,其化学式为____________________ 。
以钇矿石(Y2FeBe2Si2O10) 为原料生产氧化钇(Y2O3) 的主要流程如下:

资料卡:有关金属离子形成氢氧化物沉淀时的pH如下表:
| 开始沉淀时的pH | 完全沉淀时的pH | |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
(2)操作Ⅰ是
(3)加盐酸时,发生中和反应的化学方程式为:
(4)调节pH=a,则a应控制在
(5)沉淀C是草酸钇,其化学式为
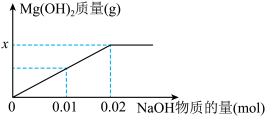
制盐在我国有着悠久的历史。某粗盐中主要含有NaCl、Na2SO4及少量MgSO4和CaSO4,为获取NaCl和Na2SO4,取样品溶于水得到溶液A,进行如图实验:______ g。_______ 。
(3)Ⅲ中加入过量稀盐酸的目的是_______ 。
(4)将“溶液D”在80℃时蒸发浓缩,有少量固体析出。
NaCl和Na2SO4在不同温度下的溶解度:
①经检验,少量固体是纯净的Na2SO4。分析NaCl不析出的原因是______ 。
②停止蒸发浓缩,降温至10℃并过滤,得到大量固体及母液。设计实验检验所得固体中是否含有NaCl:_______ 。从母液中获得NaCl固体的方法是_______ 。

(3)Ⅲ中加入过量稀盐酸的目的是
(4)将“溶液D”在80℃时蒸发浓缩,有少量固体析出。
NaCl和Na2SO4在不同温度下的溶解度:
| 温度/℃ | 10 | 40 | 80 | |
| 溶解度(g/100g水) | NaCl | 35.8 | 36.6 | 38.4 |
| Na2SO4 | 9.1 | 48.8 | 43.7 | |
②停止蒸发浓缩,降温至10℃并过滤,得到大量固体及母液。设计实验检验所得固体中是否含有NaCl:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


