科学探究题 较难0.4 引用1 组卷193
某兴趣小组对鸡蛋壳的主要成分和含量进行了探究。
I.定性探究
实验一:探究鸡蛋壳的主要成分
【查阅资料】鸡蛋壳中含钙元素。
【实验步骤和现象】取一些鸡蛋壳于一支洁净的试管中,加入过量稀盐酸,产生无色无气味的气体,将该气体通入澄清石灰水中,石灰水变浑浊。
【结论】____________ ;
写出该气体通入澄清石灰水中的化学反应方程式_____________________ ;
实验二:做无壳鸡蛋
【实验步骤和现象】如图所示:将一个新鲜鸡蛋放入水中,鸡蛋沉入水底。加入量浓盐酸后,鸡蛋会出现上浮、下沉、再上浮、再下沉的现象,反复多次。最后变成无壳鸡蛋。
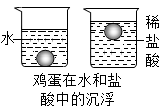
【解释与交流】用化学和物理知识解释鸡蛋上浮、下沉多次的原因_____________________ ;
Ⅱ.定量探究
化学兴趣小组为了测定鸡蛋壳中主要成分的含量(其它成分不溶于水也不与酸反应)做如下实验。取用2.00 g鸡蛋壳样品,把20.00 g稀盐酸分4次加入样品中,充分反应后过滤,取滤渣,洗涤、干燥、称量,得实验数据如下:
(1)从以上数据可知,这四次实验中,第___________ 次样品中主要成分已完全反应。
[(2)(3)计算过程中和最后数字精确到0.01,若是百分数,则精确到0.1%]
(2)求出鸡蛋壳中主要成分的含量和所用稀盐酸的溶质质量分数为______ (写出计算过程)。
(3)在上述实验所得滤液中加30.00g水,加入__________ g氢氧化钙能使溶液pH等于7。此时,所得溶液的溶质质量分数为 ______________ 。
(4)用36.5%的浓盐酸配制20.00g上述稀盐酸需加水的体积为_______ (保留一位小数)。
I.定性探究
实验一:探究鸡蛋壳的主要成分
【查阅资料】鸡蛋壳中含钙元素。
【实验步骤和现象】取一些鸡蛋壳于一支洁净的试管中,加入过量稀盐酸,产生无色无气味的气体,将该气体通入澄清石灰水中,石灰水变浑浊。
【结论】
写出该气体通入澄清石灰水中的化学反应方程式
实验二:做无壳鸡蛋
【实验步骤和现象】如图所示:将一个新鲜鸡蛋放入水中,鸡蛋沉入水底。加入量浓盐酸后,鸡蛋会出现上浮、下沉、再上浮、再下沉的现象,反复多次。最后变成无壳鸡蛋。

【解释与交流】用化学和物理知识解释鸡蛋上浮、下沉多次的原因
Ⅱ.定量探究
化学兴趣小组为了测定鸡蛋壳中主要成分的含量(其它成分不溶于水也不与酸反应)做如下实验。取用2.00 g鸡蛋壳样品,把20.00 g稀盐酸分4次加入样品中,充分反应后过滤,取滤渣,洗涤、干燥、称量,得实验数据如下:
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入5.00 g | 1.50 g |
| 第二次加入5.00 g | 1.00 g |
| 第三次加入5.00 g | 0.50 g |
| 第四次加入5.00 g | 0.30 g |
(1)从以上数据可知,这四次实验中,第
[(2)(3)计算过程中和最后数字精确到0.01,若是百分数,则精确到0.1%]
(2)求出鸡蛋壳中主要成分的含量和所用稀盐酸的溶质质量分数为
(3)在上述实验所得滤液中加30.00g水,加入
(4)用36.5%的浓盐酸配制20.00g上述稀盐酸需加水的体积为
2015·江苏南京·一模
类题推荐
H2O2溶液俗称双氧水,在生活、生产和实验研究中均有广泛应用。现有一瓶已开启过一段时间的H2O2溶液,标签内容见图-1。

【配制溶液】配制浓度约为5%的过氧化氢溶液
(1)用这种溶质质量分数为30%的H2O2溶液,与H2O以1:5的体积比混合后,所得溶液的溶质质量分数为______ 。(结果精确到0.1%)
【测定浓度】H2O2溶液的浓度可以采用酸化的KMnO4溶液来标定,主要的反应方程式为: 。
。
(2)取20mL配得的H2O2溶液(密度近似为1.0g/mL)加入少量稀H2SO4,不断滴入一定浓度的KMnO4标准液(每1000mL溶液中含KMnO415.8g),边滴边振荡,直到溶液刚好呈浅红色为止(可认为KMnO4和H2O2恰好完全反应),测得该H2O2溶液的溶质质量分数为1.5%。计算:标定中滴入KMnO4标准液多少毫升?(结果精确到0.1mL)
(3)配得溶液的浓度和标定浓度直偏差的原因是______ 。
【拓展研究】
(4)以图-2所示装置进行实验I~IV,研究影响H2O2分解的因素,每组实验做3次,内容见表格。(室温为20℃,氧气浓度传感器初始读数为21%,水浴时间均为5分钟。)
①实验I试管中产生的气泡是溶解在水中的空气,说明气体的溶解性受________ 影响。
②实验I的目的是________ 。
③通过以上实验,得出加快H2O2分解的原因是________ 。
④实验V:将光亮的粗铜丝灼烧后,迅速伸入盛有10mL30%H2O2溶液和1mL2%H2SO4溶液的试管中(见图-3)。溶液中立即产生大量气泡,该气体能使带火星的木条复燃。
(5)仅通过实验V,得出“Cu也能加快H2O2分解”的证据是否充足?请做出判断,并说明理由:______ 。

【配制溶液】配制浓度约为5%的过氧化氢溶液
(1)用这种溶质质量分数为30%的H2O2溶液,与H2O以1:5的体积比混合后,所得溶液的溶质质量分数为
【测定浓度】H2O2溶液的浓度可以采用酸化的KMnO4溶液来标定,主要的反应方程式为:
(2)取20mL配得的H2O2溶液(密度近似为1.0g/mL)加入少量稀H2SO4,不断滴入一定浓度的KMnO4标准液(每1000mL溶液中含KMnO415.8g),边滴边振荡,直到溶液刚好呈浅红色为止(可认为KMnO4和H2O2恰好完全反应),测得该H2O2溶液的溶质质量分数为1.5%。计算:标定中滴入KMnO4标准液多少毫升?(结果精确到0.1mL)
(3)配得溶液的浓度和标定浓度直偏差的原因是
【拓展研究】
(4)以图-2所示装置进行实验I~IV,研究影响H2O2分解的因素,每组实验做3次,内容见表格。(室温为20℃,氧气浓度传感器初始读数为21%,水浴时间均为5分钟。)
| 实验编号 | 具支试管内的试剂 | 水浴温度 | 试管内现象 | 传感器3次读数(%) |
| I | 10mL蒸馏水 1mL2%H2SO4溶液 | 20℃ | 无气泡 | 21,21,21 |
| 40℃ | 极少量气泡 | 21,21,21 | ||
| II | 10mL30%H2O2溶液 | 20℃ | 无气泡 | 21,21,21 |
| 40℃ | 极少量气泡 | 24,23,24 | ||
| III | 10mL30%H2O2溶液 1mL2%H2SO4溶液 | 20℃ | 无气泡 | 21,21,21 |
| 40℃ | 少量气泡 | 27,28,28 | ||
| IV | 10mL30%H2O2溶液 1mL2%CuSO4溶液 | 20℃ | 少量气泡 | 35,34,33 |
| 40℃ | 大量气泡 | 69,70,69 |
②实验I的目的是
③通过以上实验,得出加快H2O2分解的原因是
④实验V:将光亮的粗铜丝灼烧后,迅速伸入盛有10mL30%H2O2溶液和1mL2%H2SO4溶液的试管中(见图-3)。溶液中立即产生大量气泡,该气体能使带火星的木条复燃。
(5)仅通过实验V,得出“Cu也能加快H2O2分解”的证据是否充足?请做出判断,并说明理由:
为探究过氧化氢的制取O2的反应,同学们进行了以下实验。
初步探究:探究影响过氧化氢制取O2速率的因素
继续探究:重复烧杯1、3、4实验,并分别伸入带火星木条,如图所示。
(结论与解释)
(1)过氧化氢的制取O2属于四种基本反应类型中的______ 。
(2)为证明MnO2和CuSO4能加快过氧化氢的分解速率,应增加的对比实验是______ (填具体操作)。
(3)能证明过氧化氢溶液浓度影响其分解速率的实验是______ (填烧杯的数字序号)。
(4)烧杯内出现大量白雾的原因是______ 。
(反思与评价)
(5)实验室若用双氧水制取氧气来完成木炭燃烧的实验,应选择的试剂是______ (填字母序号)。
A5%过氧化氢溶液 B10%过氧化氢溶液
C20%过氧化氢溶液 D二氧化锰
(6)实验室取68g过氧化氢溶液和2g二氧化锰混合制取氧气,充分反应后,称量剩余溶液和滤渣为68.4g。则参加反应的过氧化氢溶液中溶质的质量分数为______ 。
初步探究:探究影响过氧化氢制取O2速率的因素
| 序号 | 烧杯1 | 烧杯2 | 烧杯3 | 烧杯4 |
| 实验操作 |  |  |  |  |
| 实验现象 | 立即冒大量气泡,烧杯内有 少量白雾出现。 | 5分钟后,有比较大量的气泡冒出。 | 立即冒大量气泡,烧杯内有白雾。 | 立即冒大量气泡,烧杯内有大量白雾。 |
继续探究:重复烧杯1、3、4实验,并分别伸入带火星木条,如图所示。
| 实验方案 | 序号 | 实验现象 |
 | 烧杯1 | 木条复燃,燃烧很旺 |
| 烧杯3 | 木条复燃,之后火焰变微弱 | |
| 烧杯4 | 木条复燃,之后立即熄灭 |
(结论与解释)
(1)过氧化氢的制取O2属于四种基本反应类型中的
(2)为证明MnO2和CuSO4能加快过氧化氢的分解速率,应增加的对比实验是
(3)能证明过氧化氢溶液浓度影响其分解速率的实验是
(4)烧杯内出现大量白雾的原因是
(反思与评价)
(5)实验室若用双氧水制取氧气来完成木炭燃烧的实验,应选择的试剂是
A5%过氧化氢溶液 B10%过氧化氢溶液
C20%过氧化氢溶液 D二氧化锰
(6)实验室取68g过氧化氢溶液和2g二氧化锰混合制取氧气,充分反应后,称量剩余溶液和滤渣为68.4g。则参加反应的过氧化氢溶液中溶质的质量分数为
小梅在实验室发现一瓶标签残缺的无色溶液,其标签如图所示。

【提出问题】该溶液的溶质是什么?
【分析问题】根据老师的介绍及试剂的存放规律,该溶液的溶质可能是Ba(OH)2、BaCl2,或Ba(NO3)2中的一种。
【查阅资料】20℃时几种物质的溶解度如表:
【推理分析】通过分析该溶液一定不是______ ,理由是______ 。
【实验探究】为确定该溶液究竟是剩余两种溶液中的哪一种,同学们设计了如下实验:
发生反应的化学方程式为______ 。
【拓展探究】实验后,小梅在整理实验室时,发现有一瓶含有氯化钡的废液,经检测,该溶液显酸性。老师指出,这是某同学进行酸碱中和反应实验产生的,则参加反应的酸和碱溶液分别为______ 。为了对该废液进行处理,小梅同学向废液中逐滴滴入碳酸钠溶液,记录滴人碳酸钠溶液质量(x)与有关量的变化关系如图所示。
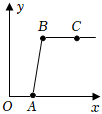
①图中纵坐标(y)表示______ (填“生成气体的质量”或“生成沉淀的质量”)。
②表示氯化钡与碳酸钠溶液反应的区间为______ (填“OA”“AB”或“BC”)段。

【提出问题】该溶液的溶质是什么?
【分析问题】根据老师的介绍及试剂的存放规律,该溶液的溶质可能是Ba(OH)2、BaCl2,或Ba(NO3)2中的一种。
【查阅资料】20℃时几种物质的溶解度如表:
| 物质 | Ba(OH)2 | Ba(NO3)2 | BaCl2 |
| 溶解度/g | 3.89 | 9.02 | 35.8 |
【实验探究】为确定该溶液究竟是剩余两种溶液中的哪一种,同学们设计了如下实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴入硝酸银溶液 | 该溶液为氯化钡溶液 |
【拓展探究】实验后,小梅在整理实验室时,发现有一瓶含有氯化钡的废液,经检测,该溶液显酸性。老师指出,这是某同学进行酸碱中和反应实验产生的,则参加反应的酸和碱溶液分别为

①图中纵坐标(y)表示
②表示氯化钡与碳酸钠溶液反应的区间为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


