科学探究题 适中0.65 引用1 组卷41
化学小组的同学对“暖宝宝”(标签如下图)感到好奇,进行了一系列探究活动。
【查阅资料】
①蛭石:一种天然矿物,加工后具有极强的保温隔热性能。
②吸水性树脂:一种新型高分子材料,吸水能力强,可反复吸收水、释放水。
③暖宝宝的发热原理是铁粉吸氧腐蚀过程中放出热量。加入活性炭能形成微电池,反应更快。
(1)请补全铁吸氧腐蚀的总反应方程式:
___________  ;
;
【提出问题1】
如何证明“暖宝宝”袋内含有铁粉?
【进行实验】
①取出袋内粉末于滤纸上,用磁铁充分吸引。
②将少量磁铁吸出的粉末置于试管内,加入足量稀盐酸。
【观察现象】
(2)磁铁吸出的粉末与稀盐酸反应,___________ 。
【得出结论】
袋内含有铁粉。
【提出问题2】
哪些因素会影响铁吸氧腐蚀的速率?
【进行实验】
小组同学设计了如图所示的实验装置,进行如下5组实验。
每组实验加入的铁炭总质量为 ,食盐水体积为
,食盐水体积为 ,恰好能将固体润湿。
,恰好能将固体润湿。
【解释与结论】
(3)通过实验发现,铁炭质量比对铁吸氧腐蚀速率的影响是___________ 。
(4)要分析食盐水浓度对铁吸氧腐蚀速率的影响,应对比实验___________ (填实验序号)。
(5)示数差 是指U型管左侧液面比右侧液面高
是指U型管左侧液面比右侧液面高 。出现该现象的原因是
。出现该现象的原因是___________ 。
【反思与评价】
(6)依据以上实验,你认为最佳原料配比为第几组,并说明理由___________ 。
【查阅资料】
①蛭石:一种天然矿物,加工后具有极强的保温隔热性能。
②吸水性树脂:一种新型高分子材料,吸水能力强,可反复吸收水、释放水。
③暖宝宝的发热原理是铁粉吸氧腐蚀过程中放出热量。加入活性炭能形成微电池,反应更快。
| 【产品名称】一次性发热贴 【主要成分】铁粉、活性炭、水、吸水性树脂、食盐、蛭石 【产品性能】平均温度53℃,持续时间≥10h |
(1)请补全铁吸氧腐蚀的总反应方程式:
【提出问题1】
如何证明“暖宝宝”袋内含有铁粉?
【进行实验】
①取出袋内粉末于滤纸上,用磁铁充分吸引。
②将少量磁铁吸出的粉末置于试管内,加入足量稀盐酸。
【观察现象】
(2)磁铁吸出的粉末与稀盐酸反应,
【得出结论】
袋内含有铁粉。
【提出问题2】
哪些因素会影响铁吸氧腐蚀的速率?
【进行实验】
小组同学设计了如图所示的实验装置,进行如下5组实验。
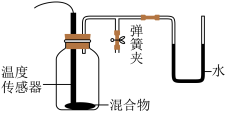
每组实验加入的铁炭总质量为
| 序号 | 铁炭质量比 | 食盐水浓度/% | 示数差3cm所用时间/s | 10分钟时温度升高值/℃ |
| ① | 26 | 90 | 7.8 | |
| ② | 26 | 170 | 4.2 | |
| ③ | 26 | 190 | 3.3 | |
| ④ | 13 | 140 | 6 | |
| ⑤ | 6.5 | 150 | 6 |
(3)通过实验发现,铁炭质量比对铁吸氧腐蚀速率的影响是
(4)要分析食盐水浓度对铁吸氧腐蚀速率的影响,应对比实验
(5)示数差
【反思与评价】
(6)依据以上实验,你认为最佳原料配比为第几组,并说明理由
2024·湖南衡阳·二模
类题推荐
小明网购金鱼时,暖心的商家附赠了一些增氧颗粒一粒粒氧。打开包装,里面是一些白色的颗粒(如图所示)。小明对此产生了极大的兴趣,于是展开了探究。



【查阅资料】过碳酸钠,它是一种白色结晶颗粒,易溶于水,且能与水反应生成碳酸钠和其他化合物。
【猜想与假设】增氧颗粒的主要成分是过碳酸钠。
【设计并实施实验】
【结果分析】增氧颗粒的主要成分是过碳酸钠,根据化学反应方程式:X+H2O=Na2CO3+H2O2,推出过碳酸钠的化学式X为______ 。
【反思应用】通过实验探究,小明更加体会到分液漏斗的优点______ ,同时也意识到在日常保存增氧颗粒时应注意______ 。




【查阅资料】过碳酸钠,它是一种白色结晶颗粒,易溶于水,且能与水反应生成碳酸钠和其他化合物。
【猜想与假设】增氧颗粒的主要成分是过碳酸钠。
【设计并实施实验】
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取少量增氧颗粒于烧杯中,加入足量蒸馏水充分搅拌 | 固体完全溶解形成无色溶液 | / |
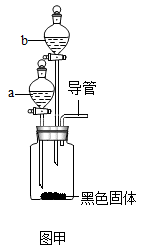
| ② | 在如图甲的集气瓶中加入少量 | 生成大量气泡, | 增氧剂溶于水生成了过氧化氢 |
| ③ | 关闭仪器a,在仪器b中加入稀盐酸;打开活塞,放出适量溶液后,在导管口放一燃着的木条;将乙装置与甲装置相连,将气体通入澄清的石灰水 | 生成大量气泡,木条 | 增氧剂溶于水生成了碳酸钠 |
【结果分析】增氧颗粒的主要成分是过碳酸钠,根据化学反应方程式:X+H2O=Na2CO3+H2O2,推出过碳酸钠的化学式X为
【反思应用】通过实验探究,小明更加体会到分液漏斗的优点
过氧化氢在生产生活中有广泛应用。实验小组对过氧化氢的某些性质进行研究。
Ⅰ.不稳定性
(1)如图所示进行实验,过氧化氢分解的化学方程式为______ ,产生3.2gO2时分解的过氧化氢的质量为______ g。
(2)能用排水法收集O2的原因是______ 。
(3)探究温度对过氧化氢分解速率的影响
同学们进行了如下的实验,实验数据如下表:
由此得出的结论是______ 。
Ⅱ.腐蚀性
【查阅资料】H2O2溶液有腐蚀性。
【进行实验】
将铜片分别浸泡在3种溶液中进行实验,如下表。
【解释与结论】
(4)实验①的作用是______ 。
(5)铜片被腐蚀的反应如下,补全该反应的化学方程式:Cu+H2O2+H2SO4=CuSO4+______ 。
【反思交流】
(6)某同学提出,实验②中,除发生(5)的反应外。还发生了一个反应导致有细小气泡产生,该反应的反应物为______ 。

Ⅰ.不稳定性
(1)如图所示进行实验,过氧化氢分解的化学方程式为
(2)能用排水法收集O2的原因是
(3)探究温度对过氧化氢分解速率的影响
同学们进行了如下的实验,实验数据如下表:
| 实验序号 | ① | ② | ③ |
| H2O2溶液的浓度% | 30 | 30 | 30 |
| H2O2溶液的体积/mL | 6 | 6 | 6 |
| 温度/℃ | 20 | 35 | 55 |
| MnO2的用量/g | 0 | 0 | 0 |
| 收集O2的体积/mL | 0 | 1.9 | 7.8 |
| 反应时间 | 40min | 40min | 40min |
Ⅱ.腐蚀性
【查阅资料】H2O2溶液有腐蚀性。
【进行实验】
将铜片分别浸泡在3种溶液中进行实验,如下表。
| 编号 | ① | ② | ③ |
| 实验 |  |  |  |
| 一段时间后的现象 | 无明显变化 | 溶液变蓝,缓慢产生细小气泡 | 无明显变化 |
(4)实验①的作用是
(5)铜片被腐蚀的反应如下,补全该反应的化学方程式:Cu+H2O2+H2SO4=CuSO4+
【反思交流】
(6)某同学提出,实验②中,除发生(5)的反应外。还发生了一个反应导致有细小气泡产生,该反应的反应物为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



