实验题 适中0.65 引用1 组卷79
氢气是一种清洁、高能燃料。用图1、图2装置开展H2制取、性质的实验。
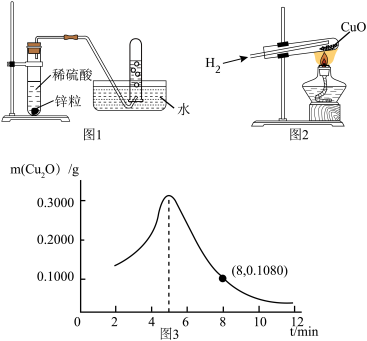
(1)如图1,制取氢气的化学方程式为______ ;可用排水法收集氢气的原因是______ ;当观察到______ 时,说明氢气已收集满。
(2)如图1,是H2还原CuO的实验。
①实验中要向试管内先通一会氢气,然后再加热的目的是______ 。
②反应过程中试管内固体由______ 色变红色,说明氢气具有还原性。
③称取0.6000g的CuO,用H2还原。用热分析仪检测到在不同时间(t)所得固体中Cu2O的质量(m)如图3所示。若反应进行至8分钟时,固体全部为红色。分析红色固体的组成及质量______ 。
(1)如图1,制取氢气的化学方程式为
(2)如图1,是H2还原CuO的实验。
①实验中要向试管内先通一会氢气,然后再加热的目的是
②反应过程中试管内固体由
③称取0.6000g的CuO,用H2还原。用热分析仪检测到在不同时间(t)所得固体中Cu2O的质量(m)如图3所示。若反应进行至8分钟时,固体全部为红色。分析红色固体的组成及质量
2024·上海崇明·二模
类题推荐
我国科学家屠呦呦因研制出抗疟新药——青蒿素和双氢青蒿素而获得诺贝尔奖,被誉为“拯救 2 亿人口”的发现。
(1)下列关于青蒿素(化学式为 C15H22O5)的说法正确的是_____ (从 AB、C 中选 );
A.青蒿素属于有机物
B.青蒿素中氧元素的质量分数最小
C.青蒿素由由 C、H、O 三种原子构成
D.青蒿素中氢、氧元素质量比为_____ (填最简整数比)。
(2)为测定双氢青蒿素的组成元素及各元素的质量比,兴趣小组进行了以下探究。
【设计实验】兴趣小组设计并进行了如图一所示的实验(装置气密性良好)。
①装置 AB 中盛放的试剂分别是____ (填序号)。
I.足量 NaOH 溶液、足量浓硫酸 II.足量浓硫酸、足量 NaOH 溶液
其中,NaOH 溶液的作用是(用化学方程式表示)_____ 。
【记录数据】加热前,先通入空气一段时间,再称量装置 D 的质量、装置 E 的质量(反应前的质量)。双青蒿素完全反应后,停止加热,继续通入空气一段时间,再次称量装置 D 的质量、装置 E 的质量(反应后的质量),实验数据如表所示。
【实验结论】
②有机物化学式一般是按 C、H、O、N 元素的顺序书写。根据表中数据计算,双青蒿素中各元素的质量比是_______ ;双青蒿素分子中各原子的个数比是______ 。
【实验反思】
③实验过程中,加热前要先通入空气一段时间,该操作的作用是_______ 。
【实验分析】
④有同学建议,为使实验结果更准确,需要在装置 C 和 D 之间增加图二所示的装置,其目的是_____ 。
【拓展提高】
⑤你还有什么改进的措施,使实验结果更加准确,请简述你的方法及理由:_______ 。
(1)下列关于青蒿素(化学式为 C15H22O5)的说法正确的是
A.青蒿素属于有机物
B.青蒿素中氧元素的质量分数最小
C.青蒿素由由 C、H、O 三种原子构成
D.青蒿素中氢、氧元素质量比为
(2)为测定双氢青蒿素的组成元素及各元素的质量比,兴趣小组进行了以下探究。
【设计实验】兴趣小组设计并进行了如图一所示的实验(装置气密性良好)。
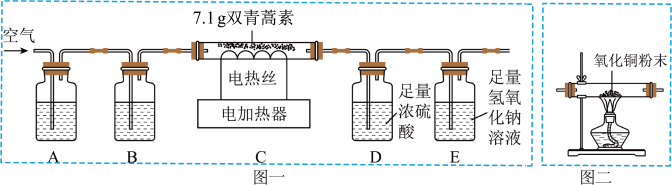
①装置 AB 中盛放的试剂分别是
I.足量 NaOH 溶液、足量浓硫酸 II.足量浓硫酸、足量 NaOH 溶液
其中,NaOH 溶液的作用是(用化学方程式表示)
【记录数据】加热前,先通入空气一段时间,再称量装置 D 的质量、装置 E 的质量(反应前的质量)。双青蒿素完全反应后,停止加热,继续通入空气一段时间,再次称量装置 D 的质量、装置 E 的质量(反应后的质量),实验数据如表所示。
| 装置 | 反应前的质量/g | 反应后的质量/g |
| D | 74.7 | 80.1 |
| E | 80.3 | 96.8 |
②有机物化学式一般是按 C、H、O、N 元素的顺序书写。根据表中数据计算,双青蒿素中各元素的质量比是
【实验反思】
③实验过程中,加热前要先通入空气一段时间,该操作的作用是
【实验分析】
④有同学建议,为使实验结果更准确,需要在装置 C 和 D 之间增加图二所示的装置,其目的是
【拓展提高】
⑤你还有什么改进的措施,使实验结果更加准确,请简述你的方法及理由:
下图是实验室制取气体常用的发生装置和收集装置。
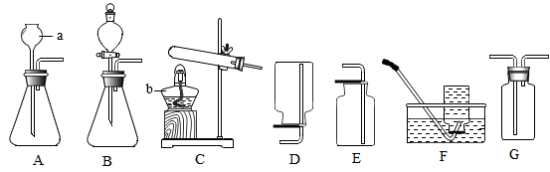
请你回答下列问题:
(1)写出标号仪器的名称:a__________ ,b_________ 。
(2)实验室用过氧化氢溶液制取氧气,若从控制反应速率和节约药品的角度考虑,应选择的发生装置是_________ (填字母编号)。实验室用高锰酸钾制取氧气,反应的化学方程式是________________________ ,反应后的固体剩余物属于_________ (填“混合物”或“纯净物”)。D、E、F、G都是气体的收集装置,其中不能用来收集氧气的是_________ (填字母编号)。
(3)6.32克高锰酸钾加热一段时间后,剩余固体中K、O原子个数比为2:7,则生成氧气的质量为________ 。
(4)某气体X可用D装置收集,若改用G装置收集,则气体X应从_________ (填“左”或“右”)端导管通入。
(5)某校兴趣小组在实验室做制取氧气的实验,他们取氯酸钾和二氧化锰的混合物6.0g放入大试管中进行加热,并在不同时刻测定试管内剩余固体的质量如下表。
分析表中数据,完成下列问题:
①氯酸钾中钾、氯、氧三种元素的质量比为______ (最简整数比)
②生成氧气的质量为______ g.
③原混合物中二氧化锰的质量分数是多少?(写出计算过程,计算结果精确到0.1%)_____

请你回答下列问题:
(1)写出标号仪器的名称:a
(2)实验室用过氧化氢溶液制取氧气,若从控制反应速率和节约药品的角度考虑,应选择的发生装置是
(3)6.32克高锰酸钾加热一段时间后,剩余固体中K、O原子个数比为2:7,则生成氧气的质量为
(4)某气体X可用D装置收集,若改用G装置收集,则气体X应从
(5)某校兴趣小组在实验室做制取氧气的实验,他们取氯酸钾和二氧化锰的混合物6.0g放入大试管中进行加热,并在不同时刻测定试管内剩余固体的质量如下表。
| 反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 |
| 剩余固体质量/g | 5.1 | 4.5 | 4.2 | 4.08 | 4.08 | 4.08 |
①氯酸钾中钾、氯、氧三种元素的质量比为
②生成氧气的质量为
③原混合物中二氧化锰的质量分数是多少?(写出计算过程,计算结果精确到0.1%)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网