科学探究题 适中0.65 引用2 组卷130
“暖宝宝”是我们日常生活中常用的物品。小孔同学打开一个使用过的“吸宝宝”内包装,发现黑色固体中掺杂有红棕色物质,于是她把这包固体带到实验室,和兴趣小组的同学在老师的指导下对这包固体的成分展开了探究。
①铁与空气中的氧气、水蒸气等发生缓慢氧化而生锈;
②“暖宝宝”中只有氯化钠含有氯元素。
【初步判断】
(1)通过阅读标签(如1图),大家一致认为使用“暖宝宝”的过程中,铁扮与空气接触发生了______ (埃“物理变化”或“化学变化”),并有______ (填“吸热”或“放热”)的现象;其中出现的红棕色物质是______ (填物质名称)。
【提出问题】这包使用过的“暖宝宝”中是否还有铁粉、活性炭、氯化钠?
【实验探究】
(2)兴趣小组同学设计如下实验方案并进行实验:
(3)写出实验3中反应的化学方程式______ 。
【反思评价】
(4)小孔同学认为实验2不能得出固体中有活性炭的结论,理由是______ (写一点)。

①铁与空气中的氧气、水蒸气等发生缓慢氧化而生锈;
②“暖宝宝”中只有氯化钠含有氯元素。
【初步判断】
(1)通过阅读标签(如1图),大家一致认为使用“暖宝宝”的过程中,铁扮与空气接触发生了
【提出问题】这包使用过的“暖宝宝”中是否还有铁粉、活性炭、氯化钠?
【实验探究】
(2)兴趣小组同学设计如下实验方案并进行实验:
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验1 | 取少量固体于试管中,加入足量的稀硫酸 | 有铁粉 | |
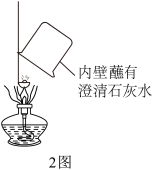
| 实验2 | 取少量固体放在燃烧匙中,用酒精灯灼烧,上方罩一个内壁沾有澄清石失水的烧杯(如2图) | 澄清石灰水变浑浊 | 有活性炭 |
| 实验3 | 取少量固体于烧杯中,加入足量的水溶解,过滤,往滤液中滴加少量 | 产生白色沉淀 | 有氯化钠 |
(3)写出实验3中反应的化学方程式
【反思评价】
(4)小孔同学认为实验2不能得出固体中有活性炭的结论,理由是
2024·广东东莞·二模
类题推荐
蜡烛在古代是一种日常照明工具,某兴趣小组对蜡烛进行了如下探究。
【查阅资料】湿润的黄色氯化钯试纸遇一氧化碳会变蓝。
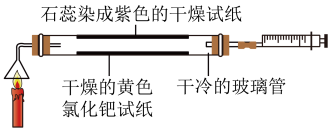
【实验步骤】按图组装仪器,点燃蜡烛,待其正常燃烧后轻轻后拉注射器活塞,将燃烧产物吸入玻璃管内。
【实验现象】
(1)玻璃管内黄色氯化钯试纸变______ 。
(2)石蕊染成紫色的干燥试纸变红,解释试纸变红的原因:______ (用化学方程式表示)。
【实验结论】蜡烛燃烧的产物有水、二氧化碳和一氧化碳。
【活动二】探究蜡烛燃烧时水蒸气和氧气体积分数变化
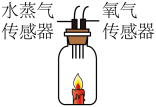
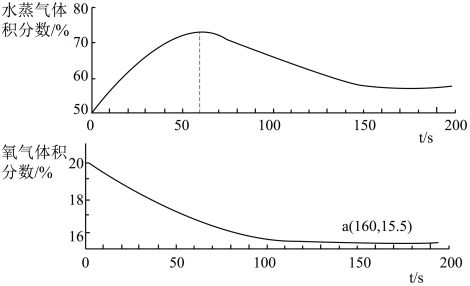
(3)利用水蒸气传感器和氧气传感器同时测出水蒸气体积分数、氧气体积分数与时间的变化关系,其实验装置及数据如图所示。结合水蒸气体积分数曲线,分析60~150s时间段内曲线下降的原因:______ 。______ (写出1点即可)。
【活动三】探究“吹不灭蜡烛”吹不灭的原因及烛芯包裹合金的成分
某同学发现一种蜡烛吹灭大约5s后会重新复燃。于是对这种“吹不灭的蜡烛”进行如下探究。
【查阅资料】①“吹不灭的蜡烛”烛芯里包裹了一层由铜、铁、镁中的一种金属制成的合金,其着火点为150℃。合金中的其他成分化学性质稳定;
②蜡烛燃烧时温度约为550℃~600℃。
【进行实验】为确定该合金中金属的成分,同学们展开了以下探究。
【解释与结论】
(5)根据实验1可确定合金中的金属不是______ 。
(6)实验2中加入的试剂X是______ ,得出“合金中的金属是镁”的理由是______ 。
(7)蜡烛吹灭后又复燃的原因是______ 。
【查阅资料】湿润的黄色氯化钯试纸遇一氧化碳会变蓝。
【实验步骤】按图组装仪器,点燃蜡烛,待其正常燃烧后轻轻后拉注射器活塞,将燃烧产物吸入玻璃管内。
【实验现象】
(1)玻璃管内黄色氯化钯试纸变
(2)石蕊染成紫色的干燥试纸变红,解释试纸变红的原因:
【实验结论】蜡烛燃烧的产物有水、二氧化碳和一氧化碳。
【活动二】探究蜡烛燃烧时水蒸气和氧气体积分数变化
(3)利用水蒸气传感器和氧气传感器同时测出水蒸气体积分数、氧气体积分数与时间的变化关系,其实验装置及数据如图所示。结合水蒸气体积分数曲线,分析60~150s时间段内曲线下降的原因:
【活动三】探究“吹不灭蜡烛”吹不灭的原因及烛芯包裹合金的成分
某同学发现一种蜡烛吹灭大约5s后会重新复燃。于是对这种“吹不灭的蜡烛”进行如下探究。
【查阅资料】①“吹不灭的蜡烛”烛芯里包裹了一层由铜、铁、镁中的一种金属制成的合金,其着火点为150℃。合金中的其他成分化学性质稳定;
②蜡烛燃烧时温度约为550℃~600℃。
【进行实验】为确定该合金中金属的成分,同学们展开了以下探究。
| 序号 | 实验步骤 | 实验现象 |
| 实验1 | 取出烛芯内的合金,用砂纸打磨 | 呈银白色 |
| 实验2 | 取少量打磨后的合金于试管中,滴加适量试剂X,观察现象 | 固体逐渐溶解,有气泡生成,溶液为无色 |
(5)根据实验1可确定合金中的金属不是
(6)实验2中加入的试剂X是
(7)蜡烛吹灭后又复燃的原因是
同学们在学习金属与盐溶液的反应时,老师强调:“金属K、Ca、Na必须除外。”化学兴趣小组的同学们对此产生了兴趣,并在老师的指导下,进行如下探究:
【提出问题】将金属钠投入到硫酸铜溶液中,结果会怎样?
【查找资料】(1)少量钠通常保存在煤油中。
(2)钠是银白色的软金属,可用小刀切割,熔点97.81℃,沸点882.9℃,密度为0.97g/cm3。
(3)钠是一种很活泼的金属,遇水发生剧烈反应,生成氢氧化钠和氢气。
【做出猜想】猜想一:放出气体,生成蓝色沉淀,能置换出铜;猜想二:放出气体,生成蓝色沉淀,不能置换出铜。
【实验探究】
【现象分析】(1)钠熔成小球是因为______ 。
(2)钠与水发生剧烈反应伴有气体生成,反应后的溶液呈碱性,说明溶液中含_____ (填离子符号)。
(3)实验②析出蓝色沉淀是因为______ (用化学方程式表示)。
【继续探究】有部分同学认为置换出的铜可能被蓝色沉淀掩盖。于是他们进一步探究:
【实验结论】猜想______ 正确。在金属活动性顺序里,位于前面的金属(K、Ca、Na必须除外)能把位于后面的金属从它们盐的溶液里置换出来。K、Ca、Na必须除外是因为_______ 。
【提出问题】将金属钠投入到硫酸铜溶液中,结果会怎样?
【查找资料】(1)少量钠通常保存在煤油中。
(2)钠是银白色的软金属,可用小刀切割,熔点97.81℃,沸点882.9℃,密度为0.97g/cm3。
(3)钠是一种很活泼的金属,遇水发生剧烈反应,生成氢氧化钠和氢气。
【做出猜想】猜想一:放出气体,生成蓝色沉淀,能置换出铜;猜想二:放出气体,生成蓝色沉淀,不能置换出铜。
【实验探究】
| 实验操作 | 实验现象 |
| ①取一块钠,用滤纸吸干表面煤油,再切取绿豆大小的一块,投入到盛有20ml蒸馏水的烧杯中。待反应结束后向烧杯中滴入几滴无色酚酞溶液。 | 钠浮在液面上,熔化成闪亮小球,钠球游动,发出“嘶嘶”的声响,滴入酚酞溶液后溶液变红色。 |
| ②取20mL一定溶质质量分数的硫酸铜溶液,倒入50mL的烧杯里。取一块钠,用滤纸吸干表面煤油,再切取绿豆大小的一块,投入溶液中。 | 钠浮在液面上,熔化成闪亮小球,钠球游动,发出“嘶嘶”的声响,溶液中有蓝色沉淀析出。 |
【现象分析】(1)钠熔成小球是因为
(2)钠与水发生剧烈反应伴有气体生成,反应后的溶液呈碱性,说明溶液中含
(3)实验②析出蓝色沉淀是因为
【继续探究】有部分同学认为置换出的铜可能被蓝色沉淀掩盖。于是他们进一步探究:
| 实验操作 | 实验现象 | 结论 |
| 取烧杯中少许沉淀于试管中,再向其中加入过量的稀硫酸 | 沉淀全部溶解,溶液变蓝色 |
【实验结论】猜想
为了防止食品腐败,在许多食品包装盒中都有一包黑色粉末。这种粉末是一种除氧剂。该粉末没有失效时呈黑色,失效后带有红棕色。为了确定该粉末的成分,小明做出了以下的猜想:
猜想1:该粉末是木炭粉
猜想2:该粉末是铁粉
猜想3:该粉末是木炭粉和铁粉的混合物
实验探究:
小明取该粉末,分别用不同的方法进行如下实验,填写表中空格。
现象与分析:写出实验2中的化学反应方程式:___________________________________ 。
交流与反思:
⑴根据失效后的颜色判断,该粉末失效的原因是____________________ ,变质后得到的红棕色粉末的主要成分是_____________ (填物质的化学式)。
⑵采用什么实验方法可以使失效的粉末“再生”?_________________ (用化学方程式表示)。
猜想1:该粉末是木炭粉
猜想2:该粉末是铁粉
猜想3:该粉末是木炭粉和铁粉的混合物
实验探究:
小明取该粉末,分别用不同的方法进行如下实验,填写表中空格。
| 实验操作 | 实验现象 | 猜想是否成立 | |
| 实验1 | 加入足量的硫酸铜溶液 | 猜想1:不成立 | |
| 实验2 | 加入足量的稀盐酸 | 猜想2:成立 | |
| 实验3 | 用磁铁吸引 | 粉末被全部吸引 | 猜想3: |
现象与分析:写出实验2中的化学反应方程式:
交流与反思:
⑴根据失效后的颜色判断,该粉末失效的原因是
⑵采用什么实验方法可以使失效的粉末“再生”?
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


