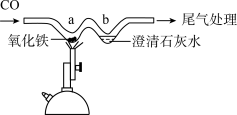
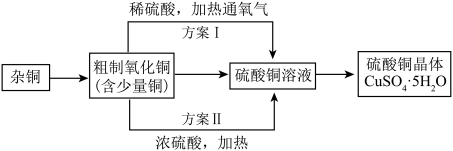
综合应用题 较难0.4 引用2 组卷136
过碳酸钠(2Na2CO3·3H2O2)兼具碳酸钠和过氧化氢双重性质,广泛应用于洗涤、纺织、医药等领域。一种制备过碳酸钠的流程如下。
已知:过碳酸钠在异丙醇中的溶解度较低。______ 。
②结晶发生的化学反应方程式为______ ,加入异丙醇的作用是______ 。
(2)过碳酸钠中有效氧的含量越高,产品的品质越高。已知有效氧[O]%定义为:
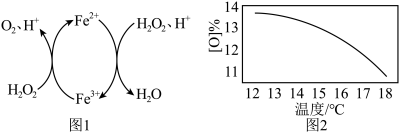
过碳酸钠的理论有效氧为15.29%。在过碳酸钠的制备过程中,温度对产品有效氧[O]%的影响如题28图2所示。取某次制备的产品,测量其有效氧的实验步骤如下:
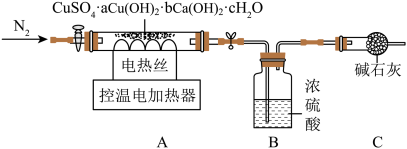
步骤1:称量一定质量的样品加入锥形瓶中,加入10%硫酸至不再产生气体,将所得气体依次通过浓硫酸和碱石灰(由烧碱和氧化钙组成),充分吸收后碱石灰质量增加17.6g。
步骤2:称量与步骤1等质量的样品,放入坩埚中,加热,每隔10分钟测量一次坩埚和坩埚内固体的总质量,记录数据如下:
①计算样品的有效氧,写出计算过程______ 。
②产品有效氧低于理论有效氧的可能原因是______ 。
已知:过碳酸钠在异丙醇中的溶解度较低。
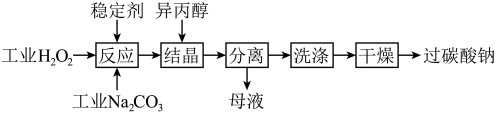
②结晶发生的化学反应方程式为
(2)过碳酸钠中有效氧的含量越高,产品的品质越高。已知有效氧[O]%定义为:
过碳酸钠的理论有效氧为15.29%。在过碳酸钠的制备过程中,温度对产品有效氧[O]%的影响如题28图2所示。取某次制备的产品,测量其有效氧的实验步骤如下:
步骤1:称量一定质量的样品加入锥形瓶中,加入10%硫酸至不再产生气体,将所得气体依次通过浓硫酸和碱石灰(由烧碱和氧化钙组成),充分吸收后碱石灰质量增加17.6g。
步骤2:称量与步骤1等质量的样品,放入坩埚中,加热,每隔10分钟测量一次坩埚和坩埚内固体的总质量,记录数据如下:
| 测量时间/min | 0 | 10 | 20 | 30 | 40 |
| 坩埚和坩埚内固体总质量/g | 109.4 | 102.2 | 95.8 | 92.4 | 92.4 |
②产品有效氧低于理论有效氧的可能原因是
2024·江苏无锡·一模
类题推荐
我国首个大型页岩气田新增页岩气探明储量超千亿立方米,成为我国重要的能源来源。
Ⅰ.页岩气是重要的能源
(1)目前人类大量使用的三大化石能源是煤、石油和天然气,都属于_________ (填“可再生”或“不可再生”)能源。页岩气被公认为是一种清沽、高效的能源资源。为缓解能源危机,人们正积极开发利用新能源,请还列举出其中一种为____________ 。
(2)已知下列表格,请阅读表格数据回答:
①计算1g页岩气中主要成分完全燃烧产生CO2质量m是_____________ ?
②利用表中数据说明,与煤炭相比较,使用页岩气作燃料的优点有(至少一点)_____________ 。
Ⅱ.页岩气是重要的化工原料
(3)甲烷除做燃料外,甲烷还是一种重要的化工原料,在900℃和催化剂条件下,适当比例的甲烷和水反应能生成氢气和一氧化碳。试写出该反应的方程式___________ 。
(4)甲烷无氧催化重整可获得碳氢化合物X,取106g该碳氢化合物X完全燃烧得到90g水,则X的化学式为_____________ 。
Ⅰ.页岩气是重要的能源
(1)目前人类大量使用的三大化石能源是煤、石油和天然气,都属于
(2)已知下列表格,请阅读表格数据回答:
1g物质完全燃烧产生CO2质量 | 1g物质完全燃烧放出的热量 | |
页岩气(主要成分为CH4) | m | 56kJ |
煤炭(主要成分为C) | 3.67g | 32kJ |
①计算1g页岩气中主要成分完全燃烧产生CO2质量m是
②利用表中数据说明,与煤炭相比较,使用页岩气作燃料的优点有(至少一点)
Ⅱ.页岩气是重要的化工原料
(3)甲烷除做燃料外,甲烷还是一种重要的化工原料,在900℃和催化剂条件下,适当比例的甲烷和水反应能生成氢气和一氧化碳。试写出该反应的方程式
(4)甲烷无氧催化重整可获得碳氢化合物X,取106g该碳氢化合物X完全燃烧得到90g水,则X的化学式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网