科学探究题 适中0.65 引用2 组卷147
我国首款具有自主知识产权的大型民用客机C919使用了大量的金属材料。
(1)用铜作导线,利用了铜的_______ 性。
(2)铝常用于制造合金。铝有很强的抗腐蚀性,主要原因是铝的表面形成一层致密的氧化铝薄膜,发生反应的化学方程式为_______ 。
(3)探究Al、Fe和Cu三种金属的活动性顺序。
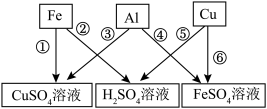
【设计实验】同学们设计了如图的6个实验(图中“→”表示将足量金属片加入到溶液中,如③表示将Al片加入到CuSO4溶液中)。_______ 。
【交流讨论】甲同学做了③和④两个实验,经过观察和分析,得出结论:A1>Fe>Cu。乙同学认为甲同学的结论不合理,理由是______ 。
【反思结论】为达实验目的,从①~⑥的实验中,选择必要的(不多选)实验组合完成探究任务,正确的组合有______ (填实验序号)。
(4)物质的性质决定物质的用途,由以上金属的利用和实验探究归纳出金属的化学性质有______ 。
(5)工业上用CO与赤铁矿(主要成分Fe2O3)高温下反应冶炼铁,该反应的化学方程式为______ 。
(1)用铜作导线,利用了铜的
(2)铝常用于制造合金。铝有很强的抗腐蚀性,主要原因是铝的表面形成一层致密的氧化铝薄膜,发生反应的化学方程式为
(3)探究Al、Fe和Cu三种金属的活动性顺序。
【设计实验】同学们设计了如图的6个实验(图中“→”表示将足量金属片加入到溶液中,如③表示将Al片加入到CuSO4溶液中)。
【交流讨论】甲同学做了③和④两个实验,经过观察和分析,得出结论:A1>Fe>Cu。乙同学认为甲同学的结论不合理,理由是
【反思结论】为达实验目的,从①~⑥的实验中,选择必要的(不多选)实验组合完成探究任务,正确的组合有
(4)物质的性质决定物质的用途,由以上金属的利用和实验探究归纳出金属的化学性质有
(5)工业上用CO与赤铁矿(主要成分Fe2O3)高温下反应冶炼铁,该反应的化学方程式为
2024·贵州·一模
类题推荐
自嗨锅内有一个发热包,加水后即可加热食物,持续时间长达2小时。赫行中学化学兴趣小组对发热包非常感兴趣,在化学实验室对其成分进行探究。
【查阅资料】
a、发热包内的粉末主要由生石灰、铁粉、铝粉、碳粉、氯化钠等组成;
b、铝是一种两性金属,与强酸、强碱溶液反应都能生成H2;
c、AgCl是既不溶于水又不溶于酸的白色沉淀。
d、AgNO3+NaCl=AgCl↓+NaNO3
【实验探究】为确认发热包中各种成分的存在,兴趣小组的同学们设计了实验方案并进行操作。
【实验反思】生石灰与水反应放出的热量是发热包主要的热量来源,该反应的化学方程式为______ ;用完后的发热包按______ (填“可回收垃圾”或“其它垃圾”)分类处理。
【查阅资料】
a、发热包内的粉末主要由生石灰、铁粉、铝粉、碳粉、氯化钠等组成;
b、铝是一种两性金属,与强酸、强碱溶液反应都能生成H2;
c、AgCl是既不溶于水又不溶于酸的白色沉淀。
d、AgNO3+NaCl=AgCl↓+NaNO3
【实验探究】为确认发热包中各种成分的存在,兴趣小组的同学们设计了实验方案并进行操作。
步骤 | 实验操作 | 实验现象 | 实验结论 |
一 | 取部分粉末,将磁铁靠近 | 发现有黑色物质 被磁铁吸引 | 成分中有 |
二 | 将磁铁充分吸附后的剩余粉末分成两份, 其中一份加水溶解,过滤,取滤液测pH | pH试纸变蓝紫色 | pH 成分中有生石灰 |
三 | 取少量滤液于试管中,先加入过量稀 硝酸,再加入少量硝酸银溶液 | 生成白色沉淀 | 成分中有 |
四 | 将另一份粉末放入烧杯,加入适量 NaOH溶液 | 成分中有铝粉 | |
五 | 将步骤二中过滤得到的滤渣放入硬质 玻璃管中 体通入澄清石灰水 | 石灰水变浑浊 | 成分中有碳粉 |
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
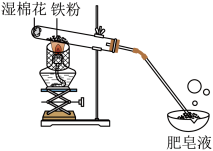
(1)试管尾部放一团湿棉花的目的是______ 。
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中、说明生成的气体是______ 。
(3)探究试管中剩余固体成分是什么?
【查阅资料】
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是______ 。
【实验探究】
【实验结论】铁和水蒸气反应的化学方程式为______ 。

(1)试管尾部放一团湿棉花的目的是
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中、说明生成的气体是
(3)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | |
| 能否被磁铁吸引 | 否 | 否 | 能 |
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是
【实验探究】
| 实验操作 | 实验现象及结论 |
| 取黑色固体少许于试管中,加入 | 有 |
在一次实践活动中,化学兴趣小组的同学们对废旧电池展开了探究。
活动一:观察废旧干电池。
【查阅资料】干电池的结构如图所示,糊状电解质主要成分是氯化铵(化学式NH4C1)。
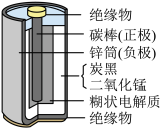
【交流讨论】锌、碳棒作电极,所利用的性质是___________ 。废旧电池中含有Cu、Zn、Hg、Pb等金属元素,其中有害元素是___________ ,因此废旧电池需集中处理。
活动二:拆解废旧干电池,回收利用。
同学们用钳子和剪刀剪开一个废旧电池,取下表层的锌皮,该锌皮可用于_______ 。拆出来的碳棒可继续用作电极。从电池内的黑色粉末(炭黑与二氧化锰的混合物)中回收二氧化锰,除去炭黑的方法是______ (用化学方程式表示)。
活动三:验证废旧干电池中含有氯化铵。
将上述拆解开的废旧干电池中的糊状电解质置于烧杯中,加入足量蒸馏水,搅拌,充分溶解,静置沉淀。取上层清液进行了如下实验:
【实验小结】废旧干电池中含有氯化铵。实验步骤2中发生反应的化学方程式是__________ 。
活动一:观察废旧干电池。
【查阅资料】干电池的结构如图所示,糊状电解质主要成分是氯化铵(化学式NH4C1)。

【交流讨论】锌、碳棒作电极,所利用的性质是
活动二:拆解废旧干电池,回收利用。
同学们用钳子和剪刀剪开一个废旧电池,取下表层的锌皮,该锌皮可用于
活动三:验证废旧干电池中含有氯化铵。
将上述拆解开的废旧干电池中的糊状电解质置于烧杯中,加入足量蒸馏水,搅拌,充分溶解,静置沉淀。取上层清液进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 1.取少量上层清液于试管中,向其中滴加 | 产生刺激性气味的气体 | 含有 |
| 2. | 有白色沉淀生成 | 含有Cl- |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


