填空与简答-填空题 适中0.65 引用1 组卷22
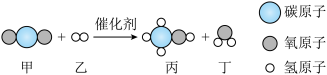
化学知识在生产、生活中有广泛的应用。
(1)检测某水样的pH>7,则该水样呈________ 性。
(2)喝完汽水后会打嗝,这是因为气体溶解度与_________有关。(选填序号)
(3)用下列物质除去油污时,利用乳化作用的是________(选填序号)。
(4)金属铜常用做导线是利用它的________ 性
(5)金属铝表面常有一层致密的氧化膜,氧化膜主要成分是________ (填化学式)
(1)检测某水样的pH>7,则该水样呈
(2)喝完汽水后会打嗝,这是因为气体溶解度与_________有关。(选填序号)
| A.压强 | B.温度 |
(3)用下列物质除去油污时,利用乳化作用的是________(选填序号)。
| A.汽油 | B.洗洁精 | C.氢氧化钠溶液. |
(4)金属铜常用做导线是利用它的
(5)金属铝表面常有一层致密的氧化膜,氧化膜主要成分是
23-24九年级下·湖北襄阳·阶段练习
类题推荐
某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾(CuSO4·5H2O)。其设计的实验过程如下图所示:
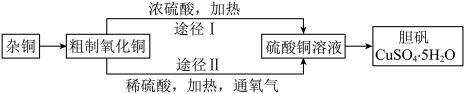
请回答下列问题:
(1)杂质铜中有含有大量的碳粉,可采用在蒸发皿中灼烧的方法除去,其化学方程式为__________ 。
(2)灼烧后的蒸发皿中依然有黑色粉末,于是小华得出了碳粉没有反应完的结论,但遭到了其他同学的反对,他们的理由是__________ 。
(3)杂铜经灼烧后得到的产物是氧化铜和少量铜的混合物,灼烧后含有少量铜的可能原因是:_________
(4)通过途径Ⅱ实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、__________ (填操作名称)、冷却结晶。
(5)由粗制氧化铜通过途径Ⅰ制取胆矾的反应方程式为:Cu+2H2SO4(浓) CuSO4+2X+SO2↑,X的化学式为
CuSO4+2X+SO2↑,X的化学式为__________ 。与途径Ⅰ相比,途径Ⅱ的优点是__________ (答出一点即可)。

请回答下列问题:
(1)杂质铜中有含有大量的碳粉,可采用在蒸发皿中灼烧的方法除去,其化学方程式为
(2)灼烧后的蒸发皿中依然有黑色粉末,于是小华得出了碳粉没有反应完的结论,但遭到了其他同学的反对,他们的理由是
(3)杂铜经灼烧后得到的产物是氧化铜和少量铜的混合物,灼烧后含有少量铜的可能原因是:_________
| A.灼烧过程中部分氧化铜被还原 |
| B.灼烧不充分铜未被完全氧化 |
| C.氧化铜在加热过程中分解生成铜 |
(5)由粗制氧化铜通过途径Ⅰ制取胆矾的反应方程式为:Cu+2H2SO4(浓)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网