科学探究题 较难0.4 引用1 组卷187
兴趣小组对某自热包进行项目式探究和学习。
【查阅资料】
I。自热包的主要成分为生石灰、铝粉、碳酸钠;自热包加水后持续加热时间可达40分钟。
Ⅱ、氢氧化钙微溶于水。
Ⅲ、铝会与氢氧化钠溶液反应并放热,反应原理: 。
。
任务一:探究自热包的发热原理
【提出猜想】根据自热包的成分,兴趣小组进行以下猜想。
猜想一:生石灰与水反应放热
猜想二:铝粉与反应生成的氢氧化钠溶液反应放热。
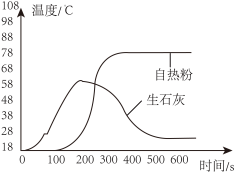
分别取 的自热粉和生石灰与等量的水反应,温度随时间的变化如图所示。
的自热粉和生石灰与等量的水反应,温度随时间的变化如图所示。
(1)生石灰与水反应的化学方程式为______ 。
(2)兴趣小组根据图推测:“生石灰与水反应放热”不是自热包放热的主要原因,理由是______ 。
任务二:探究自热包持续放热的原因
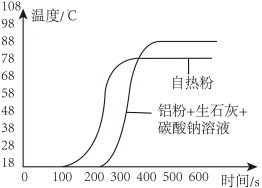
取 铝粉与适量的生石灰、碳酸钠溶液混合,使铝粉完全反应,温度随时间的变化如图所示。
铝粉与适量的生石灰、碳酸钠溶液混合,使铝粉完全反应,温度随时间的变化如图所示。
(3)根据图分析,自热包能够持续发热的可能原因是______ 。
(4)结合资料分析,在使用自热包时,应注意______ 。
任务三:测定自热包中碳酸钠的质量
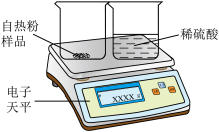
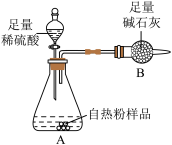
(5)方案1:利用下图实验装置通过称量反应前后两烧杯中物质的质量差作为反应生成二氧化碳的质量,来计算碳酸钠的含量,该方案______ (选填“可行”或“不可行”),请说明理由:______ 。______ ;该方案会导致测定碳酸钠的质量偏______ (选填“大”或“小”),理由是______ (写一点)。
【查阅资料】
I。自热包的主要成分为生石灰、铝粉、碳酸钠;自热包加水后持续加热时间可达40分钟。
Ⅱ、氢氧化钙微溶于水。
Ⅲ、铝会与氢氧化钠溶液反应并放热,反应原理:
任务一:探究自热包的发热原理
【提出猜想】根据自热包的成分,兴趣小组进行以下猜想。
猜想一:生石灰与水反应放热
猜想二:铝粉与反应生成的氢氧化钠溶液反应放热。
分别取
(1)生石灰与水反应的化学方程式为
(2)兴趣小组根据图推测:“生石灰与水反应放热”不是自热包放热的主要原因,理由是
任务二:探究自热包持续放热的原因
取
(3)根据图分析,自热包能够持续发热的可能原因是
(4)结合资料分析,在使用自热包时,应注意
任务三:测定自热包中碳酸钠的质量
(5)方案1:利用下图实验装置通过称量反应前后两烧杯中物质的质量差作为反应生成二氧化碳的质量,来计算碳酸钠的含量,该方案
2024·福建·模拟预测
类题推荐
在上化学探究课时,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
【提出问题】黑色颗粒和白色物质是什么?
【进行猜想】
(1)甲认为黑色颗粒是碳(C),白色物质可能是Na2O或___________ 或____________ ,乙同学还认为白色物质是氢氧化钠。
甲同学立刻认为乙同学的猜想是错误的,其理由是_______________ 。
【查阅资料】氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O+H2O =2NaOH。
【实验探究】
(2)甲同学对白色物质进行实验探究。
【反思评价】
(3)丙同学认为方案1得到的结论不正确,其理由是_______________________ 。
【得出结论】
(4)写出钠在二氧化碳中燃烧的化学方程式为________________________ 。
【提出问题】黑色颗粒和白色物质是什么?
【进行猜想】
(1)甲认为黑色颗粒是碳(C),白色物质可能是Na2O或
甲同学立刻认为乙同学的猜想是错误的,其理由是
【查阅资料】氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O+H2O =2NaOH。
【实验探究】
(2)甲同学对白色物质进行实验探究。
| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取样品少量于试管中,加入适量水,振荡, 样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取样品少量于试管中,加入适量水,振荡, 样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | 白色物质是 |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
【反思评价】
(3)丙同学认为方案1得到的结论不正确,其理由是
【得出结论】
(4)写出钠在二氧化碳中燃烧的化学方程式为
碱式碳酸铜是一种绿色的固体,受热分解成黑色固体物质、二氧化碳和水。这种黑色固体的成分是什么呢?亮亮与同学们进行以下探究:
【猜想】该黑色固体可能是氧化铜,也可能是氧化铜和炭的混合物。
【设计与实验】
接着小明与同学们用氢气还原氧化铜制取铜。
(1)要制得纯净的氢气,小明应选用的药品是______ 。
A 铁和稀硫酸 B 锌和浓盐酸 C 镁和稀硫酸 D 锌和稀硫酸
(2)实验开始时,应先_____ ,然后再加热。
(3)实验结束后,小方同学对还原后的红色物质产生了兴趣,该红色物质一定是单质铜吗?
查阅有关资料获知:氢气与氧化铜在加热条件下能生成氧化亚铜( ),氧化亚铜也呈红色,且能与稀硫酸反应生成硫酸铜、铜和水。
),氧化亚铜也呈红色,且能与稀硫酸反应生成硫酸铜、铜和水。
为此,小方同学又做了两次实验,第一次称取 氧化铜进行实验,得到了
氧化铜进行实验,得到了 红色物质;第二次同样用
红色物质;第二次同样用 氧化铜进行实验,得到了
氧化铜进行实验,得到了 红色物质。
红色物质。
①小方通过对所得实验数据进行计算分析后得知第二次实验得到的红色物质全部是铜,第一次得到的红色物质除铜外,还含有氧化亚铜。小方的分析依据是_____ 。
②随后,他用化学实验方法验证了上述分析结果的正确性。其验证方法是(简要写出操作现象、结论)_____ 。
③从上述实验中,小方获得以下结论:在氢气还原氧化铜实验中,若还原不充分,会得到红色氧化亚铜,请写出氢气还原氧化铜生成氧化亚铜的化学方程式_____ 。
【猜想】该黑色固体可能是氧化铜,也可能是氧化铜和炭的混合物。
【设计与实验】
| 实验步骤 | 实验现象 | 结论和化学方程式 |
| 亮亮同学取少量黑色固体,放入试管中,加入足量的稀硫酸,微热 | 黑色固体完全消失,溶液变 | 此黑色固体是氧化铜。该反应的化学方程式为 |
接着小明与同学们用氢气还原氧化铜制取铜。
(1)要制得纯净的氢气,小明应选用的药品是
A 铁和稀硫酸 B 锌和浓盐酸 C 镁和稀硫酸 D 锌和稀硫酸
(2)实验开始时,应先
(3)实验结束后,小方同学对还原后的红色物质产生了兴趣,该红色物质一定是单质铜吗?
查阅有关资料获知:氢气与氧化铜在加热条件下能生成氧化亚铜(
为此,小方同学又做了两次实验,第一次称取
①小方通过对所得实验数据进行计算分析后得知第二次实验得到的红色物质全部是铜,第一次得到的红色物质除铜外,还含有氧化亚铜。小方的分析依据是
②随后,他用化学实验方法验证了上述分析结果的正确性。其验证方法是(简要写出操作现象、结论)
③从上述实验中,小方获得以下结论:在氢气还原氧化铜实验中,若还原不充分,会得到红色氧化亚铜,请写出氢气还原氧化铜生成氧化亚铜的化学方程式
2012年1月,广西河池宜州市境内龙江河发生了镉浓度超标事件。根据该事件某化学活动小组开展了一次关于金属镉与铜、银活动性顺序的探究及镉污染事故处理方法的研讨活动。
查阅资料:①镉(Cd)是一种银白色金属,在化合物中通常表现为+2价 ②水体中镉元素通常以氯化镉的形式存在 ③氯化镉能溶于水,氢氧化镉难溶于水
(一)金属镉与铜、银活动性顺序的探究
实验结论:活动性顺序:________________________
(二)对镉污染事故处理方法的讨论
小聪认为可用向受污染河段抛撒过量烧碱固体的方法除去氯化镉,反应原理用化学方程式表示为___________________________________ 。小敏认为该方案虽然有效,但有缺陷,原因是__________ 。受小聪与小敏启发,你认为可以用__________ (写俗称)代替烧碱。
查阅资料:①镉(Cd)是一种银白色金属,在化合物中通常表现为+2价 ②水体中镉元素通常以氯化镉的形式存在 ③氯化镉能溶于水,氢氧化镉难溶于水
(一)金属镉与铜、银活动性顺序的探究
| 实验步骤 | 实验现象 | 实验结论 |
| 取适量镉、铜、银于试管中,加入足量 | 镉表面有气泡产生,铜、银表面无气泡产生 | |
| 取适量铜于试管中,加入少量硝酸银溶液 | 铜的活动性顺序大于银 |
(二)对镉污染事故处理方法的讨论
小聪认为可用向受污染河段抛撒过量烧碱固体的方法除去氯化镉,反应原理用化学方程式表示为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


