综合应用题 适中0.65 引用1 组卷61
侯德榜先生为制取纯碱作出了杰出贡献。
(1)实验室模拟制取碳酸氢钠。
“侯氏制碱法”生产纯碱的过程中,碳酸氢钠的生成是至关重要的一环,其原理是: ,
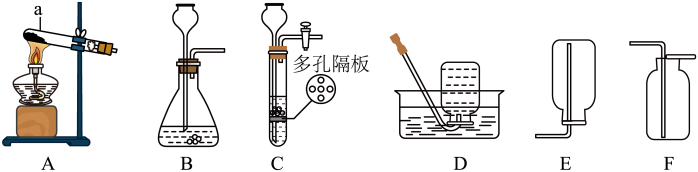
, 。兴趣小组在常温(20℃)下设计并完成了如图所示实验。
。兴趣小组在常温(20℃)下设计并完成了如图所示实验。
[已知20℃时 的溶解度为
的溶解度为 。]
。]
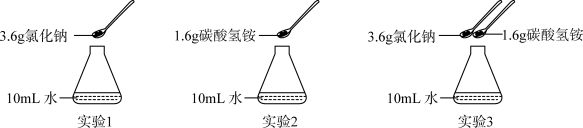
①实验1、2所得溶液处于饱和状态的是___________ (填实验序号)
②实验3的锥形瓶中出现白色浑浊,经检验为NaHCO3。写出用稀盐酸检验NaHCO3的化学方程式:___________ 。
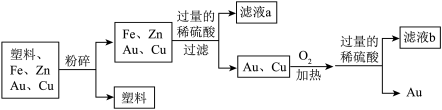
(2)侯氏制碱法的生产流程如下:
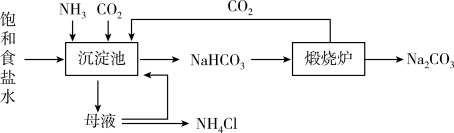
①实际生产中沉淀池内的温度不能太高,原因是___________ 。
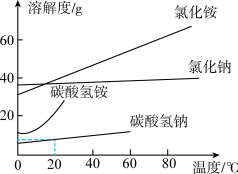
②如图是四种物质的溶解度曲线。母液中含有较高浓度的NH4Cl和少量NaCl,利用:___________ (填“蒸发结晶”或“降温结晶”)的方法可提纯NH4Cl。
③上述流程中可循环利用的物质有:NaCl和___________ 。
(3)测定纯碱样品中碳酸钠的质量分数。
纯碱产品中常混有少量氯化钠,兴趣小组设计以下两种方案测定某纯碱样品中碳酸钠的质量分数:
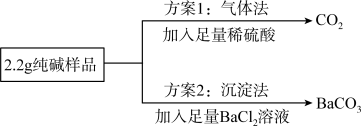
根据方案1,实验测得CO2的质量为0.88g。根据方案2,实验测得BaCO3的质量为3.94g。
请任选其中一种方案与相关数据,计算该纯碱样品中碳酸钠的质量分数(写出计算过程,结果精确到0.1%)。
___________
(1)实验室模拟制取碳酸氢钠。
“侯氏制碱法”生产纯碱的过程中,碳酸氢钠的生成是至关重要的一环,其原理是:
[已知20℃时

①实验1、2所得溶液处于饱和状态的是
②实验3的锥形瓶中出现白色浑浊,经检验为NaHCO3。写出用稀盐酸检验NaHCO3的化学方程式:
(2)侯氏制碱法的生产流程如下:

①实际生产中沉淀池内的温度不能太高,原因是
②如图是四种物质的溶解度曲线。母液中含有较高浓度的NH4Cl和少量NaCl,利用:

③上述流程中可循环利用的物质有:NaCl和
(3)测定纯碱样品中碳酸钠的质量分数。
纯碱产品中常混有少量氯化钠,兴趣小组设计以下两种方案测定某纯碱样品中碳酸钠的质量分数:

根据方案1,实验测得CO2的质量为0.88g。根据方案2,实验测得BaCO3的质量为3.94g。
请任选其中一种方案与相关数据,计算该纯碱样品中碳酸钠的质量分数(写出计算过程,结果精确到0.1%)。
23-24九年级下·江苏苏州·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


 表示一个碳原子,用
表示一个碳原子,用 表示一个氧原子,则可表示
表示一个氧原子,则可表示 的化学符号是
的化学符号是


