实验题 较难0.4 引用2 组卷134
铁丝在氧气中燃烧时,火星四射,得到黑色固体。小新认为所得黑色固体中除了有生成的四氧化三铁,还可能混有少量熔化的、未来得及反应的铁单质。小新取该种黑色固体,研成粉末,设计出3种方案,测定其中铁单质的质量。
【查阅资料】
a.四氧化三铁与稀盐酸反应,Fe3O4 + 8HCl=2FeCl3 + FeCl2 + 4H2O
b.Fe + 2FeCl3 = 3FeCl2
c.四氧化三铁与硫酸铜溶液不反应
d.碱石灰能吸收二氧化碳气体,不能吸收一氧化碳气体
【方案1】
(1)取一定量的黑色粉末,加入足量稀盐酸,准确测量生成的氢气体积,并计算出氢气的质量,再根据化学方程式(铁与稀盐酸反应)______ ,计算出铁单质的质量。
(2)经仔细分析过程中可能发生的反应后,小新的同学认为该方案不合理,存在较大误差。你认为该方案一定会使得测量结果偏大还是偏小?______ ,理由是______ 。
【方案2】实验装置如图一(装置气密性良好):
Ⅱ.连接好装置。缓缓通入CO,片刻后点燃酒精喷灯,待充分反应后,熄灭酒精喷灯,继续通入CO直至硬质玻璃管冷却,反应后测得U型管中碱石灰增加的质量为m3(不考虑空气中的成分对碱石灰质量的影响)。
(3)硬质玻璃管中反应的化学方程式为______ 。
(4)装入硬质玻璃管中样品的质量为(m2-m1),生成的二氧化碳的质量为______ ;根据化学方程式计算出原样品中四氧化三铁的质量______ ,从而计算原样品中单质铁的质量。
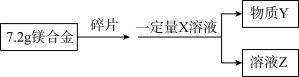
【方案3】实验装置如图二:______ 。
(6)若样品质量为16.0g,最终称量所得固体质量为16.4g,则样品中铁单质的质量为______ g。
【查阅资料】
a.四氧化三铁与稀盐酸反应,Fe3O4 + 8HCl=2FeCl3 + FeCl2 + 4H2O
b.Fe + 2FeCl3 = 3FeCl2
c.四氧化三铁与硫酸铜溶液不反应
d.碱石灰能吸收二氧化碳气体,不能吸收一氧化碳气体
【方案1】
(1)取一定量的黑色粉末,加入足量稀盐酸,准确测量生成的氢气体积,并计算出氢气的质量,再根据化学方程式(铁与稀盐酸反应)
(2)经仔细分析过程中可能发生的反应后,小新的同学认为该方案不合理,存在较大误差。你认为该方案一定会使得测量结果偏大还是偏小?
【方案2】实验装置如图一(装置气密性良好):
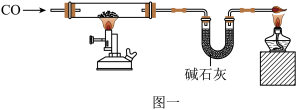
Ⅱ.连接好装置。缓缓通入CO,片刻后点燃酒精喷灯,待充分反应后,熄灭酒精喷灯,继续通入CO直至硬质玻璃管冷却,反应后测得U型管中碱石灰增加的质量为m3(不考虑空气中的成分对碱石灰质量的影响)。
(3)硬质玻璃管中反应的化学方程式为
(4)装入硬质玻璃管中样品的质量为(m2-m1),生成的二氧化碳的质量为
【方案3】实验装置如图二:
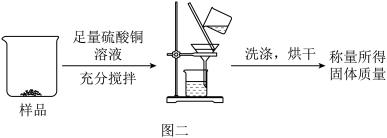
(6)若样品质量为16.0g,最终称量所得固体质量为16.4g,则样品中铁单质的质量为
23-24九年级上·江苏泰州·阶段练习
类题推荐
某小组称取4.90g氯酸钾和1.50g二氧化锰混合后进行制取氧气、验证氧气性质的实验,并在实验结束后回收得到纯净的二氧化锰。
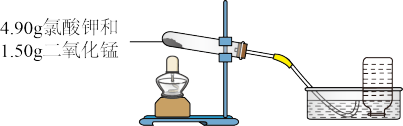
【氧气的制取及性质实验】
①生成氧气的化学方程式是___________ ;采用图中的收集方法,是因为氧气___________ 。
②将红热的木炭放入集满氧气的集气瓶中,观察到的现象是___________ 。
【回收二氧化锰】
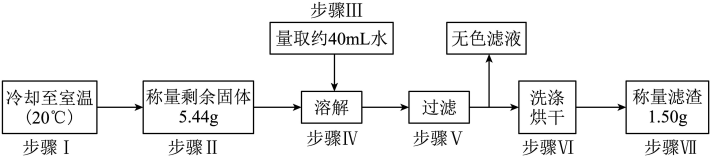
收集一定量氧气后结束实验,为回收剩余固体中的二氧化锰,进行如下实验。
③20℃时氯酸钾、氯化钾的溶解度数据见下表(假设溶液中两种物质的溶解度相互无影响)
请分析5.44g剩余固体的成分,并说明步骤III中水量约为40mL而不是30mL的原因___________ 。

【氧气的制取及性质实验】
①生成氧气的化学方程式是
②将红热的木炭放入集满氧气的集气瓶中,观察到的现象是
【回收二氧化锰】

收集一定量氧气后结束实验,为回收剩余固体中的二氧化锰,进行如下实验。
③20℃时氯酸钾、氯化钾的溶解度数据见下表(假设溶液中两种物质的溶解度相互无影响)
| 20℃的溶解度 | |
| 氯酸钾 | 7g/100g水 |
| 氯化钾 | 34g/100g水 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网