科学探究题 较易0.85 引用1 组卷31
世奇化学兴趣小组用加热氯酸钾和二氧化锰制取氧气,反应一段时间收集到所需的氧气后停止加热。大家对剩余固体的成分产生了兴趣并进行猜测和探究。
【猜想与假设】剩余固体的成分是什么?
(1)小诗猜想:KCl、MnO2
小琪猜想:KC1O3、KCl
小嘉猜想:KC1O3、MnO2
小悠猜想:________ 。
【讨论交流】
(2)小组同学交流后判断________ 猜想一定是错误的。
【实验活动】
(3)同学们为了验证猜想:取适量的剩余固体加入到试管中继续加热,然后将________ 观察到________ 的明显现象,证明小悠的猜想是正确的。
【拓展提升】
(4)小组同学根据以上结论将加热得到剩余固体的过程做出了部分图像,如图所示。若n曲线代表上述变化过程中的某种物质,请推测n曲线所代表的物质是________ 。(填物质符号)
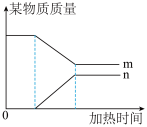
【总结与归纳】
(5)通过上述实验探究的过程,我们可以总结出:在分析反应后所得的剩余固体的成分时,我们既要考虑固体生成物,还要考虑________ 和________ 。
【猜想与假设】剩余固体的成分是什么?
(1)小诗猜想:KCl、MnO2
小琪猜想:KC1O3、KCl
小嘉猜想:KC1O3、MnO2
小悠猜想:
【讨论交流】
(2)小组同学交流后判断
【实验活动】
(3)同学们为了验证猜想:取适量的剩余固体加入到试管中继续加热,然后将
【拓展提升】
(4)小组同学根据以上结论将加热得到剩余固体的过程做出了部分图像,如图所示。若n曲线代表上述变化过程中的某种物质,请推测n曲线所代表的物质是

【总结与归纳】
(5)通过上述实验探究的过程,我们可以总结出:在分析反应后所得的剩余固体的成分时,我们既要考虑固体生成物,还要考虑
23-24八年级上·黑龙江哈尔滨·阶段练习
类题推荐
某同学阅读课外资料得知:实验室制取氧气除了用二氧化锰还可以用氧化铜等物质作催化剂,于是就对氧化铜产生了探究兴趣。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【查阅资料】氧化铜为黑色固体,不溶于水。
【设计实验】以生成等体积的氧气为标准,设计了下列三组实验(其他可能影响实验的因素均忽略)。
【进行实验】
(1)上述实验应测量的“待测数据”是收集等体积氧气所需的________ 。
(2)若实验②比实验①的“待测数据”更________ (填“长”或“短”),说明氧化铜能加快氯酸钾的分解速率。
(3)从实验②反应后的固体中,分离出氧化铜,若称得氧化铜质量仍为0.5g,说明氧化铜的________ 在化学反应前后保持不变。再将该氧化铜放入试管中,加入过氧化氢溶液,若观察到________ ,说明氧化铜的________ 在化学反应前后保持不变。
【预期结论】
(4)氧化铜________ (填“能”或“不能”)作氯酸钾分解的催化剂。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【查阅资料】氧化铜为黑色固体,不溶于水。
【设计实验】以生成等体积的氧气为标准,设计了下列三组实验(其他可能影响实验的因素均忽略)。
【进行实验】
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | ||
| ② | 1.2g | 氧化铜0.5g | |
| ③ | 1.2g | 二氧化锰0.5g |
(2)若实验②比实验①的“待测数据”更
(3)从实验②反应后的固体中,分离出氧化铜,若称得氧化铜质量仍为0.5g,说明氧化铜的
【预期结论】
(4)氧化铜
某化学兴趣小组阅读课外资料得知,双氧水分解除了二氧化锰作催化剂,还可以用氧化铜等物质作催化剂,于是对氧气制取产生了探究兴趣。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】以生成等体积的氧气为标准,设计了下列三组实验:(其他可能影响实验的因素均忽略)
(1)上述实验测量的“待测数据”是______ ;
(2)若实验②比实验①的“待测数据”更______ (填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率。
(3)对实验②反应后的固体加水溶解、过滤、洗涤、干燥,用______ 称量得到0.5g黑色固体粉末,这是为了证明氧化铜的______ 在反应前后没有改变。
【预期结论】氧化铜还能作氯酸钾分解的催化剂。
【评价设计】你认为设计实验③和实验②对比的目的是______ ;上述实验探究不能证明氧化铜能作氯酸钾分解的催化剂的理由是______ 。
【实验拓展】大家从课外资料上还获得下列信息:氧化铁、硫酸铜、猪肝、马铃薯等也可以作过氧化氢分解的催化剂。下列有关催化剂的说法正确______ 。
A.MnO2只能作为过氧化氢溶液分解的催化
B.同一个反应可能有多种催化剂
C.催化剂一定能加快反应速率
D.没有催化剂化学反应不能发生
E.对很多工业反应,加入催化剂能起到增加生成物的质量的效果
F.用作催化剂的物质不可能是其它反应的反应物或生成物
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】以生成等体积的氧气为标准,设计了下列三组实验:(其他可能影响实验的因素均忽略)
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | ||
| ② | 1.2g | CuO0.5g | |
| ③ | 1.2g | MnO20.5g |
(1)上述实验测量的“待测数据”是
(2)若实验②比实验①的“待测数据”更
(3)对实验②反应后的固体加水溶解、过滤、洗涤、干燥,用
【预期结论】氧化铜还能作氯酸钾分解的催化剂。
【评价设计】你认为设计实验③和实验②对比的目的是
【实验拓展】大家从课外资料上还获得下列信息:氧化铁、硫酸铜、猪肝、马铃薯等也可以作过氧化氢分解的催化剂。下列有关催化剂的说法正确
A.MnO2只能作为过氧化氢溶液分解的催化
B.同一个反应可能有多种催化剂
C.催化剂一定能加快反应速率
D.没有催化剂化学反应不能发生
E.对很多工业反应,加入催化剂能起到增加生成物的质量的效果
F.用作催化剂的物质不可能是其它反应的反应物或生成物
小宇通过探究发现,氯酸钾与氧化铜(CuO)或氧化铁(Fe2O3)混合加热,也能较快产生氧气,于是进行如下探究:
【查阅资料】
氯酸钾的熔点为 356℃,常温下稳定,在400℃以上则分解产生氧气。酒精灯加热温度为400℃~500℃。
【提出猜想】
除MnO2、CuO外,Fe2O3也可以作氯酸钾分解的催化剂。
【完成实验】
按如表进行实验并测定分解温度。(分解温度越低,催化效果越好)
【分析数据,得出结论】
(1)实验4中x的值应为______ ,由实验______ 与实验4相比,证明猜想合理。
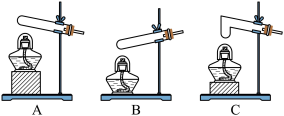
(2)小宇从如图中选择该实验的最佳发生装置是______ (填字母),该装置的优点是______ 。
(3)实验3反应的化学方程式为:______ 。
【查阅资料】
氯酸钾的熔点为 356℃,常温下稳定,在400℃以上则分解产生氧气。酒精灯加热温度为400℃~500℃。
【提出猜想】
除MnO2、CuO外,Fe2O3也可以作氯酸钾分解的催化剂。
【完成实验】
按如表进行实验并测定分解温度。(分解温度越低,催化效果越好)
| 实验编号 | 实验药品 | 分解温度 |
| 1 | 3.0g氯酸钾 | 460℃ |
| 2 | 3.0g氯酸钾和0.5g二氧化锰 | 248℃ |
| 3 | 3.0g氯酸钾和0.5g氧化铜 | 267℃ |
| 4 | 3.0g氯酸钾和xg氧化铁 | 290℃ |

【分析数据,得出结论】
(1)实验4中x的值应为
(2)小宇从如图中选择该实验的最佳发生装置是
(3)实验3反应的化学方程式为:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


