科学探究题 适中0.65 引用1 组卷19
六十九中学实验小组在实验室用加热氯酸钾和二氧化锰制取氧气,反应一段时间收集到所需的氧气后停止加热,小组成员对其剩余固体的成分产生兴趣并进行探究。
【猜想与假设】剩余固体的成分是什么?
小宣认为是:KCl、MnO2
西西认为是:MnO2
(1)你的猜想是:______ (填化学符号)
(2)【分析与判断】以上猜想中,______ 的猜想是错误的,请用表达式解释理由:______ 。
(3)【活动与探究】为了验证猜想,小组同学设计的实验方法是取少量剩余固体于试管中,加热,再伸入______ 的木条。小组同学观察到的现象是______ ,则证明你的猜想是正确的。
(4)【反思与收获】小组同学通过对此次实验的分析共同总结出:一般来说,在验证反应后的剩余固体成分时,______ 无需验证一定存在,只需验证______ 即可。
【猜想与假设】剩余固体的成分是什么?
小宣认为是:KCl、MnO2
西西认为是:MnO2
(1)你的猜想是:
(2)【分析与判断】以上猜想中,
(3)【活动与探究】为了验证猜想,小组同学设计的实验方法是取少量剩余固体于试管中,加热,再伸入
(4)【反思与收获】小组同学通过对此次实验的分析共同总结出:一般来说,在验证反应后的剩余固体成分时,
23-24八年级上·黑龙江哈尔滨·期中
类题推荐
化学兴趣小组对氯酸钾制取氧气进行了探究。
Ⅰ.探究 分解反应中不同催化剂的催化效果
分解反应中不同催化剂的催化效果
兴趣小组取5份氯酸钾固体,每份2g。分别加入相同质量的不同种类催化剂,加热反应,测定收集到 所用的时间见下表。
所用的时间见下表。
(1)实验①的目的是__________ 。
(2)实验②中发生反应的化学方程式为__________ 。
(3)“60目”和“30目”指两种颗粒大小不同的粉末(目数越高,颗粒越小)。由实验③、④可得出的结论是__________ 。
(4)对比实验①与实验⑤,得出的结论是__________ 。
Ⅱ.探究 与
与 反应的最佳质量比兴趣小组另取10份氯酸钾固体,每份2g,分别加入不同质量的二氧化锰,加热反应,收集到100mL氧气所用的时间与固体质量比的关系如图所示。
反应的最佳质量比兴趣小组另取10份氯酸钾固体,每份2g,分别加入不同质量的二氧化锰,加热反应,收集到100mL氧气所用的时间与固体质量比的关系如图所示。 的最佳质量比为
的最佳质量比为__________ 。
(6) 质量比低于最佳比时,随着
质量比低于最佳比时,随着 质量增多,反应越快的原因可能是
质量增多,反应越快的原因可能是__________ 。
(7)在催化剂的用量上,你对催化剂的新认识是__________ 。
(8)每次实验结束后,拆装置时总能闻到刺激性气味的氯气,将加热后剩余固体中的 分离并称量其质量,发现总小于加热前的
分离并称量其质量,发现总小于加热前的 质量。查阅资料后发现,一般认为
质量。查阅资料后发现,一般认为 与
与 混合物的反应过程如下:
混合物的反应过程如下:
第①步:
第②步:
第③步:
反应后剩余的 质量小于反应加入
质量小于反应加入 的质量,你认为可能的原因是
的质量,你认为可能的原因是__________ 。
Ⅰ.探究
兴趣小组取5份氯酸钾固体,每份2g。分别加入相同质量的不同种类催化剂,加热反应,测定收集到
| 实验序号 | ① | ② | ③ | ④ | ⑤ |
| 催化剂种类 | —— | KCl | |||
| 所用时间(s) | 170 | 49 | 60 | 117 | 152 |
(1)实验①的目的是
(2)实验②中发生反应的化学方程式为
(3)“60目”和“30目”指两种颗粒大小不同的粉末(目数越高,颗粒越小)。由实验③、④可得出的结论是
(4)对比实验①与实验⑤,得出的结论是
Ⅱ.探究

(6)
(7)在催化剂的用量上,你对催化剂的新认识是
(8)每次实验结束后,拆装置时总能闻到刺激性气味的氯气,将加热后剩余固体中的
第①步:
第②步:
第③步:
反应后剩余的
小雨阅读课外资料得知:双氧水分解除了用二氧化锰,还可用氧化铜等物质作催化剂,于是他对黑色的氧化铜产生了探究兴趣。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
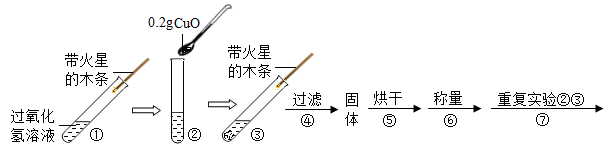
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
(1)写出氯酸钾和二氧化锰制取氧气的化学符号表达式________ 。上述实验应测量的“待测数据”是_________ 。
(2)若实验②比实验①的“待测数据”更________ (填“大”或“小),说明氧化铜能加快氯酸钾的分解速率。
(3)将实验②反应后的固体加水溶解、过滤、洗涤、干燥, 若称量得到0. 5g黑色粉末,说明黑色粉末的________ 在反应前后保持不变。
(4)再将该黑色粉末放入试管中向其中面入适量的双氧水,观察到有大量气泡产生,说明黑色粉末的_________ 在反应前后保持不变
【预期结论】氧化铜能作氯酸钾分解的催化剂。
【评价设计】你认为小雨设计实验③和实验②对比的目的是_______ 。
【拓展延伸】以下是某研究小组探究影响化学反应快慢的一些因素的相关数据:
(5)通过实验①和②对比可知,化学反应快慢与_______ 有关。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | ||
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
(2)若实验②比实验①的“待测数据”更
(3)将实验②反应后的固体加水溶解、过滤、洗涤、干燥, 若称量得到0. 5g黑色粉末,说明黑色粉末的
(4)再将该黑色粉末放入试管中向其中面入适量的双氧水,观察到有大量气泡产生,说明黑色粉末的
【预期结论】氧化铜能作氯酸钾分解的催化剂。
【评价设计】你认为小雨设计实验③和实验②对比的目的是
【拓展延伸】以下是某研究小组探究影响化学反应快慢的一些因素的相关数据:
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰用量/g | 氧气体积/mL | 反应所需时间/s |
| ① | 5 | 12 | 20 | 0.2 | 125 | 11 |
| ② | 30 | 12 | 20 | 0.2 | 125 | 2 |
| ③ | 30 | 12 | 20 | 125 | 296 | |
| ④ | 30 | 12 | 90 | 125 | 82 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网