科学探究题 较难0.4 引用6 组卷597
某同学在学习木炭和氧化铜反应的知识后,产生了疑问:木炭与氧化铜反应生成的气体有哪些?同学们带着疑问进行了下列探究:
【提出猜想】
(1)猜想一:只有______ ; 猜想二:只有CO; 猜想三:既有CO2又有CO。
【查阅资料】
a.浸有磷钼酸溶液的氯化钯试纸遇二氧化碳无变化,但遇到微量一氧化碳会立即变成蓝色。
b.二氧化碳能使澄清石灰水变浑浊
【实验步骤】
连接好实验装置,并进行实验,装置如图所示(夹持仪器已省):
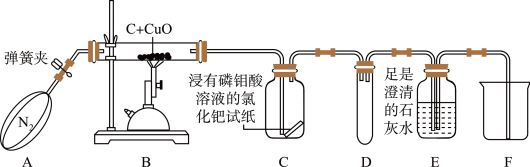
步骤一:打开弹簧夹,先通一会儿纯净干燥的氮气;
步骤二:关闭弹簧夹,点燃酒精喷灯对硬质玻璃管加热。
步骤三:实验结束后,拆洗装置和仪器。
【实验分析】
(2)若观察到氯化钯试纸______ ,澄清石灰水变浑浊,则猜想一成立。
(3)若观察到______ ,则猜想三成立。
(4)若猜想一成立则B中发生反应的方程式:______ 。
【实验反思】
(5)该实验开始前通一会儿N2的目的是______ 。实验过程中硬质玻璃管中的现象是______ 。
(6)实验结束时,熄灭酒精喷灯的同时停止通入N2,有同学认为在实验过程中装置D没有作用,可以去除,你认为是否可行?______ (填“可行”或“不可行”),请说明理由______ 。
【提出猜想】
(1)猜想一:只有
【查阅资料】
a.浸有磷钼酸溶液的氯化钯试纸遇二氧化碳无变化,但遇到微量一氧化碳会立即变成蓝色。
b.二氧化碳能使澄清石灰水变浑浊
【实验步骤】
连接好实验装置,并进行实验,装置如图所示(夹持仪器已省):

步骤一:打开弹簧夹,先通一会儿纯净干燥的氮气;
步骤二:关闭弹簧夹,点燃酒精喷灯对硬质玻璃管加热。
步骤三:实验结束后,拆洗装置和仪器。
【实验分析】
(2)若观察到氯化钯试纸
(3)若观察到
(4)若猜想一成立则B中发生反应的方程式:
【实验反思】
(5)该实验开始前通一会儿N2的目的是
(6)实验结束时,熄灭酒精喷灯的同时停止通入N2,有同学认为在实验过程中装置D没有作用,可以去除,你认为是否可行?
23-24九年级上·吉林长春·阶段练习
类题推荐
反应物的质量比不同可能会影响生成物的种类,为探究碳还原氧化铜生成的气体种类,设计了下列实验(所有反应均充分进行,浓硫酸用以吸收水蒸气):
【提出问题】:碳还原氧化铜生成的气体是什么?
【作出猜想】:猜想①:CO 猜想②:CO2 猜想③:CO2和CO
【实验设计】:装置图如图
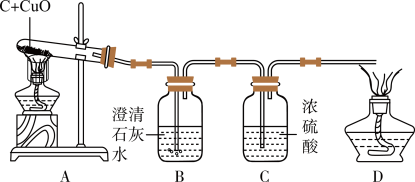
方案一:从定性观察角度判断:
①实验时,A中出现_________________ 的现象。
②若猜想①成立,B、D处的实验现象是:
B________________ ,D_________________ 。
方案二:从定量计算角度判断:
测定表格中的四个数据:
③若猜想②成立,则(m4-m3)_____ (m1-m2)(选填“>”、“<”、“=”)。此时A中发生反应的化学方程式为_____________________________ 。
④若猜想③成立,且8gCuO全部参与反应,则碳的物质的量(n)的取值范围是____ <n<_____ 。
【提出问题】:碳还原氧化铜生成的气体是什么?
【作出猜想】:猜想①:CO 猜想②:CO2 猜想③:CO2和CO
【实验设计】:装置图如图

方案一:从定性观察角度判断:
①实验时,A中出现
②若猜想①成立,B、D处的实验现象是:
B
方案二:从定量计算角度判断:
测定表格中的四个数据:
| 反应前的质量 | 反应后的质量 | |
| A(试管+固体) | m1 | m2 |
| B+C(广口瓶+溶液) | m3 | m4 |
④若猜想③成立,且8gCuO全部参与反应,则碳的物质的量(n)的取值范围是
某兴趣小组同学对碱式碳酸铜的分解产物进行探究。
Ⅰ【查阅资料】
①碱石灰是常见的干燥剂,可吸收水和二氧化碳。
②浓硫酸也是常见的干燥剂,能吸收水,但是不吸收二氧化碳。
【设计实验】该小组同学设计了如图所示的实验装置,假设每一步反应和吸收均进行完全。

【进行实验】取一定量的碱式碳酸铜固体进行实验,步骤如下:
①连接好装置并检查气密性
②装入药品,打开活塞K,通入一段时间空气
③分别称量装置C、D的质量;
④关闭活塞K,点燃酒精灯,使碱式碳酸铜固体完全分解;
⑤停止加热,同时打开活塞K,通入空气至恢复到室温;
⑥再次分别称量装置C、D的质量。
【实验分析】
(1)装置A的作用为_______ ,装置D的作用为_______ 。
(2)装置B内剩余固体为_______ ,反应中生成水的质量为_______ 。
Ⅱ小组同学继续探究装置B内剩余固体的性质,查阅资料发现剩余固体可以和焦炭在高温下发生反应,得到一种紫红色金属单质和气体产物。
【猜想与假设】
小组同学猜想紫红色金属单质为铜,气体产物可能为含碳元素的氧化物。
猜想1:产物为铜和一氧化碳;
猜想2:产物为铜和二氧化碳;
猜想3:产物为(3)_______ 。
【设计方案】
两人查找了资料:CO的特征反应是CO能使某种氯化钯的黄色混合液变蓝;CO有毒且具有可燃性。

【反思与评价】
④实验结束时,为了防止铜被氧化,必须先停止加热,待铜冷却后再将试管口的胶塞取下,因此,若没有B安全瓶,可能导致的后果是_______ 。
⑤根据实验结论,从环保角度考滤,上述装置C后应采取的措施是_______ 。
Ⅰ【查阅资料】
①碱石灰是常见的干燥剂,可吸收水和二氧化碳。
②浓硫酸也是常见的干燥剂,能吸收水,但是不吸收二氧化碳。
【设计实验】该小组同学设计了如图所示的实验装置,假设每一步反应和吸收均进行完全。

【进行实验】取一定量的碱式碳酸铜固体进行实验,步骤如下:
①连接好装置并检查气密性
②装入药品,打开活塞K,通入一段时间空气
③分别称量装置C、D的质量;
④关闭活塞K,点燃酒精灯,使碱式碳酸铜固体完全分解;
⑤停止加热,同时打开活塞K,通入空气至恢复到室温;
⑥再次分别称量装置C、D的质量。
| 装置C的质量/g | 装置D的质量/g | |
| 步骤③ | m | n |
| 步骤⑥ | x | y |
(1)装置A的作用为
(2)装置B内剩余固体为
Ⅱ小组同学继续探究装置B内剩余固体的性质,查阅资料发现剩余固体可以和焦炭在高温下发生反应,得到一种紫红色金属单质和气体产物。
【猜想与假设】
小组同学猜想紫红色金属单质为铜,气体产物可能为含碳元素的氧化物。
猜想1:产物为铜和一氧化碳;
猜想2:产物为铜和二氧化碳;
猜想3:产物为(3)
【设计方案】
两人查找了资料:CO的特征反应是CO能使某种氯化钯的黄色混合液变蓝;CO有毒且具有可燃性。

| 实验现象 | 实验结论 |
| ①A中固体由黑色变红色 ②B中黄色试纸变篮 ③C中 | ①由Cu生成 ②有 ③有CO2生成 |
④实验结束时,为了防止铜被氧化,必须先停止加热,待铜冷却后再将试管口的胶塞取下,因此,若没有B安全瓶,可能导致的后果是
⑤根据实验结论,从环保角度考滤,上述装置C后应采取的措施是
铜及其化合物的冶炼与人类生活、社会发展有密切联系。
【查阅资料】
①木炭能在较高温度环境中将氧化铜中的氧元素夺去,生成单质铜
②酒精灯防风罩能将酒精灯火焰温度提升至 600~800℃
③铜的熔点为 1083℃
【装置分析】
①该实验并未采用略向下倾斜试管的加热方法,原因可能是___________ 。
A.使火焰更好包裹住药品部位,提高反应温度
B.防止生成的气体冲散药品,降低实验成功率
C.过程中会生成液态的铜,且防止石灰水倒吸
【实验过程】
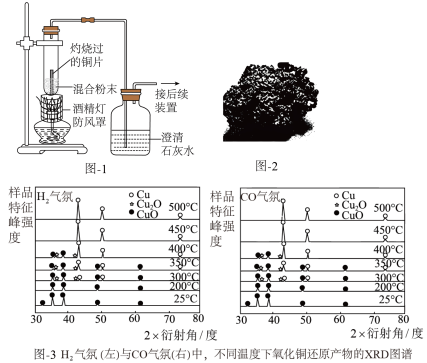
实验:取 0.1 g 木炭粉与一定量的氧化铜粉末按下表所示比例充分混合,在粉末堆中插入一块灼烧过的铜片,进行实验。
②从表中可知,木炭还原氧化铜的最佳质量比是___________ 。
③无需再进行木炭粉与氧化铜粉末质量比为 1: 14 的实验,原因是___________ 。
④取出铜片观察,发现埋入粉末的部分变红,有金属光泽,上方铜片也变为亮红色,右侧澄清石灰水变浑浊,由此推测反应中产生的气体一定有___________ 。
⑤某同学取 8.0 g CuO 固体粉末与一定量木炭以最佳质量比混合,若 CuO 完全转化为 Cu, 理论上预计能得到 Cu 的质量为___________ 。
⑥试管底部的亮红色固体呈“海绵状”,如图-2 所示,实验得到“海绵铜”而非块状铜的原因是___________ 。
(2)分别在 H2与 CO 气氛下,还原氧化铜样品。对反应后的样品进行 X 射线衍射,得到的XRD 图谱结果如图-3 所示。XRD 图谱中的峰值可以表征某物种的存在。结合图像说明,能否采用热还原的方法直接制得纯净的 Cu2O 产品,_________ (填“用H2能”或“CO 能”或“都能”或“都不能”),为什么_________ 。
【查阅资料】
①木炭能在较高温度环境中将氧化铜中的氧元素夺去,生成单质铜
②酒精灯防风罩能将酒精灯火焰温度提升至 600~800℃
③铜的熔点为 1083℃
【装置分析】
①该实验并未采用略向下倾斜试管的加热方法,原因可能是
A.使火焰更好包裹住药品部位,提高反应温度
B.防止生成的气体冲散药品,降低实验成功率
C.过程中会生成液态的铜,且防止石灰水倒吸
【实验过程】
实验:取 0.1 g 木炭粉与一定量的氧化铜粉末按下表所示比例充分混合,在粉末堆中插入一块灼烧过的铜片,进行实验。
| 序号 | 木炭粉与氧化铜粉末混合质量比 | 充分反应后试管底部固体的颜色 | |
| 1) | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
| 2) | 1:10 | 混有很少量黑色物质 | |
| 3) | 1:11 | 混有极少量黑色物质 | |
| 4) | 1:12 | 无黑色物质 | |
| 5) | 1:13 | 混有少量黑色物资 | |
③无需再进行木炭粉与氧化铜粉末质量比为 1: 14 的实验,原因是
④取出铜片观察,发现埋入粉末的部分变红,有金属光泽,上方铜片也变为亮红色,右侧澄清石灰水变浑浊,由此推测反应中产生的气体一定有
⑤某同学取 8.0 g CuO 固体粉末与一定量木炭以最佳质量比混合,若 CuO 完全转化为 Cu, 理论上预计能得到 Cu 的质量为
⑥试管底部的亮红色固体呈“海绵状”,如图-2 所示,实验得到“海绵铜”而非块状铜的原因是
(2)分别在 H2与 CO 气氛下,还原氧化铜样品。对反应后的样品进行 X 射线衍射,得到的XRD 图谱结果如图-3 所示。XRD 图谱中的峰值可以表征某物种的存在。结合图像说明,能否采用热还原的方法直接制得纯净的 Cu2O 产品,
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


