科学探究题 较难0.4 引用1 组卷40
某兴趣小组同学对过氧化氢分解的实验进行如下探究。
实验1:探究过氧化氢溶液浓度、温度对反应速率的影响
【实验方案】在一定温度下,向相同质量的过氧化氢溶液中加入相同质量的二氧化锰(MnO2)粉末,测量收集150mL氧气(O2)所需的时间。
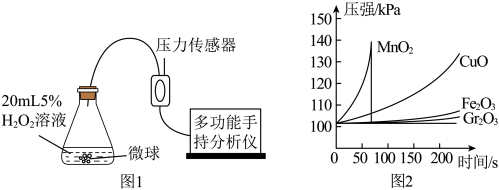
实验2:依据下图1装置进行实验(部分仪器略去),探究催化剂种类对反应速率的影响。
【实验方案】取用相同粒数的二氧化锰(MnO2)、氧化铜(CuO)、氧化铁(Fe2O3)、氧化铬(Gr2O3)四种催化剂微球(质量相等、表面积相同),分别进行实验,锥形瓶内压强随时间的变化如图2所示。
【解释与结论】
(1)实验1中反应的文字表达式是_______ 。二氧化锰在反应前后质量和_______ 没有发生改变。
(2)为了达到实验1的目的,补全实验方案。
①若a与b不相等,若a=15;则b=____ 。②若a与b相等,则设计实验I、III的目的是___ 。
(3)实验2中使用相同粒数催化剂微球的原因是_______ 。
(4)通过对实验2数据的分析,可得出的结论是_______ 。
【反思与评价】
(5)为了完成实验1,该兴趣小组收集氧气的装置可以选用下图中的_______。(可多选)
(6)实验1是通过测量收集等体积氧气(O2)所需时间来比较过氧化氢(H2O2)溶液分解的反应速率,还可以通过测量_______ 来比较过氧化氢(H2O2)溶液分解的反应速率。
(7)该兴趣小组成员通过网上查阅资料获悉:除二氧化锰、氧化铜、氧化铁、氧化铬外,硫酸铜、猪肝、马铃薯等也可以作为过氧化氢分解的催化剂。下列有关催化剂的说法正确的是_______
实验1:探究过氧化氢溶液浓度、温度对反应速率的影响
【实验方案】在一定温度下,向相同质量的过氧化氢溶液中加入相同质量的二氧化锰(MnO2)粉末,测量收集150mL氧气(O2)所需的时间。
| 实验序号 | 过氧化氢溶液的浓度/% | 温度/℃ | 时间/s |
| Ⅰ | 30 | 20 | 待测 |
| Ⅱ | 15 | 30 | 特测 |
| Ⅲ | a | b | 待测 |
【实验方案】取用相同粒数的二氧化锰(MnO2)、氧化铜(CuO)、氧化铁(Fe2O3)、氧化铬(Gr2O3)四种催化剂微球(质量相等、表面积相同),分别进行实验,锥形瓶内压强随时间的变化如图2所示。

【解释与结论】
(1)实验1中反应的文字表达式是
(2)为了达到实验1的目的,补全实验方案。
①若a与b不相等,若a=15;则b=
(3)实验2中使用相同粒数催化剂微球的原因是
(4)通过对实验2数据的分析,可得出的结论是
【反思与评价】
(5)为了完成实验1,该兴趣小组收集氧气的装置可以选用下图中的_______。(可多选)
A.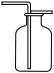 | B.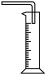 | C. | D.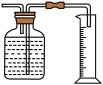 |
(7)该兴趣小组成员通过网上查阅资料获悉:除二氧化锰、氧化铜、氧化铁、氧化铬外,硫酸铜、猪肝、马铃薯等也可以作为过氧化氢分解的催化剂。下列有关催化剂的说法正确的是_______
| A.二氧化锰可作任何反应的催化剂 | B.同一个反应可能有多种催化剂 |
| C.催化剂一定能加快化学反应速率 | D.没有催化剂,化学反应不能发生 |
| E.在很多工业反应中,加入催化剂能起到增加生成物质量的效果 | |
23-24九年级上·安徽·阶段练习
类题推荐
小丽同学在实验室用MnO2和H2O2制取氧气,不小心滴加了几滴H2SO4到溶液中,发现溶液中黑色物质逐渐消失,他们对这种现象展开了探究。
【提出问题】是什么原因导致黑色的二氧化锰逐渐消失?
【提出猜想】猜想1:MnO2和H2O2反应
猜想2:MnO2和H2SO4反应
猜想3:___________ 。
【交流与反思1】写出实验室用MnO2和H2O2制取氧气的化学方程式:___________ 。小红同学认为猜想___________ 是不可能的,不需要实验验证,大家同意了他的看法。
【实验探究】他们设计了如下实验验证猜想2.
【交流与反思2】小红对这样的实验设计提出了异议,她认为题干中导致黑色物质逐渐消失的实验是在溶液中进行的,而上述实验中应该加入适量的___________ ,和题干中的实验作为对比实验,才更有说服力。
【实验拓展】为了进一步研究黑色物质消失的原因,他们设计了如下对比实验。
(1)上述实验中,滴加Na2SO4的目的是:___________ 。
(2)从上述实验现象可以得出使黑色物质逐渐消失的原因是在溶液中加入了___________ 。
(3)你认为能使黑色物质逐渐消失,还可能和___________ 有关。
【提出问题】是什么原因导致黑色的二氧化锰逐渐消失?
【提出猜想】猜想1:MnO2和H2O2反应
猜想2:MnO2和H2SO4反应
猜想3:
【交流与反思1】写出实验室用MnO2和H2O2制取氧气的化学方程式:
【实验探究】他们设计了如下实验验证猜想2.
| 实验步骤 | 实验现象 | 实验结论 |
| 取5gMnO2加入试管中,滴加几滴H2SO4,振荡,观察现象。 | 无现象 |
【交流与反思2】小红对这样的实验设计提出了异议,她认为题干中导致黑色物质逐渐消失的实验是在溶液中进行的,而上述实验中应该加入适量的
【实验拓展】为了进一步研究黑色物质消失的原因,他们设计了如下对比实验。
| 试管序号 | 药品 | 实验现象 |
| 1 | MnO2+4滴H2SO4+H2O2 | 黑色物质逐渐溶解,有无色气体产生 |
| 2 | MnO2+4滴Na2SO4+H2O2 | 黑色物质没有溶解,有无色气体产生 |
| 3 | MnO2+4滴HCl+H2O2 | 黑色物质逐渐溶解,有无色气体产生 |
(1)上述实验中,滴加Na2SO4的目的是:
(2)从上述实验现象可以得出使黑色物质逐渐消失的原因是在溶液中加入了
(3)你认为能使黑色物质逐渐消失,还可能和
某兴趣小组在学习了双氧水分解制氧气的实验后,知道催化剂(MnO2)能改变化学反应速率。到底还有哪些因素与化学反应速率有关呢?
【小组讨论】小明猜测:化学反应速率与反应物的质量分数有关
小刚猜测:化学反应速率与反应温度有关
【设计实验】他们设计并进行了以下4次实验
(1)①和④实验证明小刚的观点是正确的,_______ 实验证明小明的观点是正确的(填字母)
A ①和② B ③和④ C ②和③ D ①和③
(2)由以上实验还能得出什么结论:_______ 。
(3)【交流拓展】他们猜测:催化剂(MnO2)是一种氧化物,那么氧化铁(Fe2O3)、氧化铜(CuO)是否也有这样的催化作用呢?设计了如图的实验。

如果实验证明氧化铁、氧化铜均有催化作用,那么,小组成员应观察到的实验现象是_______ 。
(4)小明认为,要证明氧化铁、氧化铜是本实验的催化剂,还需要有氧化铁、氧化铜在实验前后____ 和____ 都没有改变的证据。
(5)小刚猜测氧化铁、氧化铜可能对用氯酸钾制氧气也能起催化作用,并进行相关实验,获得实验数据如下表,本实验中,三种催化剂的催化能力由强到弱的顺序是_______ 。
【小组讨论】小明猜测:化学反应速率与反应物的质量分数有关
小刚猜测:化学反应速率与反应温度有关
【设计实验】他们设计并进行了以下4次实验
| 实验次数 | H2O2溶液质量分数% | H2O2溶液用量/毫升 | 催化剂(MnO2)用量/克 | 反应温度/℃ | 收集气体体积/毫升 | 所需时间/秒 |
| ① | 30 | 5 | 0 | 85 | 2 | 3.8 |
| ② | 15 | 2 | 0.1 | 20 | 2 | 2.8 |
| ③ | 5 | 2 | 0.1 | 20 | 2 | 7.4 |
| ④ | 30 | 5 | 0 | 55 | 2 | 10.5 |
A ①和② B ③和④ C ②和③ D ①和③
(2)由以上实验还能得出什么结论:
(3)【交流拓展】他们猜测:催化剂(MnO2)是一种氧化物,那么氧化铁(Fe2O3)、氧化铜(CuO)是否也有这样的催化作用呢?设计了如图的实验。

如果实验证明氧化铁、氧化铜均有催化作用,那么,小组成员应观察到的实验现象是
(4)小明认为,要证明氧化铁、氧化铜是本实验的催化剂,还需要有氧化铁、氧化铜在实验前后
(5)小刚猜测氧化铁、氧化铜可能对用氯酸钾制氧气也能起催化作用,并进行相关实验,获得实验数据如下表,本实验中,三种催化剂的催化能力由强到弱的顺序是
| 实验组别 | KClO3质量克) | 催化剂 | 产生气体质量(克) | 耗时(秒) | |
| 化学式 | 质量(克) | ||||
| 1 | 0.60 | -- | -- | 0.014 | 480 |
| 2 | 0.60 | MnO2 | 0.20 | 0.096 | 36.5 |
| 3 | 0.60 | CuO | 0.20 | 0.096 | 79.5 |
| 4 | 0.60 | Fe2O3 | 0.20 | 0.096 | 34.7 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


