综合应用题 较难0.4 引用1 组卷143
扎实做好“碳达峰”“碳中和”各项工作,体现了我国主动承担应对气候变化的国际责任、推动构建人类命运共同体的责任担当。请回答:
(1)“碳达峰”“碳中和”中的“碳”指的是_____ (填化学式)。
(2)“碳”减排:使用氢能源汽车可以有效减少二氧化碳的排放。单质硼(B)可与物质X反应制取氢气,化学方程式为: ,则X的化学式为
,则X的化学式为_____ 。
(3)“碳捕捉和封存”技术是实现“碳中和”的重要途径。重庆合川实验基地通过如图技术将 压入地下实现
压入地下实现 的封存。这里的
的封存。这里的 捕集是一个
捕集是一个_____ (填“物理”或“化学”)过程。此过程中 分子间隔
分子间隔_____ 。
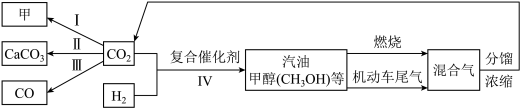
(4)转化法是实现“碳中和”的措施之一,下图为根据初中化学有关知识、结合有关资料,得到的碳的转化关系。
①若甲为单质,自然界通过光合作用完成转化I,则甲为_____ 。
②转化Ⅱ反应的化学方程式为_____ 。
③二氧化碳与碳反应,完成转化Ⅲ,反应的化学方程式为_____ 。
④转化Ⅳ是将 和
和 在催化剂的作用下转化成甲醇
在催化剂的作用下转化成甲醇 和水,是目前研究的热点,该反应的化学方程式为
和水,是目前研究的热点,该反应的化学方程式为_____ 。
(5)在日常生活中,你如何践行“低碳生活”理念_____ (写一条即可)。
(1)“碳达峰”“碳中和”中的“碳”指的是
(2)“碳”减排:使用氢能源汽车可以有效减少二氧化碳的排放。单质硼(B)可与物质X反应制取氢气,化学方程式为:
(3)“碳捕捉和封存”技术是实现“碳中和”的重要途径。重庆合川实验基地通过如图技术将

(4)转化法是实现“碳中和”的措施之一,下图为根据初中化学有关知识、结合有关资料,得到的碳的转化关系。

①若甲为单质,自然界通过光合作用完成转化I,则甲为
②转化Ⅱ反应的化学方程式为
③二氧化碳与碳反应,完成转化Ⅲ,反应的化学方程式为
④转化Ⅳ是将
(5)在日常生活中,你如何践行“低碳生活”理念
22-23八年级下·山东济宁·期末
类题推荐
北京2022冬奥会秉持着“绿色冬奥”的理念,把碳达峰、碳中和纳入了生态文明建设的整体布局,采取了低碳场馆、低碳能源、低碳交通等多项科技助推的措施,真正让“绿色”成为这场冬奥会的鲜明底色。
(1)为保护人类赖以生存的地球,我们应采取有效措施以防止大气中二氧化碳含量的大量增加,以下建议中行之有效的措施是 (填序号)。
(2)为减缓温室效应,有科学家猜想将空气中的二氧化碳输送到冰冷的深海中贮藏,但也有科学家担心这样做会增加海水的酸度,导致海洋生物死亡,二氧化碳使海水酸度增加的原因是____ (用化学方程式表示)。
(3)使用膜分离法可以从空气中分离出二氧化碳气体,该过程发生的是____ (填“物理”或“化学”)变化。
(4)实验室常用大理石和稀盐酸制取二氧化碳。某化学兴趣小组现取25g含碳酸钙的大理石于烧杯中,缓慢加入稀盐酸(大理石中的杂质不溶于水,也不与稀盐酸反应),剩余固体质量与加入稀盐酸的质量关系如图所示。请根据要求回答问题:
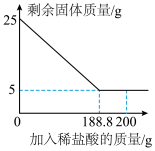
①参加反应的碳酸钙质量是____ g。
②计算恰好完全反应时,所得不饱和溶液的质量_____ (计算结果精确到0.1g)。
(1)为保护人类赖以生存的地球,我们应采取有效措施以防止大气中二氧化碳含量的大量增加,以下建议中行之有效的措施是 (填序号)。
| A.开发太阳能、风能、地热能、潮汐能等新能源 |
| B.禁止使用煤、石油、天然气等矿物燃料 |
| C.大量植树造林绿化环境,禁止乱砍滥伐 |
(2)为减缓温室效应,有科学家猜想将空气中的二氧化碳输送到冰冷的深海中贮藏,但也有科学家担心这样做会增加海水的酸度,导致海洋生物死亡,二氧化碳使海水酸度增加的原因是
(3)使用膜分离法可以从空气中分离出二氧化碳气体,该过程发生的是
(4)实验室常用大理石和稀盐酸制取二氧化碳。某化学兴趣小组现取25g含碳酸钙的大理石于烧杯中,缓慢加入稀盐酸(大理石中的杂质不溶于水,也不与稀盐酸反应),剩余固体质量与加入稀盐酸的质量关系如图所示。请根据要求回答问题:

①参加反应的碳酸钙质量是
②计算恰好完全反应时,所得不饱和溶液的质量
氧气是生产、生活中重要的物质。回答下列问题:
(1)工业上利用分离液态空气的方法制取氧气,是_______ 变化(填“物理”或“化学”)。
(2)下列关于氧气的说法错误的是______(填序号)。
(3)氧循环是自然界中的重要循环,下列①~④中消耗氧气的是______(填序号)。
①食物腐败 ②煤炭燃烧 ③植物光合作用 ④人的呼吸
(4)如图所示“氧气”要穿过迷宫,从进口顺利地走到出口,途中遇到不反应的物质才能通过(反应条件省略)。
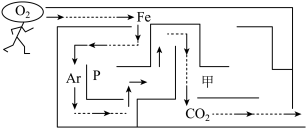
(注: :氧气;Fe:铁;Ar:氩气;P:
:氧气;Fe:铁;Ar:氩气;P: :二氧化碳)
:二氧化碳)
①“箭头”画出了“氧气”应行走的路线,“氧气”不能从甲处通过,你认为甲处的物质是_______ (填序号)。
A.氦气 B.水 C.蜡烛
②据图所示,图中有一处路线有错,请写出它在氧气中燃烧的实验现象_______ 和文字表达式_______ 。
③据图所示,氧气在进迷宫过程中,除了甲,还碰到了另外一种物质阻止它,请写出其中一个反应的文字表达式_______ ,反应类型为_______ (填基本反应类型)。
(1)工业上利用分离液态空气的方法制取氧气,是
(2)下列关于氧气的说法错误的是______(填序号)。
| A.氧气在氧化反应中提供氧,具有氧化性 |
| B.氧气具有可燃性,能使带火星的木条复燃 |
| C.红磷在空气中燃烧,实际上是与空气中的氧气反应 |
①食物腐败 ②煤炭燃烧 ③植物光合作用 ④人的呼吸
| A.①②③ | B.①③④ | C.①②④ |

(注:
①“箭头”画出了“氧气”应行走的路线,“氧气”不能从甲处通过,你认为甲处的物质是
A.氦气 B.水 C.蜡烛
②据图所示,图中有一处路线有错,请写出它在氧气中燃烧的实验现象
③据图所示,氧气在进迷宫过程中,除了甲,还碰到了另外一种物质阻止它,请写出其中一个反应的文字表达式
O2是人类赖以生存的重要物质之一。
(1)工业上将空气加压降温形成液态空气,再将液态空气蒸发制得O2,此过程属于___________ (填“物理变化”或“化学变化”)。
(2)实验室里为了探究影响H2O2分解快慢的因素,某小组分别取20mLH2O2溶液进行以下实验,测定产生10mLO2所需时间,实验结果记录如下:
①对比实验I与实验Ⅱ,t1___________ t2(填“>”“=”或“<”),说明其他条件相同时,温度越高,H2O2分解越快。
②对比实验___________ (填实验序号)与实验Ⅳ,说明其他条件相同时,H2O2溶液溶质质量分数越大,H2O2分解越___________ (填“快”或“慢”)。
③写出实验Ⅲ中反应的化学方程式:___________ 。
(3)生活中某品牌池塘增氧剂成分有过氧化钙(CaO2)、稳定剂、助效剂等,该增氧剂中CaO2能与水反应(其他成分不与水反应),其化学方程式为 。现取25g该增氧剂粉末于试管中,再逐滴滴加蒸馏水,产生的O2质量随加入的水质量变化如下图。
。现取25g该增氧剂粉末于试管中,再逐滴滴加蒸馏水,产生的O2质量随加入的水质量变化如下图。
①图中a=___________ 。
②该增氧剂中CaO2的质量分数_____ 。(计算结果精确到0.1%)
(1)工业上将空气加压降温形成液态空气,再将液态空气蒸发制得O2,此过程属于
(2)实验室里为了探究影响H2O2分解快慢的因素,某小组分别取20mLH2O2溶液进行以下实验,测定产生10mLO2所需时间,实验结果记录如下:
| 实验序号 | H2O2溶液溶质质量分数/% | 温度/℃ | MnO2粉末的质量/g | 反应时间/s |
| I | 15 | 20 | 0 | t1 |
| II | 15 | 55 | 0 | t2 |
| Ⅲ | 5 | 20 | 0.1 | 15 |
| IV | 15 | 20 | 0.1 | 2 |
②对比实验
③写出实验Ⅲ中反应的化学方程式:
(3)生活中某品牌池塘增氧剂成分有过氧化钙(CaO2)、稳定剂、助效剂等,该增氧剂中CaO2能与水反应(其他成分不与水反应),其化学方程式为

①图中a=
②该增氧剂中CaO2的质量分数
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


