科学探究题 较难0.4 引用4 组卷325
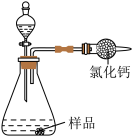
某兴趣小组用铁钉与硫酸铜溶液反应验证质量守恒定律时,发现铁钉表面有气泡产生、溶液没有变成浅绿色的异常现象,请你和兴趣小组一起探究,并回答问题。
【查阅资料】1.硫酸亚铁与氧气和水能发生反应,使得溶液中的氢离子浓度增加
2溶液中氢离子浓度越大,酸性越强
(1)探究一:铁钉表面产生的是什么气体?
【做出猜想】
猜想一:二氧化硫;猜想二:氧气;猜想三:氢气。
做出猜想的依据是___________ 。
【进行实验】
【实验分析】
硫酸铜溶液呈酸性,溶液中含有氢离子,该气体可看成由稀硫酸与铁钉反应产生的,请用化学方程式表示该气体产生的原因___________ 。
(2)探究二:铁和硫酸铜溶液反应的最佳条件是什么?
【实验探究】
分别用蒸馏水配置4%和2%的硫酸铜的冷、热溶液,各取5ml分别加入4支试管中,放入用砂纸打磨过的相同铁钉,比较反应现象,记录如下表:
①为探究反应物浓度对实验的影响,可选择实验___________ 进行对照(填实验编号)
②结合表格数据分析,铁和硫酸铜溶液反应的最佳条件是___________ 。
(3)探究三:反应中溶液pH值为什么减小?
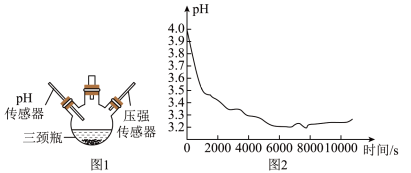
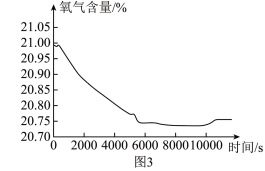
结合探究一中氢气产生的原理,兴趣小组的同学推测,随着反应的进行,溶液中氢离子浓度应该减小,pH值应该逐渐增大,于是利用如图1装置,用pH传感器测量溶液pH值的变化,同时测定了该装置中氧气含量的变化,结果如图2、图3所示,试分析溶液pH值下降的原因___________ 。
【反思与交流】
(4)结合以上探究综合分析
①探究二中配置硫酸铜溶液的蒸馏水应该___________ 。
②利用铁与硫酸铜反应验证质量守恒定律时,应注意___________ 。
【查阅资料】1.硫酸亚铁与氧气和水能发生反应,使得溶液中的氢离子浓度增加
2溶液中氢离子浓度越大,酸性越强
(1)探究一:铁钉表面产生的是什么气体?
【做出猜想】
猜想一:二氧化硫;猜想二:氧气;猜想三:氢气。
做出猜想的依据是
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①小芳用手在冒气泡的试管口轻轻扇动,使少量气体进入鼻孔 | 猜想一不正确 | |
| ②小刚用带火星的木条伸入收集该气体的试管中 | 木条不复燃 | 猜想二不正确 |
| ③小明将收集该气体的试管移近酒精灯火焰,松开拇指 | 猜想三正确 |
硫酸铜溶液呈酸性,溶液中含有氢离子,该气体可看成由稀硫酸与铁钉反应产生的,请用化学方程式表示该气体产生的原因
(2)探究二:铁和硫酸铜溶液反应的最佳条件是什么?
【实验探究】
分别用蒸馏水配置4%和2%的硫酸铜的冷、热溶液,各取5ml分别加入4支试管中,放入用砂纸打磨过的相同铁钉,比较反应现象,记录如下表:
| 实验编号 | 硫酸铜溶液 | 变为浅绿色 | 有红色固体 | 无气泡 | 符合标准现象 |
| 1 | 2%硫酸铜冷溶液 | √较慢 | √ | √ | √ |
| 2 | 2%硫酸铜热溶液 | √较快 | √ | √ | √ |
| 3 | 4%硫酸铜冷溶液 | √缓慢 | √ | √ | √ |
| 4 | 4%硫酸铜热溶液 | √较快 | √ | × | × |
②结合表格数据分析,铁和硫酸铜溶液反应的最佳条件是
(3)探究三:反应中溶液pH值为什么减小?
结合探究一中氢气产生的原理,兴趣小组的同学推测,随着反应的进行,溶液中氢离子浓度应该减小,pH值应该逐渐增大,于是利用如图1装置,用pH传感器测量溶液pH值的变化,同时测定了该装置中氧气含量的变化,结果如图2、图3所示,试分析溶液pH值下降的原因


【反思与交流】
(4)结合以上探究综合分析
①探究二中配置硫酸铜溶液的蒸馏水应该
②利用铁与硫酸铜反应验证质量守恒定律时,应注意
2023·安徽合肥·一模
类题推荐
垃圾是放错地方的资源,城市的废旧电器是一座“金属矿山”,某废旧电器中含有锌、铜、镍(Ni)三种金属,兴趣小组的同学为了从中回收金属铜和镍,做了如下的探究。
【查阅资料】硫酸镍(化学式NiSO4)能溶于水。
实验一;探究锌、铜、镍三种金属在溶液中的活动性强弱
【提出猜想】兴趣小组结合常见金属活动性顺序,提出了以下猜想。
(1)猜想一:Zn>Ni>Cu;猜想二:______ ;猜想三:Ni>Zn>Cu。
【进行实验】取三支试管,分别向其中加入等质量、等浓度的稀硫酸,然后将大小、形状相同的锌、钢、镍三种金属片分别插入三支试管中,请完成实验报告。
(2)
实验二;从含有锌、铜、镍三种金属的废旧电器中回收铜和镍3,号虽示
【设计方案】兴趣小组设计了如图所示的物质转化流程。
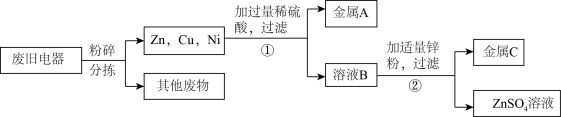
(3)步骤①中得到的A是______ ;
(4)步骤②中生成C的化学方程式是______ 。
【反思评价】
(5)合理开发城市“金属矿山”的意义是______ 。
【查阅资料】硫酸镍(化学式NiSO4)能溶于水。
实验一;探究锌、铜、镍三种金属在溶液中的活动性强弱
【提出猜想】兴趣小组结合常见金属活动性顺序,提出了以下猜想。
(1)猜想一:Zn>Ni>Cu;猜想二:
【进行实验】取三支试管,分别向其中加入等质量、等浓度的稀硫酸,然后将大小、形状相同的锌、钢、镍三种金属片分别插入三支试管中,请完成实验报告。
(2)
| 金属 | 实验现象 | 解释与结论 |
| 锌片 | 锌片表面产生的气泡较快 | 猜想 |
| 镍片 | 镍片表面产生的气泡较慢 | |
| 铜片 |
实验二;从含有锌、铜、镍三种金属的废旧电器中回收铜和镍3,号虽示
【设计方案】兴趣小组设计了如图所示的物质转化流程。

(3)步骤①中得到的A是
(4)步骤②中生成C的化学方程式是
【反思评价】
(5)合理开发城市“金属矿山”的意义是
某化学兴趣小组为探究金属铝和铜的活动性强弱,开展了以下活动。
【对比实验】
(1)比较实验乙和实验______ (填“甲”或“丙”)可得知:打磨能破坏氧化铝薄膜。
(2)实验乙中反应的化学方程式为______ ,据此可知金属活动性 Al 比 Cu ______ (填“强”或“弱”)。
(3)小明同学对实验丙的现象进行分析,认为 H2O 对氧化铝薄膜有破坏作用。但此观点马上被其他同学 否定,否定的依据是______ 。
【猜测与假设】
小组同学针对实验丙的现象,经讨论后猜测:Cl-破坏了氧化铝薄膜。
【继续实验】
(4)为检验此猜测是否正确,他们首先向两支试管中加入相同的 CuSO4 溶液,并均浸入表面未打磨的铝 丝,然后进行了新的探究:
【结论与反思】
(5)得出结论:上述猜测______ (“正确”或“不正确”)。
【对比实验】
| 编号 | 操作 | 现象 |
| 甲 | 将表面未打磨的铝丝浸入CuSO4溶液中 | 无明显现象 |
| 乙 | 将表面打磨后的铝丝浸入CuSO4溶液中 | 铝丝表面析出红色固体 |
| 丙 | 将表面未打磨的铝丝浸入CuCl2溶液中 | 铝丝表面析出红色固体 |
(1)比较实验乙和实验
(2)实验乙中反应的化学方程式为
(3)小明同学对实验丙的现象进行分析,认为 H2O 对氧化铝薄膜有破坏作用。但此观点马上被其他同学 否定,否定的依据是
【猜测与假设】
小组同学针对实验丙的现象,经讨论后猜测:Cl-破坏了氧化铝薄膜。
【继续实验】
(4)为检验此猜测是否正确,他们首先向两支试管中加入相同的 CuSO4 溶液,并均浸入表面未打磨的铝 丝,然后进行了新的探究:
| 操作 | 现象 | 结论 | 推论 |
| a、向一支试管中再加入NaCl固体 | 铝丝表面析出红色固体 | 氧化铝薄膜被破坏 | Na+或 |
| b、向另一支试管中再加入 | 氧化铝薄膜未被破坏 | Na+和 |
【结论与反思】
(5)得出结论:上述猜测
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网