实验题 0.4 引用1 组卷146
硫酸是世界上产量最大、用途最广的酸,被称为“化学工业之母”。化学兴趣小组同学时硫酸进行了多角度的研究。
【物质制备】
(1)工业上采用接触法制硫酸:先煅烧黄铁矿得到SO2,再将SO2经过一系列变化得到硫酸。SO2到硫酸的过程中硫元素的化合价______ (填“升高”或“不变”或“降低”)。
(2)实验室用100mL98%的浓硫酸(1.84g/mL)配制9.8%的稀硫酸,需要加水______ mL。
【物质性质】
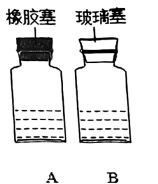
(3)探究稀硫酸与氢氧化钠溶液的反应。_______ (填“A”或“B”)中的氢氧化钠溶液5mL加入烧杯中,并插入pH计。
②从另一试剂瓶中取出稀硫酸逐滴加入①的溶液中,并不断搅拌。
反应过程中溶液pH变化的部分数据如下表所示:
在pH=12.8时,溶液中的溶质是______ (填化学式)。
③滴加稀硫酸过程中,溶液pH不断减小的原因有:a.硫酸与氢氧化钠发生了反应;b.__________________________________________ 。
④为证明溶液pH从13.1减小到10.4的过程中,④中原因a起主要作用,需设计的实验方案是___________________________________________________ 。
(4)探究稀硫酸与金属氧化物的反应。
①向氧化铜中加入足量稀硫酸,可观察到__________________________ 。
②在反应得到的溶液中,逐滴滴加氢氧化钠,刚开始没有明显现象,可能的原因是___________________________________ 。
③继续加入足量氢氧化钠溶液,生成蓝色沉淀氢氧化铜,氢氧化铜易分解,放置一天后蓝色沉淀变黑,写出分解的反应方程式_____________________________ 。
【定量研究】
(5)某工厂现有含碳酸钠的废水需要处理。为测定废水中碳酸钠的质量分数,化学兴趣小组同学取废水样品100g,加入溶质质量分数为10%的硫酸溶液9.8g,恰好完全反应(此废水中其他物质不与硫酸反应)。计算废水中碳酸钠的质量分数(写出计算过程)。
【物质制备】
(1)工业上采用接触法制硫酸:先煅烧黄铁矿得到SO2,再将SO2经过一系列变化得到硫酸。SO2到硫酸的过程中硫元素的化合价
(2)实验室用100mL98%的浓硫酸(1.84g/mL)配制9.8%的稀硫酸,需要加水
【物质性质】
(3)探究稀硫酸与氢氧化钠溶液的反应。
②从另一试剂瓶中取出稀硫酸逐滴加入①的溶液中,并不断搅拌。
反应过程中溶液pH变化的部分数据如下表所示:
稀硫酸体积/mL | 0 | 2 | 4 | 6 | 8 | … |
溶液pH | 13.1 | 12.8 | 12.3 | 11.5 | 10.4 | … |
③滴加稀硫酸过程中,溶液pH不断减小的原因有:a.硫酸与氢氧化钠发生了反应;b.
④为证明溶液pH从13.1减小到10.4的过程中,④中原因a起主要作用,需设计的实验方案是
(4)探究稀硫酸与金属氧化物的反应。
①向氧化铜中加入足量稀硫酸,可观察到
②在反应得到的溶液中,逐滴滴加氢氧化钠,刚开始没有明显现象,可能的原因是
③继续加入足量氢氧化钠溶液,生成蓝色沉淀氢氧化铜,氢氧化铜易分解,放置一天后蓝色沉淀变黑,写出分解的反应方程式
【定量研究】
(5)某工厂现有含碳酸钠的废水需要处理。为测定废水中碳酸钠的质量分数,化学兴趣小组同学取废水样品100g,加入溶质质量分数为10%的硫酸溶液9.8g,恰好完全反应(此废水中其他物质不与硫酸反应)。计算废水中碳酸钠的质量分数(写出计算过程)。
2023·江苏苏州·模拟预测


