科学探究题 适中0.65 引用1 组卷156
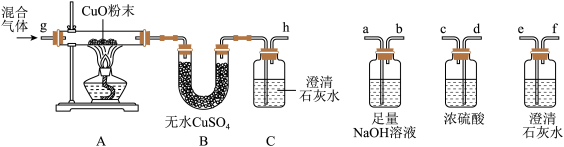
实验一:水煤气是将水蒸气通过灼热的焦炭而生成的气体,主要成分是一氧化碳、氢气及少量的二氧化碳和水蒸气。某课题组同学为验证水煤气的成分,做了以下准备:
(一)资料收集:
①
②
③无水硫酸铜遇水由白色变为蓝色
(二)设计实验装置:
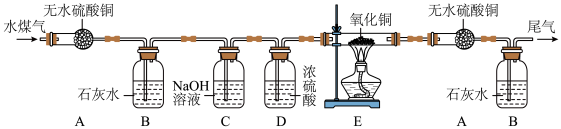
请分析上面信息后回答:
(1)你认为验证水煤气中各成分的顺序依次是_________ 。
(2)设计装置C的目的是__________ 。
(3)实验中两次用到装置A,其目的分别是________ 。
实验二:同学们用下图所示实验探究碱的化学性质,请你回答:
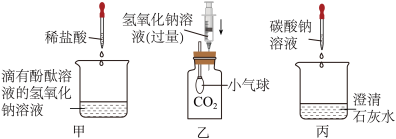
(4)做甲图所示实验时,当观察到__________ ,证明稀盐酸和氢氧化钠发生了反应。
(5)做乙图所示实验时,看到的现象是__________ ,有同学认为该现象不足以证明二氧化碳与氢氧化钠发生了反应,他提出:可以向混合后的溶液中加入_______ ,若产生明显现象,即可证明二氧化碳与氢氧化钠确实发生了反应。
(6)从微观角度分析,甲、乙、丙三个实验中,实验__________ (填实验序号)中的OH-没有真正参与反应。
将甲、乙、丙中的无色溶液均倒入洁净的废液缸,发现废液明显变浑浊且呈红色,同学们很好奇,于是接着进行了下面的拓展学习与探究。
【提出问题】使废液变成红色的物质是什么?
【做出猜想】
(7)猜想一:只有Na2CO3
猜想二:只有NaOH
猜想三:NaOH和Na2CO3
猜想四:__________ 。
你认为以上猜想中,不合理的是哪个并说明理由_______ 。
【查阅资料】CaCl2溶液呈中性。
【设计并进行实验】
(8)静置一段时间后,取少量废液缸中的上层红色清液于试管中,加入过量CaCl2溶液,观察现象。
①有白色沉淀生成,上层清液仍为红色,由此证明了猜想___________ 成立。
②若无沉淀生成,溶液呈红色,由此证明猜想二成立。
【实验反思】
(9)同学们认为上述实验②的结论不严密,原因是___________ 。
(一)资料收集:
①
②
③无水硫酸铜遇水由白色变为蓝色
(二)设计实验装置:

请分析上面信息后回答:
(1)你认为验证水煤气中各成分的顺序依次是
(2)设计装置C的目的是
(3)实验中两次用到装置A,其目的分别是
实验二:同学们用下图所示实验探究碱的化学性质,请你回答:

(4)做甲图所示实验时,当观察到
(5)做乙图所示实验时,看到的现象是
(6)从微观角度分析,甲、乙、丙三个实验中,实验
将甲、乙、丙中的无色溶液均倒入洁净的废液缸,发现废液明显变浑浊且呈红色,同学们很好奇,于是接着进行了下面的拓展学习与探究。
【提出问题】使废液变成红色的物质是什么?
【做出猜想】
(7)猜想一:只有Na2CO3
猜想二:只有NaOH
猜想三:NaOH和Na2CO3
猜想四:
你认为以上猜想中,不合理的是哪个并说明理由
【查阅资料】CaCl2溶液呈中性。
【设计并进行实验】
(8)静置一段时间后,取少量废液缸中的上层红色清液于试管中,加入过量CaCl2溶液,观察现象。
①有白色沉淀生成,上层清液仍为红色,由此证明了猜想
②若无沉淀生成,溶液呈红色,由此证明猜想二成立。
【实验反思】
(9)同学们认为上述实验②的结论不严密,原因是
2023·山东济宁·一模
类题推荐
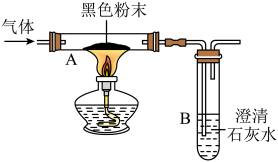
在探究课上,老师给同学们一包黑色粉末,该粉末是由铁粉和氧化铜粉末中的一种或两种组成。为了确定该粉末的成分,同学们进行如下探究:
【猜想假设】猜想一:黑色粉末是铁粉;
猜想二:黑色粉末是氧化铜粉末;
猜想三:黑色粉末是______ 。
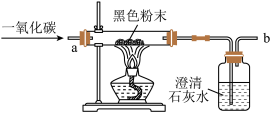
【设计方案】取少量黑色粉末,放入硬质玻璃管中,通入一氧化碳气体,片刻后加热充分反应。(一氧化碳足量,实验装置如图所示)
请填写如表空白:(不考虑铁粉和氧化铜粉末可能发生反应)
【实验结论】经过分析实验现象,确认猜想三成立。
【反思评价】
(1)从环保角度上看,上述设置有不足之处,改进措施是______ 。
(2)猜想二玻璃管中发生反应的化学方程式是______ 。
【猜想假设】猜想一:黑色粉末是铁粉;
猜想二:黑色粉末是氧化铜粉末;
猜想三:黑色粉末是
【设计方案】取少量黑色粉末,放入硬质玻璃管中,通入一氧化碳气体,片刻后加热充分反应。(一氧化碳足量,实验装置如图所示)

请填写如表空白:(不考虑铁粉和氧化铜粉末可能发生反应)
| 实验中可能出现的现象 | 结论 |
| 猜想一成立 | |
| 黑色粉末全部变红,澄清的石灰水变浑浊 | 猜想二 (填“成立”或“不成立”) |
| 猜想三成立 |
【反思评价】
(1)从环保角度上看,上述设置有不足之处,改进措施是
(2)猜想二玻璃管中发生反应的化学方程式是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网