科学探究题 适中0.65 引用1 组卷89
Cu和Cu2O均为红色固体,某小组对CO还原CuO得到的红色固体产生兴趣。
【猜测】
(1)三位同学对反应生成的红色固体提出如下猜想:
甲:固体是Cu;乙:固体是___________ ;丙:固体是Cu2O和Cu;
资料1:
【实验】
(2)取红色固体样品,加入适量的稀硫酸,观察到___________ (填实验现象),甲猜想错误。
资料2:
①加热时,H2和Cu2O能反应,产生Cu和H2O
②白色的无水CuSO4遇水蒸气会变成蓝色。
(3)为进一步确定红色固体组成,另取17.6g该样品,进行如下实验:
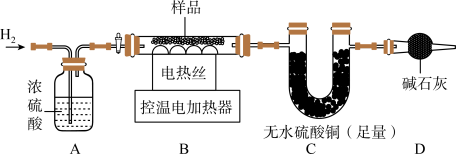
①实验时,先___________ (填“加热样品”或“通一段时间的H2”)。
②通入足量H2加热,充分反应后,C中白色固体变蓝色,且增加1.8g。实验中D装置的作用是___________ 。
【结论】
(4)通过计算,得出样品中Cu2O质量为___________ g,可知___________ (填“乙”或“丙”)猜想成立。
(5)小组同学用CO还原CuO时发生反应的化学方程式:___________ 。
【猜测】
(1)三位同学对反应生成的红色固体提出如下猜想:
甲:固体是Cu;乙:固体是
资料1:
【实验】
(2)取红色固体样品,加入适量的稀硫酸,观察到
资料2:
①加热时,H2和Cu2O能反应,产生Cu和H2O
②白色的无水CuSO4遇水蒸气会变成蓝色。
(3)为进一步确定红色固体组成,另取17.6g该样品,进行如下实验:

①实验时,先
②通入足量H2加热,充分反应后,C中白色固体变蓝色,且增加1.8g。实验中D装置的作用是
【结论】
(4)通过计算,得出样品中Cu2O质量为
(5)小组同学用CO还原CuO时发生反应的化学方程式:
22-23九年级上·江苏镇江·阶段练习
类题推荐
某小组以“寻找新的催化剂”为研究性实验,引起了化学探究小组的兴趣。
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
【实验结论】
(1)实验Ⅱ、Ⅲ证明:氧化铁的______ 在反应前后均没有发生变化;
【实验评价】
(2)实验Ⅳ中的a=______ g
(3)从上述实验观察到的现象,你得到的结论是______ 。
【拓展】
(4)下列有关催化剂的说法中正确的是______ 。
Ⅰ. 只能作过氧化氢溶液分解的催化剂
只能作过氧化氢溶液分解的催化剂
Ⅱ.同一个化学反应可以有多种催化剂
Ⅲ.催化剂能改变化学反应的速率,但不能增加产物的量
Ⅳ.用作催化剂的物质不可能是其他反应的反应物或生成物
(5)将一定量的双氧水溶液和二氧化锰混合,充分反应,测得反应的总质量(m)与反应时间(t)的数据如下表所示:

(A)写出该反应的化学方程式______ ,
(B)则双氧水的物质的量是______ 。
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
| 实验步骤 | 实验现象 |
| Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入2g氧化铁粉末,在试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
| Ⅱ.待A试管中反应停止后,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
| Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为2g。 | |
| Ⅳ.常温下,分别量取5mL5%和5mL5%的过氧化氢溶液放入C、D两支试管中,向C试管中加入2g氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 | C、D两支试管中均产生气泡,且D中产生气泡的速度更快 |
(1)实验Ⅱ、Ⅲ证明:氧化铁的
【实验评价】
(2)实验Ⅳ中的a=
(3)从上述实验观察到的现象,你得到的结论是
【拓展】
(4)下列有关催化剂的说法中正确的是
Ⅰ.
Ⅱ.同一个化学反应可以有多种催化剂
Ⅲ.催化剂能改变化学反应的速率,但不能增加产物的量
Ⅳ.用作催化剂的物质不可能是其他反应的反应物或生成物
(5)将一定量的双氧水溶液和二氧化锰混合,充分反应,测得反应的总质量(m)与反应时间(t)的数据如下表所示:

| 反应时间t/s | ||||||
| 总质量m/g | 55 | 53.5 | 52.1 | 51.0 | 50.2 | 50.2 |
(B)则双氧水的物质的量是
某化学学习小组对泡腾片的成分和原理产生了兴趣。某品牌维生素C泡腾片部分标签如图所示,据此回答问题。
【任务一】认识成分
(1)取泡腾片溶于水,滴加紫色石蕊试剂,溶液变红,说明溶液
___________ 7(选填“>”“<”或“=”)。
(2)泡腾片溶于水时闻到“橙味”香气,从微观角度解释其原因是___________ 。
【任务二】测定碳酸氢钠的含量(质量分数)
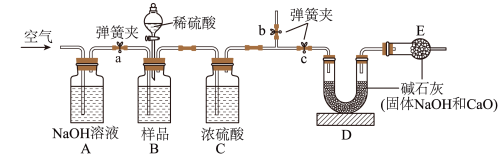
为了测定某维C泡腾片中碳酸氢钠的含量,张老师引导学生设计了如下实验装置(仪器固定装置及止水夹等均已略去)并进行实验。有关实验数据为:①取维C泡腾片2片(每片维C泡腾片的质量为 );②)盛有碱石灰(主要成分为氢氧化钠和氧化钙的固体混合物)的干燥管a质量增加了
);②)盛有碱石灰(主要成分为氢氧化钠和氧化钙的固体混合物)的干燥管a质量增加了 。
。___________ 。
(4)该实验中维C泡腾片反应完毕后通入空气的目的是___________ 。装置中干燥管b的作用是___________ 。
(5)根据实验数据,可计算出该维C泡腾片中碳酸氢钠的含量为___________ 。
(6)如果撤去装置中盛有浓硫酸的洗气瓶,则测定结果___________ (选填“偏高”“偏低”或“无影响)。
| (XX品牌)维生素C泡腾片说明书 主要成分:维生素C( |
(1)取泡腾片溶于水,滴加紫色石蕊试剂,溶液变红,说明溶液
(2)泡腾片溶于水时闻到“橙味”香气,从微观角度解释其原因是
【任务二】测定碳酸氢钠的含量(质量分数)
为了测定某维C泡腾片中碳酸氢钠的含量,张老师引导学生设计了如下实验装置(仪器固定装置及止水夹等均已略去)并进行实验。有关实验数据为:①取维C泡腾片2片(每片维C泡腾片的质量为

(4)该实验中维C泡腾片反应完毕后通入空气的目的是
(5)根据实验数据,可计算出该维C泡腾片中碳酸氢钠的含量为
(6)如果撤去装置中盛有浓硫酸的洗气瓶,则测定结果
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网