科学探究题 较难0.4 引用1 组卷116
小丽同学发现自己铜制镜框表面出现了绿色的“铜锈”,与小组同学对铜锈产生条件进行探究。
【提出问题】铜生锈的条件是什么?
【查阅资料】铜锈的主要成分是Cu2(OH)2CO3,俗称铜绿。
【作出猜想】铜生锈的条件是铜与H2O、CO2接触。
【进行实验】将4小块铜片 长度和宽度相同
长度和宽度相同 按如图装置所示放置一个月,结果如下:
按如图装置所示放置一个月,结果如下:
【得出结论】铜生锈的条件是与H2O、CO2接触。
(1)写出铜绿受热分解方程式_______ 。
(2)对比实验①、③得到的结论是_______ 。
(3)能说明铜生锈与H2O有关的实验是_______ 。
(4)经过反思,小刚同学对所得结论提出疑议:与氧气接触也可能是铜生锈的条件之一、小丽同学认为实验①、④对比即可说明铜生锈与氧气有关。请判断小丽的说法是否正确_ (填“正确”或“错误”)。
(5)通过实验证明,铜生锈的条件是铜与氧气、水、二氧化碳接触。由此,你对保存铜制品的建议是_______ 。
【提出问题】铜生锈的条件是什么?
【查阅资料】铜锈的主要成分是Cu2(OH)2CO3,俗称铜绿。
【作出猜想】铜生锈的条件是铜与H2O、CO2接触。
【进行实验】将4小块铜片
| 编号 | ① | ② | ③ | ④ |
| 实验 |  |  | 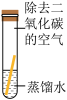 | 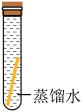 |
| 现象 | 铜片表面有绿色物质 | 无明显现象 | 无明显现象 | 无明显现象 |
(1)写出铜绿受热分解方程式
(2)对比实验①、③得到的结论是
(3)能说明铜生锈与H2O有关的实验是
(4)经过反思,小刚同学对所得结论提出疑议:与氧气接触也可能是铜生锈的条件之一、小丽同学认为实验①、④对比即可说明铜生锈与氧气有关。请判断小丽的说法是否正确
(5)通过实验证明,铜生锈的条件是铜与氧气、水、二氧化碳接触。由此,你对保存铜制品的建议是
22-23九年级上·江苏扬州·阶段练习
类题推荐
钙元素是一种重要的金属元素,它形成的物质种类很多。
(1)氢化钙(CaH2)固体是登山运动员常用的能源提供剂。
某实验探究小组的同学通过查阅资料得知:CaH2能与H2O反应生成Ca(OH)2和H2,请你写出该反应的化学方程式_______ 。
(2)生石灰溶于水可制得熟石灰,该反应过程中能量的变化是_______ (填“吸热”或“放热”),实验室可以用_______ 测定其溶液的酸碱度。
(3)实验探究小组同学将Na2CO3溶液滴加到Ca(OH)2溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
【提出问题】滤液中溶质的成分是什么?
【做出猜想】猜想一:NaOH 猜想二:NaOH和Ca(OH)2
猜想三:NaOH和______ 猜想四:NaOH、Na2CO3和Ca(OH)2
经过讨论,大家认为猜想四不合理,原因是_____ 。
【实验过程】
【拓展延伸】在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑______ 。
(1)氢化钙(CaH2)固体是登山运动员常用的能源提供剂。
某实验探究小组的同学通过查阅资料得知:CaH2能与H2O反应生成Ca(OH)2和H2,请你写出该反应的化学方程式
(2)生石灰溶于水可制得熟石灰,该反应过程中能量的变化是
(3)实验探究小组同学将Na2CO3溶液滴加到Ca(OH)2溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
【提出问题】滤液中溶质的成分是什么?
【做出猜想】猜想一:NaOH 猜想二:NaOH和Ca(OH)2
猜想三:NaOH和
经过讨论,大家认为猜想四不合理,原因是
【实验过程】
| 实验步骤 | 现象 | 结论 |
| 实验Ⅰ:取滤液,向其中滴入适量Na2CO3溶液 | 猜想二不成立 | |
| 实验Ⅱ:另取滤液,向其中加入足量 | 产生气泡 | 猜想 |
【拓展延伸】在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑
某化学课外兴趣小组通过查阅资料知道过氧化钠(Na2O2)能与水反应生成氢氧化钠和氧气,于是他们做了以下探究实验。
实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来。请你对脱脂棉燃烧的原因进行分析____________________ 。
实验2:向盛有过氧化钠粉末的试管中加入水,充分反应后,取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红,过了一会,红色又褪去了。
【提出问题】溶液为什么先变红,过了一会,红色又褪去了呢?
【猜想】甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故。乙同学认为甲同学的猜想不正确,理由是________________ 。
【查阅资料】①滴加酚酞呈现红色的溶液遇到H2O2时,H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;②酚酞在稀碱性溶液中稳定显红色,而在浓氢氧化钠等溶液中显红色后又褪色。
【猜想】通过查阅资料后,该兴趣小组对溶液的红色褪去的主要原因又进行了猜想。
猜想A:过氧化钠与水反应可能生成了H2O2;猜想B:生成的氢氧化钠溶液可能太浓。
【实验探究】请你将下列实验方案填写完整。
【得出结论】根据实验分析,过氧化钠与水反应除了生成氢氧化钠和氧气外,还存在另一反应,则另一反应的化学方程式为___________________ 。
实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来。请你对脱脂棉燃烧的原因进行分析
实验2:向盛有过氧化钠粉末的试管中加入水,充分反应后,取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红,过了一会,红色又褪去了。
【提出问题】溶液为什么先变红,过了一会,红色又褪去了呢?
【猜想】甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故。乙同学认为甲同学的猜想不正确,理由是
【查阅资料】①滴加酚酞呈现红色的溶液遇到H2O2时,H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;②酚酞在稀碱性溶液中稳定显红色,而在浓氢氧化钠等溶液中显红色后又褪色。
【猜想】通过查阅资料后,该兴趣小组对溶液的红色褪去的主要原因又进行了猜想。
猜想A:过氧化钠与水反应可能生成了H2O2;猜想B:生成的氢氧化钠溶液可能太浓。
【实验探究】请你将下列实验方案填写完整。
| 猜想 | 实验操作 | 实验现象 | 结论 |
| A | 取过氧化钠与水反应后的溶液放入试管中, 加入适量的二氧化锰后,将带火星的木条放在试管口 | 猜想A 正确 | |
| B | 取过氧化钠与水反应后的溶液放入试管中, | 猜想B 错误 |
某化学兴趣小组在探究氢氧化钠的化学性质时,将二氧化碳通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究。
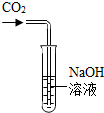
探究一:二氧化碳是否与氢氧化钠溶液发生了化学反应?
取少量大试管中的液体,滴加足量的稀盐酸,观察到_______ ,证明二氧化碳与氢氧化钠发生了反应。
探究二:反应后大试管中溶液所含溶质的成分是什么?
【查阅资料】
①CO2与碳酸钠溶液反应的化学方程式为_______ :
②NaHCO3溶液呈碱性,能与NaOH反应,且与澄清石灰水反应生成白色沉淀
③BaC12溶液呈中性,与Na2CO3反应生成白色沉淀,与 NaHCO3不发生反应
小组成员经过分析讨论,一致认为溶质的成分为Na2CO3、NaHCO3、NaOH中的一种成几种。
【猜想假设】
猜想一:NaOH、Na2CO3猜想二:Na2CO3
猜想三:_______ 猜想四:NaHCO3
【实验探究】
实验1:小华设计了以下实验。
【实验结论】
小华根据观察到的实验现象得出猜想_______ 成立。
实验2:小红设计了以下实验。
小红根据观察到的实验现象得出猜想_______ 成立。
【实验反思】化学反应是否发生,可以借助反应过程中伴随的实验现象来判断,也可以借助生成物的性质来判断。

探究一:二氧化碳是否与氢氧化钠溶液发生了化学反应?
取少量大试管中的液体,滴加足量的稀盐酸,观察到
探究二:反应后大试管中溶液所含溶质的成分是什么?
【查阅资料】
①CO2与碳酸钠溶液反应的化学方程式为
②NaHCO3溶液呈碱性,能与NaOH反应,且与澄清石灰水反应生成白色沉淀
③BaC12溶液呈中性,与Na2CO3反应生成白色沉淀,与 NaHCO3不发生反应
小组成员经过分析讨论,一致认为溶质的成分为Na2CO3、NaHCO3、NaOH中的一种成几种。
【猜想假设】
猜想一:NaOH、Na2CO3猜想二:Na2CO3
猜想三:
【实验探究】
实验1:小华设计了以下实验。
| 序号 | 实验操作 | 实验现象 |
| ① | 取一定量大试管中的溶液于试管中,加入足量的BaC12溶液 | 产生白色沉 |
| ② | 过滤 |  |
| ③ | 取一定量的滤液于试管中,加入澄清石灰水 | 没有明显现象 |
| ④ | 取一定量的滤液于另一支试管中,滴加适量酚酞溶液 |
【实验结论】
小华根据观察到的实验现象得出猜想
实验2:小红设计了以下实验。
| 序号 | 实验操作 | 实验现象 |
| ① | 取一定量大试管中的溶液于试管中,加入足量的BaC12溶液 | 产生白色沉 |
| ② | 过滤 |  |
| ③ | 取一定量的滤液于试管中,加入澄清石灰水 | 产生白色沉 |
小红根据观察到的实验现象得出猜想
【实验反思】化学反应是否发生,可以借助反应过程中伴随的实验现象来判断,也可以借助生成物的性质来判断。
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


