选择题-单选题 适中0.65 引用2 组卷105
物质的除杂和鉴别是重要的实验技能。下列实验方法不能达到目的的是
实验目的 | 实验操作 | |
A | 除去铁粉中的少量铜粉 | 加足量稀硫酸充分反应后过滤 |
B | 除去氧化钙中混有的少量碳酸钙 | 高温煅烧 |
C | 鉴别过氧化氢水溶液和水 | 各取少量液体分别加入MnO2,观察现象 |
D | 鉴别黄铜(铜锌合金)和黄金 | 分别取样滴加稀盐酸,观察现象 |
| A.A | B.B | C.C | D.D |
21-22九年级上·吉林长春·期末
类题推荐
在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量的关系能用右下图曲线表示的是
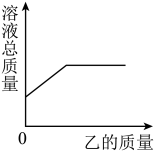
| 序号 | 甲 | 乙 |
| ① | HCl溶液 | NaOH溶液 |
| ② | HCl溶液 | 大理石 |
| ③ | H2SO4溶液 | 锌粒 |
| ④ | Ca(OH)2溶液 | Na2CO3溶液 |
| ⑤ | CuSO4溶液 | 铁粉 |

| A.①② | B.③④ | C.①⑤ | D.②③ |
物质的性质决定用途。下列关于物质的性质与用途的说法不正确的是
| A.熟石灰呈碱性,可用于改良酸性土壤 |
| B.氮气的化学性质活泼,可用于食品充氮防腐 |
| C.稀盐酸能与 |
| D.活性炭具有吸附性,可用做冰箱除味剂 |
硫酸亚铁铵【(NH4)2SO4·FeSO4·6H2O】俗称摩尔盐,可用于净水和治疗缺铁性贫血。工业上常利用机械加工行业产生的废铁屑(含有少量杂质Fe2O3)为原料制备(如图)。某化学兴趣小组拟用下列方案制备硫酸亚铁铵并进行相关探究。查阅资料:
(1)Fe和Fe3+会反应生成Fe2+
(2)FeSO4易被氧气氧化为Fe2(SO4)3,影响硫酸亚铁铵的等级。
(3)在FeSO4溶液中加入(NH4)2SO4固体可制备硫酸亚铁铵晶体,该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
(4)在0~60℃时,硫酸亚铁铵的溶解度比硫酸铵、硫酸亚铁的溶解度小,冷却混合液至室温便析出硫酸亚铁铵。
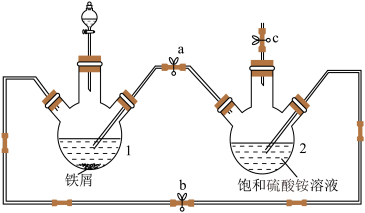
用下图所示装置制备硫酸亚铁铵。下列说法错误的是
(1)Fe和Fe3+会反应生成Fe2+
(2)FeSO4易被氧气氧化为Fe2(SO4)3,影响硫酸亚铁铵的等级。
(3)在FeSO4溶液中加入(NH4)2SO4固体可制备硫酸亚铁铵晶体,该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
(4)在0~60℃时,硫酸亚铁铵的溶解度比硫酸铵、硫酸亚铁的溶解度小,冷却混合液至室温便析出硫酸亚铁铵。
用下图所示装置制备硫酸亚铁铵。下列说法错误的是

| A.先关闭止水夹a,再打开止水夹b和c,滴加稀硫酸,充分反应后,烧瓶1溶液中有两种金属阳离子 |
| B.该过程中氢气的作用是防止硫酸亚铁被氧化成硫酸铁 |
| C.待烧瓶1中不再产生气泡时,关闭止水夹b、c,打开止水夹a,烧瓶2中有晶体出现 |
| D.为获得产品,需将烧瓶2中(NH4)2SO4·FeSO4·6H2O粗产品洗涤后干燥,洗涤的方式是先用冷水洗,后用无水乙醇洗 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


