科学探究题 适中0.65 引用1 组卷121
实验探究一:小明学习了过氧化氢溶液分解知识后,脑洞大开,还想寻找新的催化剂,于是设计了如下探究方案:
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】请写出红砖粉末(成分以Fe2O3表示)催化过氧化氢溶液分解反应的符号表达式_______ 。
实验探究二:小明继续探究带火星的木条在不同体积分数氧气中的复燃情况,部分实验数据记录如表:
①根据上述实验数据得出的结论:能使带火星的小木条复燃的_______ (填一定或不一定)是纯氧。
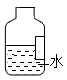
②在集气瓶中注入占其容器50%的水(如图),用排水法收集氧气,刚好将瓶内的水排尽,用带火星的木条在该集气瓶中进行实验,小木条_______ (填“复燃”或“不复燃”)理由是_______ 。
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
| 实验步骤及操作 | 实验现象 | 实验结论及解释 |
Ⅰ.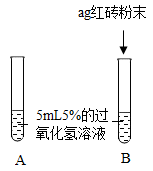 | A中无明显现象,B中产生大量能使带火星木条复燃的气体 | ①产生的气体是 ②红砖粉末能改变过氧化氢分解速率 |
| Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ①又产生大量能使带火星木条复燃的气体 ②滤渣质量等于ag | 红砖粉末的 |
Ⅲ.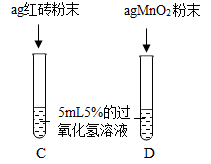 | 两试管中均产生气泡且 | 红砖粉末的催化效果没有二氧化锰粉末好 |
【实验探究】请写出红砖粉末(成分以Fe2O3表示)催化过氧化氢溶液分解反应的符号表达式
实验探究二:小明继续探究带火星的木条在不同体积分数氧气中的复燃情况,部分实验数据记录如表:
| 氧气体积分数(%) | 30 | 40 | 60 | 70 |
| 带火星的木条 | 不变 | 稍亮 | 复燃 | 复燃 |
①根据上述实验数据得出的结论:能使带火星的小木条复燃的
②在集气瓶中注入占其容器50%的水(如图),用排水法收集氧气,刚好将瓶内的水排尽,用带火星的木条在该集气瓶中进行实验,小木条

21-22九年级上·湖南常德·期中
类题推荐
某化学兴趣小组在学习O2制备时,对影响双氧水分解速率的因素产生了兴趣。于是,小组同学对双氧水分解速率的影响因素展开探究。
【提出问题】影响双氧水分解速率的因素有哪些?
【查阅资料】影响化学反应速率的因素有很多,如使用催化剂、改变温度、改变反应物的浓度。
【实验探究】
Ⅰ.探究催化剂对双氧水分解速率的影响。
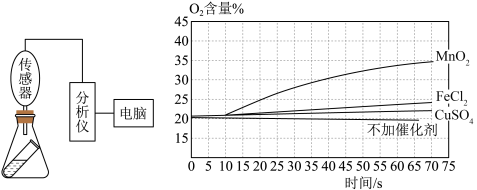
小组同学按图组装,在室温下分别进行了四组实验,并用О2传感器测定实验过程中O2含量的变化情况,得到如图所示曲线。
【交流与解释】对比四条曲线,进行分析:
(1)第1组实验的目的是_________ 。
(2)写出第2组实验的化学反应方程式__________ 。
(3)根据本实验可知,对双氧水的分解有催化作用的物质有_______ 。
Ⅱ.探究温度和浓度对双氧水分解速率的影响。
小组同学不加催化剂,在不同温度下,用不同浓度的双氧水进行实验,记录实验现象如表。
【实验结论】
(4)浓度为15%的双氧水,随着温度的升高,分解速率增大。70℃时,双氧水的浓度对分解速率的影响是______ 。
【拓展与延伸】
(5)控制变量法是科学探究常用的方法之一。它是通过控制某几个因素不变,只让其中一个因素改变,从而转化为多个单一因素影响某一研究因素的问题的研究方法。请分析实验探究Ⅰ能否得出MnO2是双氧水分解最优的催化剂?说明理由:_________ 。
【提出问题】影响双氧水分解速率的因素有哪些?
【查阅资料】影响化学反应速率的因素有很多,如使用催化剂、改变温度、改变反应物的浓度。
【实验探究】
Ⅰ.探究催化剂对双氧水分解速率的影响。
小组同学按图组装,在室温下分别进行了四组实验,并用О2传感器测定实验过程中O2含量的变化情况,得到如图所示曲线。
| 组别 | 试剂 | 催化剂 |
| 第1组 | 2mL5%H2O2溶液 | 无 |
| 第2组 | 2mL5%H2O2溶液 | 3滴FeCl3溶液 |
| 第3组 | 2mL5%H2O2溶液 | 3滴CuSO4溶液 |
| 第4组 | 2mL5%H2O2溶液 | 少量MnO2粉末(与3滴FeCl3溶液或3滴CuSO4溶液的量相当) |
(1)第1组实验的目的是
(2)写出第2组实验的化学反应方程式
(3)根据本实验可知,对双氧水的分解有催化作用的物质有
Ⅱ.探究温度和浓度对双氧水分解速率的影响。
小组同学不加催化剂,在不同温度下,用不同浓度的双氧水进行实验,记录实验现象如表。
温度 浓度 | 50℃ | 60℃ | 70℃ |
| 5% | 无明显气泡 | 无明显气泡 | 极少量气泡 |
| 10% | 无明显气泡 | 无明显气泡 | 少量气泡 |
| 15% | 无明显气泡 | 少量气泡 | 较多气泡 |
(4)浓度为15%的双氧水,随着温度的升高,分解速率增大。70℃时,双氧水的浓度对分解速率的影响是
【拓展与延伸】
(5)控制变量法是科学探究常用的方法之一。它是通过控制某几个因素不变,只让其中一个因素改变,从而转化为多个单一因素影响某一研究因素的问题的研究方法。请分析实验探究Ⅰ能否得出MnO2是双氧水分解最优的催化剂?说明理由:
某校化学兴趣小组的同学对实验室制氧气和氧气的某些性质进行了如下探究。
【探究一】探究催化剂种类对过氧化氢分解速率的影响。
【设计方案】常温下,取两份5%H2O2溶液各100mL,分别加入1g氧化铜和二氧化锰固体,测量各生成125mLO2所需的时间。
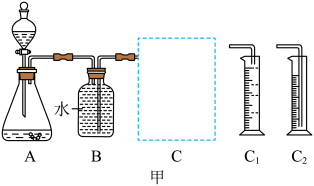
【实验探究】该小组采用了如图甲所示装置进行实验,检查装置气密性良好后,将分液漏斗中的液体加入锥形瓶中,收集气体。
【实验记录】
【实验分析】
(1)若要证明二氧化锰、氧化铜是该反应的催化剂,还需要验证它们在化学反应前后的质量和_________ 没有改变。写出实验2中反应的化学方程式: _______________ 。
(2)图甲中C装置应该选择_______________ (选填“C1”或“C2”)。
(3)分析表格中数据,可以得出相同条件下催化剂的催化效果较好的是______________ 。
(4)要定量地比较化学反应速度的快慢,除了上述方法外,还可以______________ 。
【探究二】利用图乙所示装置探究氧气的浓度对燃烧的影响。
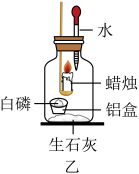
【实验方案】点燃蜡烛后立即塞紧橡皮塞,待蜡烛熄灭后,将滴管中的水全部滴入瓶中,铝盒中的白磷立即燃烧。
(5)白磷燃烧的主要现象是______________ 。
(6)由“蜡烛熄灭,白磷燃烧”可得出的结论是______________ 。
(7)滴入水后白磷立即燃烧的原因是______________ 。
【探究一】探究催化剂种类对过氧化氢分解速率的影响。
【设计方案】常温下,取两份5%H2O2溶液各100mL,分别加入1g氧化铜和二氧化锰固体,测量各生成125mLO2所需的时间。
【实验探究】该小组采用了如图甲所示装置进行实验,检查装置气密性良好后,将分液漏斗中的液体加入锥形瓶中,收集气体。

【实验记录】
| 实验编号 | ① | ② |
| 反应物 | 5%H2O2溶液100mL | 5%H2O2溶液100mL |
| 加入固体 | 1gCuO | 1gMnO2 |
| 收集125mLO2所需时间 | 165s | 46s |
(1)若要证明二氧化锰、氧化铜是该反应的催化剂,还需要验证它们在化学反应前后的质量和
(2)图甲中C装置应该选择
(3)分析表格中数据,可以得出相同条件下催化剂的催化效果较好的是
(4)要定量地比较化学反应速度的快慢,除了上述方法外,还可以
【探究二】利用图乙所示装置探究氧气的浓度对燃烧的影响。

【实验方案】点燃蜡烛后立即塞紧橡皮塞,待蜡烛熄灭后,将滴管中的水全部滴入瓶中,铝盒中的白磷立即燃烧。
(5)白磷燃烧的主要现象是
(6)由“蜡烛熄灭,白磷燃烧”可得出的结论是
(7)滴入水后白磷立即燃烧的原因是
小明同学在做家庭实验时,不小心将过氧化氢溶液溅到妈妈刚刚切好的土豆丝上,发现土豆丝上立即冒气泡,激发了小明的探究欲望,请你参与小明的探究。
【猜想】土豆丝可作过氧化氢分解的催化剂
【实验】设计并完成下表所示的探究实验:
(1)请你初小明同学填写如衣中未填完的空格。
(2)在小明的探究实验中,“实验二”起的作用是______ 。
【反思】
(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完全证明猜想是正确的。
第一补充实验:在实验三前后,各对土豆丝进行一次称量,其目的是______ 。
第二补充实验:待实验三无气泡产生,_______ (填操作)。说明土豆丝的化学性质没变。
【结论】
(4)通过上述同学所做的实验,我们知道了土豆丝可以作为过氧化氢制取氧气的催化剂。请写出该反应的化学符号表达式______ 。
【拓展】
(5)下列有关催化剂的说法中不正确的是_______。
【猜想】土豆丝可作过氧化氢分解的催化剂
【实验】设计并完成下表所示的探究实验:
(1)请你初小明同学填写如衣中未填完的空格。
| 实验操作 | 实验现象 | 实验结论 | 总结 | |
| 实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是a | 土豆丝可作过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入土豆丝,伸入带火星的木条 | 没有明显现象 | 水和土豆丝不能放出氧气 | |
| 实验三 | 取5mL5%的过氧化氢溶液于试管中,加入土豆丝,伸入带火星的木条 | b | 土豆丝能加快过氧化氢的分解 |
【反思】
(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完全证明猜想是正确的。
第一补充实验:在实验三前后,各对土豆丝进行一次称量,其目的是
第二补充实验:待实验三无气泡产生,
【结论】
(4)通过上述同学所做的实验,我们知道了土豆丝可以作为过氧化氢制取氧气的催化剂。请写出该反应的化学符号表达式
【拓展】
(5)下列有关催化剂的说法中不正确的是_______。
| A.二氧化锰可以做所有反应的催化剂 |
| B.对很多工业反应,加入催化剂能起到增加生成物的质量的效果 |
| C.有的反应如果没有催化剂就不能进行 |
| D.催化剂能改变化学反应速率,而本身的质量和性质在化学反应前后不发生改变 |
| E.同一个反应可能有多种催化剂 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


