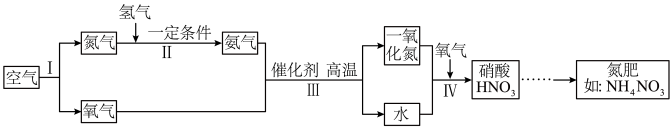
填空与简答-填空题 较易0.85 引用1 组卷43
眼镜是人们常用的护眼工具,如图是一款变色眼镜图片。
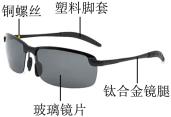
(1)眼镜架上的铜螺丝生锈会生成铜绿【Cu2(OH)2CO3】,铜绿由______________ 种元素组成。
(2)该款变色眼镜的玻璃里加入了溴化银(AgBr)和氧化铜。在强光照射下,溴化银转化为溴和银,玻璃颜色变深,写出该反应的文字表达式______________ ,此反应类型属于______________ 反应:当光线变暗时,溴和银在氧化铜作用下,很快重新生成溴化银,玻璃颜色变浅,氧化铜在反应中起______________ 作用。

(1)眼镜架上的铜螺丝生锈会生成铜绿【Cu2(OH)2CO3】,铜绿由
(2)该款变色眼镜的玻璃里加入了溴化银(AgBr)和氧化铜。在强光照射下,溴化银转化为溴和银,玻璃颜色变深,写出该反应的文字表达式
22-23九年级上·江苏常州·阶段练习
类题推荐
阅读下面的科普短文,回答相关问题:
“远在高空是地球卫士,近在身边是健康杀手。”臭氧(O3)对环境的作用需辩证地认识。
材料一:高空中臭氧层能吸收紫外线,研究人员发现大气层中特别是南极上空的臭氧层日益变薄。进入大气平流层的氯氟烃(一类合成有机化合物,应用于冰箱和空调的制冷剂、灭火器等)是造成臭氧层变薄的主要原因。因为制冷剂氟利昂进入高空大气后会产生氯原子(Cl),引发I、II两个反应:(I) (II)
(II) 。
。
研究表明:平流层中1个氯原子大约可以破坏1×105个臭氧分子。
材料二:地面附近的臭氧是一种空气污染物,其含量过高会对人的呼吸道产生刺激作用,影响肺部功能,还能刺激、损伤眼睛,导致视力下降。
(1)Cl加快了上述转化过程总反应的速率,但自身的质量和化学性质在总反应前后没有发生变化,其作用是______ ,请写出臭氧在一定条件下转化为氧气的符号表达式______ 。
(2)臭氧属于______ (填“单质”或“化合物”),还可以表示一个______ (填“原子”“分子”或“离子”)。
(3)如果近地面处的臭氧含量过高,将直接导致下列哪一类疾病增加?______。
(4)有人提出:你吸入的空气中的某个氧原子可能来自于若干年前恐龙的身体。该说法主要表达的观点是______。(填字母)
“远在高空是地球卫士,近在身边是健康杀手。”臭氧(O3)对环境的作用需辩证地认识。
材料一:高空中臭氧层能吸收紫外线,研究人员发现大气层中特别是南极上空的臭氧层日益变薄。进入大气平流层的氯氟烃(一类合成有机化合物,应用于冰箱和空调的制冷剂、灭火器等)是造成臭氧层变薄的主要原因。因为制冷剂氟利昂进入高空大气后会产生氯原子(Cl),引发I、II两个反应:(I)
研究表明:平流层中1个氯原子大约可以破坏1×105个臭氧分子。
材料二:地面附近的臭氧是一种空气污染物,其含量过高会对人的呼吸道产生刺激作用,影响肺部功能,还能刺激、损伤眼睛,导致视力下降。
(1)Cl加快了上述转化过程总反应的速率,但自身的质量和化学性质在总反应前后没有发生变化,其作用是
(2)臭氧属于
(3)如果近地面处的臭氧含量过高,将直接导致下列哪一类疾病增加?______。
| A.呼吸道疾病 | B.血液传染病 | C.糖尿病 |
| A.分子聚集形成物质,分子在不停地运动 |
| B.在化学变化中原子既不会产生,也不会消失 |
| C.原子内部结构复杂,原子不是构成物质的最小微粒 |
过氧化氢是实验室中重要化学试剂,在生产生活中有重要用途。
(1)某兴趣小组探究过氧化氢溶液的溶质质量分数的大小对反应速率的影响。在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间情况如表:
实验中,二氧化锰在反应中的作用是______ 。
上述实验中,产生氧气的速率最快的是实验______ ,说明______ 。
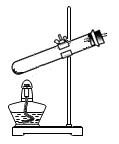
(2)通过查阅资料得知,过氧化氢溶液在70℃以上会较快分解产生氧气。为了验证加热过氧化氢溶液也可以产生氧气,小组同学选择如图装置(气密性良好)进行实验。实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是______ 。同学们分析原因后,采用了排水法收集气体,再检验,证明加热过氧化氢溶液也可产生氧气。
(3)长期放置的油画色彩变暗,是因为生成了黑色的PbS。油画修复的方法是用H2O2将PbS变为白色的PbSO4,其反应方程式为4H2O2+PbS═PbSO4+______ (补充完方程式)。
(1)某兴趣小组探究过氧化氢溶液的溶质质量分数的大小对反应速率的影响。在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间情况如表:
| 实验 | 30%过氧化氢溶液的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| ① | 10 | 40 | 5 | 200 |
| ② | 20 | 30 | 5 | 100 |
| ③ | 30 | 20 | 5 | 67 |
上述实验中,产生氧气的速率最快的是实验
(2)通过查阅资料得知,过氧化氢溶液在70℃以上会较快分解产生氧气。为了验证加热过氧化氢溶液也可以产生氧气,小组同学选择如图装置(气密性良好)进行实验。实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是

(3)长期放置的油画色彩变暗,是因为生成了黑色的PbS。油画修复的方法是用H2O2将PbS变为白色的PbSO4,其反应方程式为4H2O2+PbS═PbSO4+
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网