填空与简答-填空题 适中0.65 引用1 组卷65
根据图示回答下列问题。
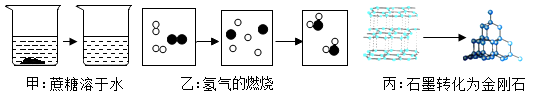
(1)图甲中,从微观角度你获得的一条信息是___________________________________ 。
(2)图乙所示变化从微观角度分析,其实质是________________________ ,该反应的化学方程式为_________________________ ,基本类型为__________________ 。
(3)图丙所示变化,你的微观解释是_________________________________ 。

(1)图甲中,从微观角度你获得的一条信息是
(2)图乙所示变化从微观角度分析,其实质是
(3)图丙所示变化,你的微观解释是
21-22九年级上·内蒙古赤峰·期末
类题推荐
探索物质的组成与结构
I.构建原子模型,认识物质组成规律
为了揭示原子结构的奥秘,人类经历了漫长的探索。
材料一:1803年,道尔顿在原子论中提出:物质由微小的不可再分的原子构成。
材料二:1897年,汤姆生发现原子内有带负电的微粒,否定了“原子不可再分”。
材料三:1911年,卢瑟福进行了著名的α粒子(α粒子由2个质子和2个中子构成)轰击金箔实验。结果发现:绝大多数α粒子穿过金箔后仍沿原方向前进,但是有少数α粒子却发生了较大角度的偏转,并且有极少数α粒子被金箔弹了回来。
材料四:1919年,卢瑟福用加速了的高能α粒子轰击氮原子,发现一个α粒子留在了一个氮原子中,使氮原子变成了氧原子,同时有微粒从氮原子中被打出。
(1)汤姆生实验中,带负电的微粒是______ 。
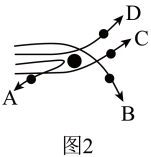
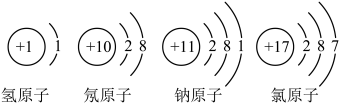
(2)卢瑟福实验中使用的金箔是由______ (填微观粒子的名称)构成的;通过卢瑟福实验,可推出的原子结构模型为______ (填图1中字母)。______ (填图2中字母)。______ 。该过程是否属于化学变化?请结合化学变化的微观本质进行回答:______ 。
(5)万物皆原子,原子是构成一切化学物质的基本单元。______ 。
II.探索分子构成的奥秘
十九世纪初,科学家们提出早期的分子学说,部分观点如下:
观点1:分子不能用物理方法分割,化学方法可使它解离。
观点2:单质分子由同种原子构成,化合物分子由质子数不同的不同种原子构成。
观点3:分子质量大,原子质量小。
观点4:分子质量等于组成它的原子质量总和。
(6)根据以上材料回答问题:
①举例说明观点1是正确的______ 。
②从元素角度谈谈你对观点2的认识______ 。
③举例说明观点3的局限性______ 。
④原子、分子质量很小,为计算和使用方便引入相对原子质量,结合观点4判断下列说法正确的是(填字母序号)_______ 。
A.相对原子质量是采用以小比小使数值变大的计量原理
B.相对原子质量是一个原子质量与一个碳-12原子质量的比值
C.两种原子的相对原子质量之比与相对质量比没有必然联系。
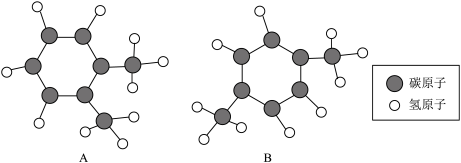
(7)图中A、B是汽油中所含物质的分子结构模型。______ 构成相同(填“元素”、“原子”或“离子”)。你认为A和B的化学性质______ (填“是”或“否”)相同。
III.探究元素与物质组成的奥秘
1783年,拉瓦锡研究水的组成,装置示意图如图,将水加热成蒸气通过灼热的铁管,一段时间后,在出口处收集到一种可燃性气体。实验后称量发现水的质量减少,铁管质量增加。
(9)一定条件下,W在密闭容器内发生反应,反应前后各物质的质量如图所示。______ 。
②组成物质W的元素有______ (填名称),W的化学式为______ 。
③根据物质W的化学式,你可获得哪些信息______ 、______ (请从物质的组成、分子的构成两个方面写出两条)。
④请写出该反应的化学方程式______ 。
I.构建原子模型,认识物质组成规律
为了揭示原子结构的奥秘,人类经历了漫长的探索。
材料一:1803年,道尔顿在原子论中提出:物质由微小的不可再分的原子构成。
材料二:1897年,汤姆生发现原子内有带负电的微粒,否定了“原子不可再分”。
材料三:1911年,卢瑟福进行了著名的α粒子(α粒子由2个质子和2个中子构成)轰击金箔实验。结果发现:绝大多数α粒子穿过金箔后仍沿原方向前进,但是有少数α粒子却发生了较大角度的偏转,并且有极少数α粒子被金箔弹了回来。
材料四:1919年,卢瑟福用加速了的高能α粒子轰击氮原子,发现一个α粒子留在了一个氮原子中,使氮原子变成了氧原子,同时有微粒从氮原子中被打出。
(1)汤姆生实验中,带负电的微粒是
(2)卢瑟福实验中使用的金箔是由

(5)万物皆原子,原子是构成一切化学物质的基本单元。
II.探索分子构成的奥秘
十九世纪初,科学家们提出早期的分子学说,部分观点如下:
观点1:分子不能用物理方法分割,化学方法可使它解离。
观点2:单质分子由同种原子构成,化合物分子由质子数不同的不同种原子构成。
观点3:分子质量大,原子质量小。
观点4:分子质量等于组成它的原子质量总和。
(6)根据以上材料回答问题:
①举例说明观点1是正确的
②从元素角度谈谈你对观点2的认识
③举例说明观点3的局限性
④原子、分子质量很小,为计算和使用方便引入相对原子质量,结合观点4判断下列说法正确的是(填字母序号)
A.相对原子质量是采用以小比小使数值变大的计量原理
B.相对原子质量是一个原子质量与一个碳-12原子质量的比值
C.两种原子的相对原子质量之比与相对质量比没有必然联系。
(7)图中A、B是汽油中所含物质的分子结构模型。
III.探究元素与物质组成的奥秘
1783年,拉瓦锡研究水的组成,装置示意图如图,将水加热成蒸气通过灼热的铁管,一段时间后,在出口处收集到一种可燃性气体。实验后称量发现水的质量减少,铁管质量增加。
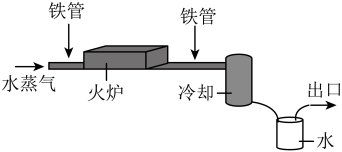
| A.实验中收集到的可燃性气体是氢气 |
| B.铁在该实验中起催化作用 |
| C.实验中水蒸气减少的质量等于铁管增加的质量 |
| D.由该实验可得出“水不是一种元素” |
(9)一定条件下,W在密闭容器内发生反应,反应前后各物质的质量如图所示。
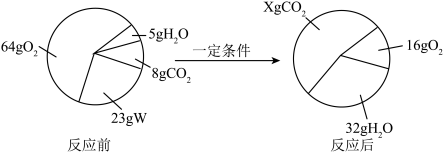
②组成物质W的元素有
③根据物质W的化学式,你可获得哪些信息
④请写出该反应的化学方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网