科学探究题 适中0.65 引用1 组卷51
为了证明MnO2在低温条件下是KClO3发生化学反应的催化剂,某同学进行如下探究:
【提出问题】MnO2在低温下是KClO3的催化剂吗?
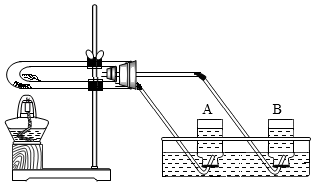
【设计实验】实验室某同学称取一份0.5gMnO2和两份1.5gKClO3并设计如图实验,你认为大试管装___________ ,小试管装___________ ;若实验成功,实验时,A、B两个集气瓶内均有气泡产生,但不同的是___________ 。
【讨论交流】
(1)上述实验探究了催化剂的___________ 性质,在此基础上还要继续探究,实验是___________ 。
(2)在某同学设计的实验结束后,先撤走酒精灯,你会看到的现象是___________ 。请写出实验室用氯酸钾制氧气的符号表达式为___________ ;

【提出问题】MnO2在低温下是KClO3的催化剂吗?
【设计实验】实验室某同学称取一份0.5gMnO2和两份1.5gKClO3并设计如图实验,你认为大试管装
【讨论交流】
(1)上述实验探究了催化剂的
(2)在某同学设计的实验结束后,先撤走酒精灯,你会看到的现象是
21-22九年级上·黑龙江佳木斯·期中
类题推荐
实验室常用双氧水和用二氧化锰作催化剂制取氧气。
【提出问题】
二氧化锰是催化剂,二氧化锰的用量对反应速率是否有影响?
【设计实验】
(1)实验装置如图 1 所示。

(2)测定相关数据记录于下表中:
【分析】
(1)写出该反应的文字表达式______ 。
(2)上述实验应该测定的“待测数据(mL)”可能是______ 。本实验中,测定“待测数据” 的装置(图 2 中方框内)是 ______ (填序号)。
(3)第 II 次实验过氧化氢的体积应为______ mL。
(4)若第Ⅱ次实验比第Ⅲ次实验的“待测数据”更______ (填“大”或“小”),说明催化剂的用量越多,反应越快。二氧化锰可作为该反应的催化剂的依据是:加快该反应的反应速率,反应前后本身的 ______ 和______ 不改变。

【提出问题】
二氧化锰是催化剂,二氧化锰的用量对反应速率是否有影响?
【设计实验】
(1)实验装置如图 1 所示。

(2)测定相关数据记录于下表中:
| 次数 | 过氧化氢体积 (mL) | 过氧化氢浓度 | 二氧化锰质量(g) | 待测数据 (mL) |
| Ⅰ | 30 | 5% | 0.1 | |
| Ⅱ | ________ | 5% | 0.2 | |
| Ⅲ | 30 | 5% | 0.3 |
(1)写出该反应的文字表达式
(2)上述实验应该测定的“待测数据(mL)”可能是
(3)第 II 次实验过氧化氢的体积应为
(4)若第Ⅱ次实验比第Ⅲ次实验的“待测数据”更

某兴趣小组同学对实验室制取氧气的催化剂进行如下探究:
【提出问题】二氧化锰常作为氯酸钾分解制取氧气的催化剂,那其他氧化物是否也能催化氯酸钾分解呢?是否比二氧化锰效果更好?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解(分解释放出热量)有催化作用。
分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
任务一 做出猜想
(1)实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂最好选用的氧化物是_____ ;
(2)作为催化剂必须满足2个条件:
A.改变反应速率。B.物质本身的_____ 和_____ 在化学反应前后保持不变。
任务二 设计并完成实验
I.将3.0g氯酸钾放在试管中加热
II.将3.0g氯酸钾与1.0g二氧化锰混合均匀加热
III.xg氯酸钾与1.0g氧化铜混合均匀加热
【实验现象分析】
(3)将实验III反应后的固体加水溶解、过滤、洗涤、干燥,称量得到1.0g黑色粉末,质量与原来的氧化铜相等,再将黑色粉末和xg氯酸钾混合加热,现象与实验Ⅲ相同。实验中x的数值应为_____ 。实验I和III比较可证明_____ 。
【结论】
(4)氧化铜_____ 作氯酸钾分解的催化剂。(填“能”或“不能”)
任务三 实验反思
(5)实验Ⅱ和III对比的目的是_____ 。
(6)在相同温度下比较两组实验产生氧气的快慢通常可采用的方法有:
①测量相同时间内收集的氧气的体积
②测量_____ 。
【提出问题】二氧化锰常作为氯酸钾分解制取氧气的催化剂,那其他氧化物是否也能催化氯酸钾分解呢?是否比二氧化锰效果更好?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解(分解释放出热量)有催化作用。
分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
| 氧化铁 | 氧化铝 | 氧化铜 | 氧化镁 | |
| 开始反应(℃) | 420 | 515 | 305 | 490 |
| 剧烈反应(℃) | 490 | 540 | 350 | 545 |
(1)实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂最好选用的氧化物是
(2)作为催化剂必须满足2个条件:
A.改变反应速率。B.物质本身的
任务二 设计并完成实验
I.将3.0g氯酸钾放在试管中加热
II.将3.0g氯酸钾与1.0g二氧化锰混合均匀加热
III.xg氯酸钾与1.0g氧化铜混合均匀加热
【实验现象分析】
(3)将实验III反应后的固体加水溶解、过滤、洗涤、干燥,称量得到1.0g黑色粉末,质量与原来的氧化铜相等,再将黑色粉末和xg氯酸钾混合加热,现象与实验Ⅲ相同。实验中x的数值应为
【结论】
(4)氧化铜
任务三 实验反思
(5)实验Ⅱ和III对比的目的是
(6)在相同温度下比较两组实验产生氧气的快慢通常可采用的方法有:
①测量相同时间内收集的氧气的体积
②测量
为研究影响H2O2分解的因素,用如图装置进行实验。
已知:①室温为20℃,水浴时间均为5分钟
②
(1)实验组Ⅰ的目的是________ 。
(2)实验6中设置的水浴温度为________ 。
(3)①对比实验________ 和________ (填序号,从1~8中选择),可知硫酸铜可以加快H2O2分解。
②从以上实验可知,除了加入硫酸铜等催化剂,还可以通过________ 方法加快H2O2分解。
(4)写出实验8中H2O2分解反应的化学方程式________ 。
迁移拓展:
实验Ⅴ:将光亮的粗铜丝灼烧后,迅速伸入盛有10mL30%H2O2溶液和1mL2% H2SO4溶液的试管中(如图)。溶液中立即产生大量气泡,该气体能使带火星的木条复燃。 分解”的证据是否充足?请做出判断,并说明理由:
分解”的证据是否充足?请做出判断,并说明理由:________ 。

已知:①室温为20℃,水浴时间均为5分钟
②
| 实验组号 | 实验序号 | 具支试管内的试剂 | 水浴温度 | 试管内现象 |
| Ⅰ | 1 | 10mL蒸馏水,1mL2%H2SO4溶液 | 20℃ | 无气泡 |
| 2 | 40℃ | 极少量气泡 | ||
| Ⅱ | 3 | 10mL30% H2O2溶液 | 20℃ | 无气泡 |
| 4 | 40℃ | 极少量气泡(比实验2略多) | ||
| Ⅲ | 5 | 10mL30%H2O2溶液,1mL2% H2SO4溶液 | 20℃ | 无气泡 |
| 6 | _____ | 少量气泡 | ||
| Ⅳ | 7 | 10mL30% | 20℃ | 少量气泡 |
| 8 | 40℃ | 大量气泡 |
(1)实验组Ⅰ的目的是
(2)实验6中设置的水浴温度为
(3)①对比实验
②从以上实验可知,除了加入硫酸铜等催化剂,还可以通过
(4)写出实验8中H2O2分解反应的化学方程式
迁移拓展:
实验Ⅴ:将光亮的粗铜丝灼烧后,迅速伸入盛有10mL30%H2O2溶液和1mL2% H2SO4溶液的试管中(如图)。溶液中立即产生大量气泡,该气体能使带火星的木条复燃。
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


