填空与简答-流程题 适中0.65 引用2 组卷113
现有一包白色粉末样品,可能是碳酸钠、硫酸钾、氢氧化钠、氯化钾中的一种或几种,为确定其组成,将适量样品配成溶液,并进行以下实验。根据实验,回答问题。
步骤Ⅰ:取少量样品溶液于试管中,滴入酚酞溶液,溶液由无色变成红色;
步骤Ⅱ:取少量样品溶液于另一支试管中,滴加过量的硝酸钡溶液,有白色沉淀产生,过滤;
步骤Ⅲ:向步骤Ⅱ所得的沉淀中滴入足量的稀盐酸,沉淀部分溶解,并生成气泡;
步骤Ⅳ:取少量步骤Ⅱ所得的滤液于试管中,滴入足量稀硝酸,再滴入硝酸银溶液,振荡,没有明显现象。
(1)写出步骤Ⅲ中生成气泡的反应化学方程式_______ 。
(2)分析上述实验过程,关于样品的组成,可以得到的结论:肯定没有的是_______ (填化学式,下同),肯定有的是_______ 。
步骤Ⅰ:取少量样品溶液于试管中,滴入酚酞溶液,溶液由无色变成红色;
步骤Ⅱ:取少量样品溶液于另一支试管中,滴加过量的硝酸钡溶液,有白色沉淀产生,过滤;
步骤Ⅲ:向步骤Ⅱ所得的沉淀中滴入足量的稀盐酸,沉淀部分溶解,并生成气泡;
步骤Ⅳ:取少量步骤Ⅱ所得的滤液于试管中,滴入足量稀硝酸,再滴入硝酸银溶液,振荡,没有明显现象。
(1)写出步骤Ⅲ中生成气泡的反应化学方程式
(2)分析上述实验过程,关于样品的组成,可以得到的结论:肯定没有的是
2021·广东广州·二模
类题推荐
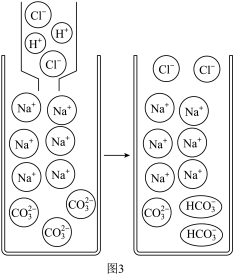
可溶性酸、碱、盐在水中可解离出阴阳离子,我们现阶段所学的复分解反应的实质就是酸、碱、盐解离出的一些阴、阳离子相互结合生成难解离的水、气体或沉淀,根据如下所列溶解性表及氢氧化钠溶液和盐酸反应的微观示意图回答问题。
部分碱和盐的溶解性表(20℃)
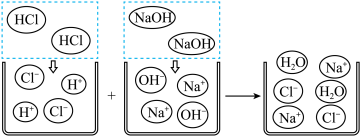
(1)如上图所示,HCl在水中会解离出H+和Cl-,NaOH在水中会解离出Na+和OH-,以此类推H2SO4在水中会解离出的离子是____________ (填离子符号)。
(2)根据上述微观示意图写出化学反应方程式____________ ,判断反应前后溶液中数目发生变化的离子是____________ (填离子符号)。
(3)根据溶解性表及复分解反应的实质判断,将“H2SO4、BaCl2、NaOH、K2CO3”四种物质的溶液两两混合,能发生的反应有________________________ 个。
部分碱和盐的溶解性表(20℃)
阴离子 | 阳离子 | ||
Na+ | K+ | Ba2+ | |
OH- | 溶 | 溶 | 溶 |
SO42- | 溶 | 溶 | 不溶 |
CO32- | 溶 | 溶 | 不溶 |

(1)如上图所示,HCl在水中会解离出H+和Cl-,NaOH在水中会解离出Na+和OH-,以此类推H2SO4在水中会解离出的离子是
(2)根据上述微观示意图写出化学反应方程式
(3)根据溶解性表及复分解反应的实质判断,将“H2SO4、BaCl2、NaOH、K2CO3”四种物质的溶液两两混合,能发生的反应有
铬(Cr)及其化合物在催化金属防腐等方面具有重要应用。铬是一种“氢前金属”,金属活动性介于锌和铜之间。 难溶于水。
难溶于水。
(1)根据金属化学性质的一般规律,下列预测不合理的是_______(填标号)。
(2)催化剂 可由重铬酸铵加热分解制得。
可由重铬酸铵加热分解制得。
①化学方程式
_____  。
。
②重铬酸的化学式为________ 。
(3)设计 转化为
转化为 的方案:
的方案:_______ 。
(1)根据金属化学性质的一般规律,下列预测不合理的是_______(填标号)。
| A.铬能与稀硫酸反应 | B.铬粉中的铜粉可加稀盐酸除去 | C.铬能与氧气反应 |
①化学方程式
②重铬酸的化学式为
(3)设计
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网