科学探究题 较难0.4 引用2 组卷353
今天是化学实验室开放日,小明带着一包脱氧剂和一包食品干燥剂走进实验室,和小组同学一起开始了令人兴奋的探究之旅(忽略实验过程中空气的影响)。
【查阅资料】脱氧剂成分是铁粉、碳粉、碳酸钠、氯化钠,食品干燥剂的成分是生石灰。
探究活动一:脱氧剂脱氧原理
【进行实验】
(1)取适量脱氧剂于大试管中,加足量的水振荡,充分溶解后过滤,得到滤液A和滤渣甲;
(2)向滤渣甲中加入足量稀盐酸,观察到有气泡产生,得到黄色溶液,溶液底部有黑色不溶物。
【得出结论】脱氧剂脱氧的原理是铁粉与______ 发生了化学反应,生成铁锈。写出加入盐酸得到黄色溶液对应的化学方程式______ 。
探究活动二:探究食品干燥剂是否变质
【进行实验】
(1)取一包干燥剂放入小烧杯中,加入适量的水,充分搅拌后,用手触摸烧杯外壁,发烫,过滤,得到滤液B和滤渣乙;
(2)向滤渣乙中加入足量的稀盐酸,可观察到固体全部溶解,有气泡产生,据此判断滤渣乙中有CaCO3。
【得出结论】该干燥剂______ (选填“完全”或“部分”或“没有”)变质。
探究活动三:探究溶液混合后溶质的成分
小组同学将上述实验中的滤液A和滤液B倒入废液缸中,观察到有白色沉淀生成,过滤后得到滤液C,他们对C中溶质的成分进行了探究。
【提出猜想】
猜想一:______ 。
猜想二:NaCl、NaOH、Na2CO3
猜想三:NaCl、NaOH、Ca(OH)2
【进行实验】小明按照自己设计的方案进行了如下实验:
【反思评价】小组同学经过讨论,一致认为根据步骤(2)的现象不足以证明猜想三是正确的,理由是______ 、______ (用化学方程式表示)。
小明经过认真思考后,对步骤(2)进行了修改,并做了下面的实验,最终得出了正确的结论,记录如下、请你完善实验报告。
【查阅资料】脱氧剂成分是铁粉、碳粉、碳酸钠、氯化钠,食品干燥剂的成分是生石灰。
探究活动一:脱氧剂脱氧原理
【进行实验】
(1)取适量脱氧剂于大试管中,加足量的水振荡,充分溶解后过滤,得到滤液A和滤渣甲;
(2)向滤渣甲中加入足量稀盐酸,观察到有气泡产生,得到黄色溶液,溶液底部有黑色不溶物。
【得出结论】脱氧剂脱氧的原理是铁粉与
探究活动二:探究食品干燥剂是否变质
【进行实验】
(1)取一包干燥剂放入小烧杯中,加入适量的水,充分搅拌后,用手触摸烧杯外壁,发烫,过滤,得到滤液B和滤渣乙;
(2)向滤渣乙中加入足量的稀盐酸,可观察到固体全部溶解,有气泡产生,据此判断滤渣乙中有CaCO3。
【得出结论】该干燥剂
探究活动三:探究溶液混合后溶质的成分
小组同学将上述实验中的滤液A和滤液B倒入废液缸中,观察到有白色沉淀生成,过滤后得到滤液C,他们对C中溶质的成分进行了探究。
【提出猜想】
猜想一:
猜想二:NaCl、NaOH、Na2CO3
猜想三:NaCl、NaOH、Ca(OH)2
【进行实验】小明按照自己设计的方案进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少滤液C于试管中,加入足量的氯化钡溶液 | 无明显现象 | 猜想 |
| (2)继续向步骤(1)所得溶液中通入二氧化碳 | 有白色沉淀生成 | 猜想三正确 |
【反思评价】小组同学经过讨论,一致认为根据步骤(2)的现象不足以证明猜想三是正确的,理由是
小明经过认真思考后,对步骤(2)进行了修改,并做了下面的实验,最终得出了正确的结论,记录如下、请你完善实验报告。
| 实验步骤 | 实验现象 | 实验结论 |
| 有白色沉淀生成 | 猜想三正确 |
2022·山东泰安·三模
类题推荐
小丹同学在学习酸的性质时,从同一卷镁带中剪取相等的两根镁带,分别与室温下H+浓度相同的稀盐酸、稀硫酸反应。观察发现:镁带在稀盐酸中放出气泡的速率明显快于在稀硫酸中放出气泡的速率。
【查阅资料】
1、金属与酸发生置换反应,其本质是金属单质与H+反应。
2、生产H2速率主要取决于:①金属的表面积②溶液中H+浓度③温度等条件。
3、H+的浓度与1L溶液中H+数目成正比。
4、溶液中除H+外的其它离子可能会影响反应速率。
【提出问题】
①小丹同学在进行上述实验时,控制了镁带与酸反应的哪几个条件?(回答两条即可)
____________________
②上述反应中Cl-、SO42-如何影响反应速率?
【猜想假设】
Ⅰ、Cl-促进了镁与酸的反应,SO42-对反应无影响。
Ⅱ、SO42-抑制了镁与酸的反应,Cl-对反应无影响。
Ⅲ、________________________________________ 。
请回答问题①,完成猜想Ⅲ。
【实验探究】为了证明猜想,小丹设计了如下实验:
试剂B是_______ (化学式)固体。
【结论】结论A为___________________________________________ 。
【反思】将试剂B改用HCl气体,不能达到实验目的,其原因是________ 。
【查阅资料】
1、金属与酸发生置换反应,其本质是金属单质与H+反应。
2、生产H2速率主要取决于:①金属的表面积②溶液中H+浓度③温度等条件。
3、H+的浓度与1L溶液中H+数目成正比。
4、溶液中除H+外的其它离子可能会影响反应速率。
【提出问题】
①小丹同学在进行上述实验时,控制了镁带与酸反应的哪几个条件?(回答两条即可)
②上述反应中Cl-、SO42-如何影响反应速率?
【猜想假设】
Ⅰ、Cl-促进了镁与酸的反应,SO42-对反应无影响。
Ⅱ、SO42-抑制了镁与酸的反应,Cl-对反应无影响。
Ⅲ、
请回答问题①,完成猜想Ⅲ。
【实验探究】为了证明猜想,小丹设计了如下实验:
| 实验编号 | 铝片长度 | H+浓度相同的酸 | 反应片刻后添加少量试剂 | 产生气泡的速率 | 结论 |
| A | 2cm | 5mL | Na2SO4固体 | 无明显变化 | (结论A) |
| B | 2cm | 5mL | (试剂B) | 明显加快 | Cl-对反应有促进作用 |
试剂B是
【结论】结论A为
【反思】将试剂B改用HCl气体,不能达到实验目的,其原因是
有一包白色固体,可能含有硝酸钡、氢氧化钠、硫酸钠和碳酸钠、氯化钠中的一种或几种,为了探究其组成,某学习小组的同学们设计了如下方案并进行了实验:
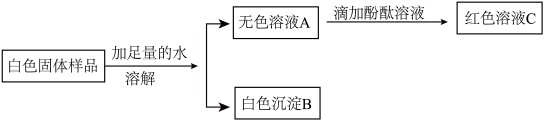
[初步探究]
根据现象可以确定白色固体中一定含有的一种固体是______ 。
[继续探究]
甲同学进行了如下实验:取少量白色沉淀B于试管中,滴加足量稀硝酸,固体质量变化情况如图所示:
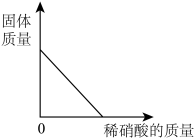
[表达与交流]
甲同学通过上述实验推知:加足量水溶解后白色固体样品中一定发生反应的化学方程式______ 。
乙同学通过红色溶液C,确定白色固体样品中一定含有氢氧化钠。
同学们一致认为乙同学结论不正确。
[深入探究]
丙同学要确定溶液变红的原因,继续实验,他取红色溶液C,请完成下面实验报告。
为确定可能存在的物质是否存在,同学们取红色溶液C,逐滴滴加______ 。溶液变为无色,再滴加_______ 溶液,没有观察到明显现象。
[总结提升]
通过同学们共同努力,最终确定了白色固体成分为______ 。老师为同学们的表现喝彩的同时,又提出了一个新的课题,为节约药品,将无色溶液A中加入适当适量的试剂,充分反应后蒸发结晶可得到一种盐为___________ 。

[初步探究]
根据现象可以确定白色固体中一定含有的一种固体是
[继续探究]
甲同学进行了如下实验:取少量白色沉淀B于试管中,滴加足量稀硝酸,固体质量变化情况如图所示:

[表达与交流]
甲同学通过上述实验推知:加足量水溶解后白色固体样品中一定发生反应的化学方程式
乙同学通过红色溶液C,确定白色固体样品中一定含有氢氧化钠。
同学们一致认为乙同学结论不正确。
[深入探究]
丙同学要确定溶液变红的原因,继续实验,他取红色溶液C,请完成下面实验报告。
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量红色液体C于试管中,加入过量的硝酸钡溶液 | 溶液中出现白色沉淀,且 | C中含有碳酸钠,不含氢氧化钠 |
[总结提升]
通过同学们共同努力,最终确定了白色固体成分为
在一次我区组织的化学实验操作考中某同学制取了一瓶CO2,验满后,将澄清石灰水倒入集气瓶中,充分振荡,发现石灰水没有变浑油,该同学对这个异常现象进行了探究。
【提出问题】澄清石灰水为什么没有变浑油?
【查阅资料】
①CO2过量时,CaCO3沉淀会转化为可溶干水的Ca(HCO3)2;
②CO2在水中溶解度不大;HCl气体很易溶于水;AgCl不溶于稀硝酸。
③CO2在饱和碳酸氢钠溶液中不溶解,也不反应。
【提出猜想】猜想一:石灰水已完全变质;猜想二:_______ ;猜想三:CO2中溶有较多HCl。
【实验方案】该同学用原药品继续制取CO2并进行探究
【实验结论】制败的CO2气体中混入了较多HCl,所以澄清石灰水没有变浑浊。
【文流讨论】若要收集到纯净、干燥的CO2,需将此混合气体依次通入_______ (填溶液名称)和浓硫酸进行洗气。
【拓展思考】该同学用原药品继续制取CO2,但尝试改用排水法收集了一瓶CO2,倒入足量澄清石灰水后,石灰水变浑浊,你认为该实验成功的主要原因是_______ 。
【提出问题】澄清石灰水为什么没有变浑油?
【查阅资料】
①CO2过量时,CaCO3沉淀会转化为可溶干水的Ca(HCO3)2;
②CO2在水中溶解度不大;HCl气体很易溶于水;AgCl不溶于稀硝酸。
③CO2在饱和碳酸氢钠溶液中不溶解,也不反应。
【提出猜想】猜想一:石灰水已完全变质;猜想二:
【实验方案】该同学用原药品继续制取CO2并进行探究
| 步骤 | 实验操作 | 实验现象 | 结论及化学方程式 |
| (1) | 取少量澄清石灰水于试管中,加入MgCl2溶液。 | 猜想Ⅰ不成立, | |
| (2) | 将制取的气体(少量)通入装有足量澄清石灰水的试管中。 | 猜想Ⅱ不成立。 | |
| (3) | 将制取的气体通入盛有硝酸银溶液的试管中,再加足量稀硝酸。 | 试管中有白色沉淀生成 | 猜想Ⅲ成立,反应方程式为 |
【文流讨论】若要收集到纯净、干燥的CO2,需将此混合气体依次通入
【拓展思考】该同学用原药品继续制取CO2,但尝试改用排水法收集了一瓶CO2,倒入足量澄清石灰水后,石灰水变浑浊,你认为该实验成功的主要原因是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


