科学探究题 0.65 引用3 组卷158
碳酸亚铁(FeCO3)能用于制备可溶性乳酸亚铁补血剂。某化学兴趣小组对其制备和性质进行了如下探究。
【查阅资料】
Ⅰ.pH大于8.8时,Fe2+会全转化为Fe(OH)2沉淀。
Ⅱ.FeCO3是白色固体,难溶于水,置于潮湿空气中易变质生成Fe(OH)3,FeCO3与稀盐酸反应的化学方程式为
Ⅲ.FeCl3溶液中滴加KSCN溶液,会出现血红色絮状物;而FeCl2溶液中滴加KSCN溶液,不会出现血红色絮状物。
I:探究新鲜FeCO3的制备
(1)该兴趣小组用pH=11.9的Na2CO3溶液和FeSO4溶液在烧杯中制备FeCO3时,应选用的加料方式是_______ (填字母)。
A.将FeSO4溶液与Na2CO3溶液同时加入到烧杯中
B.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的烧杯中
C.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的烧杯中
(2)制备FeCO3的化学方程式为________ 。
II:探究久置于空气中FeCO3的性质
【提出问题】久置于空气中的FeCO3固体的成分是什么?
【猜想假设】猜想1:只有 FeCO3; 猜想2:FeCO3和Fe(OH)3; 猜想3:________ 。
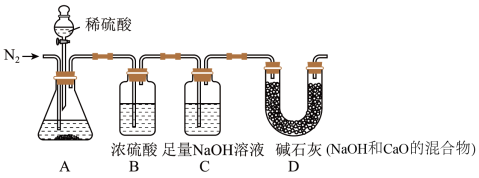
【定量研究】该兴趣小组为进一步确定固体中FeCO3的质量分数,称取10.0g固体做了如图所示的实验。________ 。
(4)实验结束后,测得装置C增重0.44g,则固体中FeCO3 的质量分数为多少?(写出计算过程)_______
(5)关于上述实验过程,下列说法正确的是_______
A.装置A中加入的稀硫酸可用盐酸代替 B.装置B的作用是除去水蒸气
C.如果去掉装置D,会使实验结果偏大 D.反应开始前,也要通入一段时间N2
【查阅资料】
Ⅰ.pH大于8.8时,Fe2+会全转化为Fe(OH)2沉淀。
Ⅱ.FeCO3是白色固体,难溶于水,置于潮湿空气中易变质生成Fe(OH)3,FeCO3与稀盐酸反应的化学方程式为
Ⅲ.FeCl3溶液中滴加KSCN溶液,会出现血红色絮状物;而FeCl2溶液中滴加KSCN溶液,不会出现血红色絮状物。
I:探究新鲜FeCO3的制备
(1)该兴趣小组用pH=11.9的Na2CO3溶液和FeSO4溶液在烧杯中制备FeCO3时,应选用的加料方式是
A.将FeSO4溶液与Na2CO3溶液同时加入到烧杯中
B.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的烧杯中
C.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的烧杯中
(2)制备FeCO3的化学方程式为
II:探究久置于空气中FeCO3的性质
【提出问题】久置于空气中的FeCO3固体的成分是什么?
【猜想假设】猜想1:只有 FeCO3; 猜想2:FeCO3和Fe(OH)3; 猜想3:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,加入足量的稀盐酸 | 固体完全溶解,有气泡产生 | |
| 取少量上述反应后的溶液于试管中,滴加KSCN溶液 | 猜想2成立 |
(4)实验结束后,测得装置C增重0.44g,则固体中FeCO3 的质量分数为多少?(写出计算过程)
(5)关于上述实验过程,下列说法正确的是
A.装置A中加入的稀硫酸可用盐酸代替 B.装置B的作用是除去水蒸气
C.如果去掉装置D,会使实验结果偏大 D.反应开始前,也要通入一段时间N2
2022·江苏无锡·二模


